名校
1 . (1)比较结合H+的能力的相对强弱:C6H5O-___________ CO (填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱
(填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱___________ 。
(2)(CN)2 的性质与氯气相似,又称拟卤素,各原子均满足 8 电子稳定结构。写出 (CN)2 的电子式________ 。
(3)常压下,水的沸点比氟化氢高,其主要原因是___________ 。
 (填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱
(填“>”、“<”或“=”);用一个离子方程式说明 C6H5OH和 H2CO3给出 H+能力的相对强弱(2)(CN)2 的性质与氯气相似,又称拟卤素,各原子均满足 8 电子稳定结构。写出 (CN)2 的电子式
(3)常压下,水的沸点比氟化氢高,其主要原因是
您最近一年使用:0次
2 . (1)甲烷和苯都不能使酸性高锰酸钾溶液褪色,甲苯却可以使其褪色,主要原因是_______ 。
(2)常温下硝酸为液体且易挥发,尿素为固体,两者沸点高低差异的可能原因是_______ 。
(2)常温下硝酸为液体且易挥发,尿素为固体,两者沸点高低差异的可能原因是
您最近一年使用:0次
3 . 下列说法正确的是
A.2克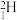 与2克 与2克 所含的质子数相同但中子数不同 所含的质子数相同但中子数不同 |
| B.H2O的沸点比HF高是因为H-O键的极性比H-F键更强 |
| C.金属越纯,机械强度越高,因此纯铁广泛用作结构材料 |
| D.HF为共价化合物,NaH为离子化合物 |
您最近一年使用:0次
2021·浙江·模拟预测
4 . (1)比较得电子能力的相对强弱:
_______ (填“>”“<”或“=”) ;用一个化学方程式说明
;用一个化学方程式说明 和
和 得电子能力的相对强弱:
得电子能力的相对强弱:_______ 。
(2)液态 中存在分子缔合现象,原因是
中存在分子缔合现象,原因是_______ 。

 ;用一个化学方程式说明
;用一个化学方程式说明 和
和 得电子能力的相对强弱:
得电子能力的相对强弱:(2)液态
 中存在分子缔合现象,原因是
中存在分子缔合现象,原因是
您最近一年使用:0次
名校
解题方法
5 . (1)比较给出H+能力的相对强弱:H2O___________ C2H5OH(填“>”“<”或“=”);用一个化学方程式说明OH-和C2H5O-结合H+能力的相对强弱___________ 。
(2) (CN)2称为“拟卤素”,各原子均满足8电子稳定结构。写出(CN)2的电子式___________ 。
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是___________ 。
(2) (CN)2称为“拟卤素”,各原子均满足8电子稳定结构。写出(CN)2的电子式
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是
您最近一年使用:0次
20-21高二下·浙江·阶段练习
6 . (1)已知常压下,乙醇沸点为78.5℃,而与其分子量接近的丙烷的沸点是-42.1℃,两者沸点相差如此之大的主要原因是___________ 。
(2)AlCl3可作净水剂,其理由是___________ (用必要的方程式和相关文字说明)。
(3)丙氨酸的结构简式___________ 。
(2)AlCl3可作净水剂,其理由是
(3)丙氨酸的结构简式
您最近一年使用:0次
解题方法
7 . (1)酸性强弱比较:苯酚___________ 碳酸(填“>”、“=”或“<”),原因(用相应的离子方程式表示):___________ 。
(2)沸点:H2O___________ H2S(填“>”、“=”或“<”),原因___________ 。
(3)实验室欲测定Na2CO3和NaCl混合物中Na2CO3的质量分数ω(Na2CO3),实验步骤如下:称取此固体样品4.350g,溶于适量的水中,配成50mL溶液。取出25mL溶液,加入足量的AgNO3溶液充分反应,得到沉淀的质量为5.575g.则原混合物中ω(Na2CO3)=___________ (保留4位有效数字)。写出简要的计算过程。
(2)沸点:H2O
(3)实验室欲测定Na2CO3和NaCl混合物中Na2CO3的质量分数ω(Na2CO3),实验步骤如下:称取此固体样品4.350g,溶于适量的水中,配成50mL溶液。取出25mL溶液,加入足量的AgNO3溶液充分反应,得到沉淀的质量为5.575g.则原混合物中ω(Na2CO3)=
您最近一年使用:0次
20-21高一下·浙江·阶段练习
8 . 按要求回答下列问题:
(1)实验室制取氯气反应的离子方程式为_______
(2)写出铁与水蒸气反应方程式:_______
(3)某反应为: ,用单线桥表示出该反应中电子转移的方向和数目
,用单线桥表示出该反应中电子转移的方向和数目_______ 。
(4) 中各原子均满足8电子稳定结构。写出
中各原子均满足8电子稳定结构。写出 的电子式
的电子式_______
(5)请解释 的熔沸点高于
的熔沸点高于 的原因
的原因_______
(1)实验室制取氯气反应的离子方程式为
(2)写出铁与水蒸气反应方程式:
(3)某反应为:
 ,用单线桥表示出该反应中电子转移的方向和数目
,用单线桥表示出该反应中电子转移的方向和数目(4)
 中各原子均满足8电子稳定结构。写出
中各原子均满足8电子稳定结构。写出 的电子式
的电子式(5)请解释
 的熔沸点高于
的熔沸点高于 的原因
的原因
您最近一年使用:0次
解题方法
9 . 氧的常见氢化物有H2O与H2O2。
(1)纯净H2O2为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水的原因为_______ 。
(2) H2O2既有氧化性也有还原性,写出一个离子方程式其中H2O2在反应中仅体现还原性_______ 。
(1)纯净H2O2为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水的原因为
(2) H2O2既有氧化性也有还原性,写出一个离子方程式其中H2O2在反应中仅体现还原性
您最近一年使用:0次
解题方法
10 . (1)光学实验证明在溶有O2的水中存在可能为五元环状结构的O2·H2O,原因是___________ 。
(2)化合物A、B、C的熔点如下表:
化合物C的熔点明显高于A的原因是___________ 。
(2)化合物A、B、C的熔点如下表:
| A | B | C | |
| 化学式 | CH3CH2Cl | CH3CH2CH2Cl | CH3NH3Cl |
| 熔点/℃ | -139 | -123 | 230 |
化合物C的熔点明显高于A的原因是
您最近一年使用:0次



