名校
解题方法
1 . 制备 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
(1)基态 价层电子排布式为
价层电子排布式为_______ 。
(2)N、O、S三种元素的第一电离能由大到小的顺序为_______ 。
(3)沸点: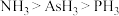 ,原因为
,原因为_______ 。
(4)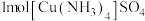 含有σ键的数目为
含有σ键的数目为_______ 。
(5)S与 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:

①该化合物的化学式为_______ 。
②已知该晶胞的晶胞参数为 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为_______  。
。
 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:(1)基态
 价层电子排布式为
价层电子排布式为(2)N、O、S三种元素的第一电离能由大到小的顺序为
(3)沸点:
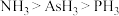 ,原因为
,原因为(4)
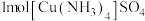 含有σ键的数目为
含有σ键的数目为(5)S与
 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
①该化合物的化学式为
②已知该晶胞的晶胞参数为
 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为 。
。
您最近一年使用:0次
名校
2 . 中国科学家在国际上首次实现了CO2到淀粉的合成,不依赖植物光合作用,原料只需CO2、H2和电,相关成果发表在《科学》上。回答下列问题:
(1)CO2的空间结构为_______ 形,其中C原子的杂化方式为_______ 。
(2)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:_______ 。
(3)淀粉在一定条件下可水解成葡萄糖 ,葡萄糖分子中键角∠H1C1O1
,葡萄糖分子中键角∠H1C1O1_______ ∠C1C2O2 (填“>”、“<”或“=”)。
(4)①(CH3NH3)PbI3的晶胞结构如图所示:

其中B代表Pb2+。则_______ 代表I-,原子分数坐标A为(0,0,0),B为( ,
, ,
, ),则C的原子分数坐标为
),则C的原子分数坐标为_______ 。
②已知(CH3NH3)PbI3的摩尔质量为Mg·mol-1,NA为阿伏加德罗常数的值,则该晶体的密度为_______ g·cm-3。
(1)CO2的空间结构为
(2)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:
(3)淀粉在一定条件下可水解成葡萄糖
 ,葡萄糖分子中键角∠H1C1O1
,葡萄糖分子中键角∠H1C1O1(4)①(CH3NH3)PbI3的晶胞结构如图所示:

其中B代表Pb2+。则
 ,
, ,
, ),则C的原子分数坐标为
),则C的原子分数坐标为②已知(CH3NH3)PbI3的摩尔质量为Mg·mol-1,NA为阿伏加德罗常数的值,则该晶体的密度为
您最近一年使用:0次
2022-09-14更新
|
360次组卷
|
3卷引用:广东省汕头市金山中学2022-2023学年高三上学期开学考试化学试题
名校
3 . 氯化铵是“侯氏制碱法”的副产品,在工农业生产中具有重要用途。回答下列问题:
(1)氯化铵的立方晶胞结构如图所示:

①与 等距离且最近的Cl-有
等距离且最近的Cl-有_______ 个。
②若氯化铵的密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞参数a=
为阿伏加德罗常数的值,则晶胞参数a=_______ nm(用含d、 的代数式表示)。
的代数式表示)。
(2)常温下,用 计测得某
计测得某 溶液的
溶液的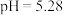 。
。
①用离子方程式表示 溶液呈酸性的原因:
溶液呈酸性的原因:____________ 。
②若溶液中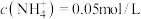 ,则水解常数
,则水解常数
_______ (提示: 和
和 的物质的量浓度几乎相等,
的物质的量浓度几乎相等,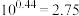 。结果保留2位有效数字)。
。结果保留2位有效数字)。
(3)为探究溶液浓度和 浓度对氯化铵水解的影响,学习小组利用
浓度对氯化铵水解的影响,学习小组利用 溶液和
溶液和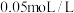 的
的 溶液,按下表配制总体积相同的系列溶液。测定
溶液,按下表配制总体积相同的系列溶液。测定 ,记录数据。
,记录数据。
①补充表中数据:a=_______ 。
②由实验I和II可知,稀释 溶液,
溶液,_______ (填“促进"或“抑制”) 水解,结合表中数据,给出判断理由:
水解,结合表中数据,给出判断理由:_______
③结合表中数据分析 增大,
增大, 水解程度
水解程度_______ (填“增大”、“减小”或“不变”)。
④画出稀释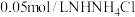 溶液时,
溶液时, 随加入水量的变化曲线图
随加入水量的变化曲线图_______ ,标注出 的变化范围。
的变化范围。
(1)氯化铵的立方晶胞结构如图所示:

①与
 等距离且最近的Cl-有
等距离且最近的Cl-有②若氯化铵的密度为
 ,设
,设 为阿伏加德罗常数的值,则晶胞参数a=
为阿伏加德罗常数的值,则晶胞参数a= 的代数式表示)。
的代数式表示)。(2)常温下,用
 计测得某
计测得某 溶液的
溶液的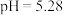 。
。①用离子方程式表示
 溶液呈酸性的原因:
溶液呈酸性的原因:②若溶液中
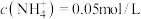 ,则水解常数
,则水解常数
 和
和 的物质的量浓度几乎相等,
的物质的量浓度几乎相等,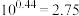 。结果保留2位有效数字)。
。结果保留2位有效数字)。(3)为探究溶液浓度和
 浓度对氯化铵水解的影响,学习小组利用
浓度对氯化铵水解的影响,学习小组利用 溶液和
溶液和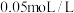 的
的 溶液,按下表配制总体积相同的系列溶液。测定
溶液,按下表配制总体积相同的系列溶液。测定 ,记录数据。
,记录数据。| 序号 | 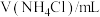 |  | 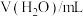 |  |
| I | 20 | 0 | 0 | 5.28 |
| II | 2 | 0 | 18 | 5.78 |
| III | 2 | a | 16 | 5.78 |
| IV | 2 | 10 | 8 | 5.78 |
②由实验I和II可知,稀释
 溶液,
溶液, 水解,结合表中数据,给出判断理由:
水解,结合表中数据,给出判断理由:③结合表中数据分析
 增大,
增大, 水解程度
水解程度④画出稀释
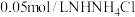 溶液时,
溶液时, 随加入水量的变化曲线图
随加入水量的变化曲线图 的变化范围。
的变化范围。
您最近一年使用:0次
2022-08-05更新
|
225次组卷
|
2卷引用:广东省2023届高三上学期开学联考化学试题
21-22高三上·广东广州·期末
名校
4 . 回答下列问题:
(1)据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
①基态锌原子的电子排布式为___ ,原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为___ 。
②Cd与Zn同族,价电子数相同,若配离子[Cd(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=____ 。
③碲和硫同主族,TeO 的空间构型为
的空间构型为___ ,写出一个与TeO 互为等电子体的分子
互为等电子体的分子___ 。
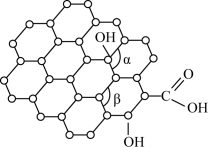
(2)石墨烯是一种二维碳纳米材料,具有优异的光学、力学、电学特性,在材料学、微纳加工、能源、生物医学和药物传递方面具有重要应用前景。1mol石墨烯含六元环的数目为___ ;石墨烯中部分碳原子被氧化后,其平面结构将发生改变,转化为氧化石墨烯(如图),氧化石墨烯中键角α___ (填“>”、“<”或“=”)键角β,原因是___ 。
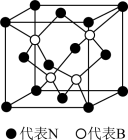
(3)立方氮化硼晶体的结构和硬度都与金刚石相似,晶胞结构如图所示,B原子填在由N原子构成的___ (填“四面体”、“八面体”或“立方体”)空隙中。若晶胞边长为apm,B原子半径为bpm,N原子半径为cpm,则该晶胞的空间利用率为____ (列出计算式),氮硼原子间的最短距离为___ pm。
(1)据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
①基态锌原子的电子排布式为
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的锌原子,其价电子自旋磁量子数的代数和为②Cd与Zn同族,价电子数相同,若配离子[Cd(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=
③碲和硫同主族,TeO
 的空间构型为
的空间构型为 互为等电子体的分子
互为等电子体的分子(2)石墨烯是一种二维碳纳米材料,具有优异的光学、力学、电学特性,在材料学、微纳加工、能源、生物医学和药物传递方面具有重要应用前景。1mol石墨烯含六元环的数目为

(3)立方氮化硼晶体的结构和硬度都与金刚石相似,晶胞结构如图所示,B原子填在由N原子构成的

您最近一年使用:0次
2022-01-23更新
|
612次组卷
|
4卷引用:广东名校2021-2022学年高三下学期开学测试化学试题
广东名校2021-2022学年高三下学期开学测试化学试题(已下线)广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题湖南省长沙市雅礼中学2021-2022学年高三下学期月考(七)化学试题湖南省娄底市2022届高三上学期第二次模拟考试化学试题
解题方法
5 . 下图为钠的某种氧化物D的晶胞和H3BO3(层状结构)的结构示意图。请回答下列问题:


(1)基态硼原子的电子排布图为:_______ 其第一电离能小于Be,原因是_______ 。
(2)三价B易形成多种配离子如[B(OH)4]-、BH 离子[B(OH)4]-的空间构型为
离子[B(OH)4]-的空间构型为_______ 。硼酸显弱酸性与该配离子有关写出硼酸的电离方程式_______ 。写出一种与BH 互为等电子体的分子的电子式
互为等电子体的分子的电子式_______ 。
(3)在硼酸的层状结构中B的杂化类型是_______ 层内存在的作用力有_______ 。
(4)D的化学式为_______ ;晶胞中O原子的配位数为_______ ;已知该晶体F的密度为dg·cm-3,晶胞参数a=_______ nm。


(1)基态硼原子的电子排布图为:
(2)三价B易形成多种配离子如[B(OH)4]-、BH
 离子[B(OH)4]-的空间构型为
离子[B(OH)4]-的空间构型为 互为等电子体的分子的电子式
互为等电子体的分子的电子式(3)在硼酸的层状结构中B的杂化类型是
(4)D的化学式为
您最近一年使用:0次
2021-05-17更新
|
218次组卷
|
2卷引用:广东省2023届高三上学期开学摸底考试化学试题



