名校
1 . 实现废钨-镍型加氢催化剂(主要成分为 、Ni、
、Ni、 ,还含有Fe、
,还含有Fe、 和少量含S有机物)中有价值金属回收的工艺流程如下。
和少量含S有机物)中有价值金属回收的工艺流程如下。
(1)基态Ni的价层电子排布式为______________ 。
(2) “氧化”的目的为______________________ 和将金属单质氧化至相应的价态。
(3)“钠化焙烧”中生成 的化学方程式为
的化学方程式为_____________ 。
(4)“酸化沉钨”后过滤,所得滤饼的主要成分为_______________ (填化学式)。
(5)“调pH”除铁和铝,溶液的pH范围应调节为____________ 。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
“一系列操作”依次是_____________ 、及时过滤、洗涤、干燥。
(7)强碱溶液中NaClO氧化 ,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式为:
,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式为:_______________________ 。
(8)某笼形络合物M[ ]结构中,镍离子与
]结构中,镍离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如
分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如 ),其基本结构如图(H原子未画出)。回答下列问题:
),其基本结构如图(H原子未画出)。回答下列问题:_______ 。
②晶胞的密度为___________  (用代数式表示)。
(用代数式表示)。
 、Ni、
、Ni、 ,还含有Fe、
,还含有Fe、 和少量含S有机物)中有价值金属回收的工艺流程如下。
和少量含S有机物)中有价值金属回收的工艺流程如下。
(1)基态Ni的价层电子排布式为
(2) “氧化”的目的为
(3)“钠化焙烧”中生成
 的化学方程式为
的化学方程式为(4)“酸化沉钨”后过滤,所得滤饼的主要成分为
(5)“调pH”除铁和铝,溶液的pH范围应调节为
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
晶体形态 |
|
| 多种结晶水合物 |
|
(7)强碱溶液中NaClO氧化
 ,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式为:
,可沉淀出用作电池正极材料的NiOOH,该反应的离子方程式为:(8)某笼形络合物M[
 ]结构中,镍离子与
]结构中,镍离子与 连接形成平面层,两个平面层通过
连接形成平面层,两个平面层通过 分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如
分子连接,所有N原子均参与形成配位键,中间的空隙填充大小合适的分子(如 ),其基本结构如图(H原子未画出)。回答下列问题:
),其基本结构如图(H原子未画出)。回答下列问题:
②晶胞的密度为
 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次
2 . 某工业生产上用铜镍矿石(主要成分为 、
、 、
、 、
、 及不溶于酸的杂质)制备胆矾
及不溶于酸的杂质)制备胆矾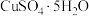 的流程如图。
的流程如图。 ,其萃取原理(org为有机相);
,其萃取原理(org为有机相);
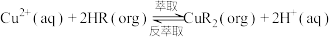
(1)焙烧前粉碎的目的是___________ 。
(2)滤渣2的成分是___________ 。
(3)向“萃取”后的水相中加入一定量的 和
和 ,能制得黑色不溶物
,能制得黑色不溶物 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(4)试剂X的最佳选择是___________ (填字母),“操作Ⅱ”包括___________ 、___________ 、过滤、洗涤和干燥。
a.盐酸 b. 溶液 c.
溶液 c. 溶液 d.
溶液 d.
(5)胆矾 可写成
可写成 ,其结构示意图如下:
,其结构示意图如下: 的核外电子排布式为
的核外电子排布式为___________ 。
②胆矾中含有的粒子间作用力有___________ (填序号)。
a.离子键 b.极性键 c.金属键
d.配位键 e.氢键 f.非极性键
③胆矾受热分解得到铜的某种氧化物,其晶胞结构如上图所示,则该铜氧化合物的化学式为___________ ,氧的配位数是___________ 。
 、
、 、
、 、
、 及不溶于酸的杂质)制备胆矾
及不溶于酸的杂质)制备胆矾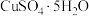 的流程如图。
的流程如图。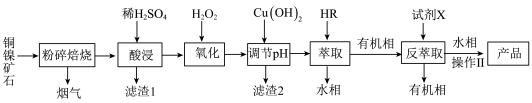
 ,其萃取原理(org为有机相);
,其萃取原理(org为有机相);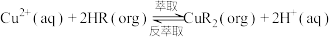
(1)焙烧前粉碎的目的是
(2)滤渣2的成分是
(3)向“萃取”后的水相中加入一定量的
 和
和 ,能制得黑色不溶物
,能制得黑色不溶物 ,该反应的离子方程式为
,该反应的离子方程式为(4)试剂X的最佳选择是
a.盐酸 b.
 溶液 c.
溶液 c. 溶液 d.
溶液 d.
(5)胆矾
 可写成
可写成 ,其结构示意图如下:
,其结构示意图如下: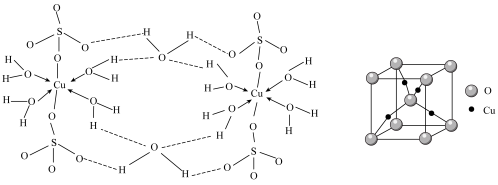
 的核外电子排布式为
的核外电子排布式为②胆矾中含有的粒子间作用力有
a.离子键 b.极性键 c.金属键
d.配位键 e.氢键 f.非极性键
③胆矾受热分解得到铜的某种氧化物,其晶胞结构如上图所示,则该铜氧化合物的化学式为
您最近一年使用:0次
3 . 碳及其化合物广泛存在于自然界中。回答下列问题:
(1)光催化还原CO2制备CH4的反应中,带状纳米Zn2GeO4是该反应的良好催化剂:
①C、H、O的第一电离能由大至小的顺序是________ 。
②Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因为________ 。
(2)在金刚石晶体(晶胞结构如图所示)中:________ 个六元环,六元环中最多有________ 个C原子在同一平面。
②已知金刚石晶体的密度为ρg∙cm-3,NA代表阿伏加德罗常数的值,该晶胞中a与b之间的距离为________ (用含ρ、NA的代数式表示)nm。
③Q原子的参数坐标为________ 。
(3)碳化硅(SiC)晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因为________ 。
(4)HSCN通常有 和
和 两种结构,比较二者沸点的高低并分析原因:
两种结构,比较二者沸点的高低并分析原因:________ 。
(1)光催化还原CO2制备CH4的反应中,带状纳米Zn2GeO4是该反应的良好催化剂:
①C、H、O的第一电离能由大至小的顺序是
②Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因为
(2)在金刚石晶体(晶胞结构如图所示)中:
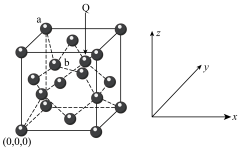
②已知金刚石晶体的密度为ρg∙cm-3,NA代表阿伏加德罗常数的值,该晶胞中a与b之间的距离为
③Q原子的参数坐标为
(3)碳化硅(SiC)晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因为
(4)HSCN通常有
 和
和 两种结构,比较二者沸点的高低并分析原因:
两种结构,比较二者沸点的高低并分析原因:
您最近一年使用:0次
2024-06-02更新
|
44次组卷
|
2卷引用:广东省部分学校2023-2024学年高二下学期期中联考化学试题
名校
解题方法
4 . 高砷烟尘(主要成分有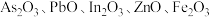 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 ,和金属铟的工业流程如下:
,和金属铟的工业流程如下: 在酸性溶液中以
在酸性溶液中以 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;
② 在
在 易分解为
易分解为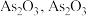 难溶于水;
难溶于水;
③ 。
。
回答下列问题:
(1)滤渣的主要成分为_______ (填化学式)。
(2)“高压酸浸”时, 的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,
时, 的浸出率随硫酸浓度增大而略微减小的原因可能为
的浸出率随硫酸浓度增大而略微减小的原因可能为_______ 。 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ 。已知 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为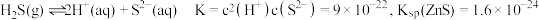 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
_______ 。
(4)“还原”后溶液酸性增强,主要原因是_______ (用离子方程式表示)。
(5)“结晶”操作为_______ 、过滤、洗涤、干燥。
(6)“萃余液”中含有的金属阳离子为_______ (填离子符号),将 溶液电解得到金属铟,阴极的电极反应式为
溶液电解得到金属铟,阴极的电极反应式为_______ 。
(7)硫化铟铜是一种新型的纳米材料,具有优异的光电性能和光催化性能。一种由S、 三种元素组成的化合物的晶胞如图所示。采用
三种元素组成的化合物的晶胞如图所示。采用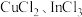 和
和 合成硫化铟铜薄膜,该反应的化学方程式是
合成硫化铟铜薄膜,该反应的化学方程式是_______ ,该晶胞的六个面均为矩形,上、下底面的晶胞参数为 ,高为
,高为 ,晶体密度为
,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为_______ (用含a、b、d的式子表示)。
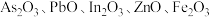 等)属于危险固体废弃物,对高砷烟尘进行综合处理回收
等)属于危险固体废弃物,对高砷烟尘进行综合处理回收 ,和金属铟的工业流程如下:
,和金属铟的工业流程如下: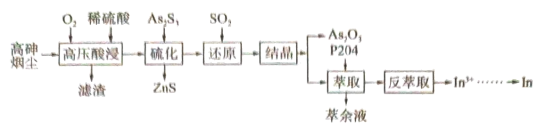
 在酸性溶液中以
在酸性溶液中以 或
或 形式存在,氧化性环境中主要存在
形式存在,氧化性环境中主要存在 ;
;②
 在
在 易分解为
易分解为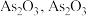 难溶于水;
难溶于水;③
 。
。回答下列问题:
(1)滤渣的主要成分为
(2)“高压酸浸”时,
 的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过
的浸出率随硫酸浓度的增大而变化的曲线如图所示,硫酸浓度超过 时,
时, 的浸出率随硫酸浓度增大而略微减小的原因可能为
的浸出率随硫酸浓度增大而略微减小的原因可能为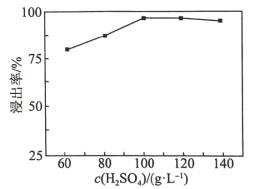
 ,发生反应的离子方程式为
,发生反应的离子方程式为 在水溶液中电离的总反应式为
在水溶液中电离的总反应式为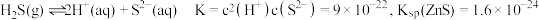 。当“硫化”操作后溶液中
。当“硫化”操作后溶液中 ,则此时溶液的
,则此时溶液的
(4)“还原”后溶液酸性增强,主要原因是
(5)“结晶”操作为
(6)“萃余液”中含有的金属阳离子为
 溶液电解得到金属铟,阴极的电极反应式为
溶液电解得到金属铟,阴极的电极反应式为(7)硫化铟铜是一种新型的纳米材料,具有优异的光电性能和光催化性能。一种由S、
 三种元素组成的化合物的晶胞如图所示。采用
三种元素组成的化合物的晶胞如图所示。采用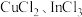 和
和 合成硫化铟铜薄膜,该反应的化学方程式是
合成硫化铟铜薄膜,该反应的化学方程式是 ,高为
,高为 ,晶体密度为
,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
2024-05-31更新
|
167次组卷
|
5卷引用:广东省梅州市部分学校2024届高三下学期5月联考化学试卷
5 . “刀片电池”通过结构创新,大大提升了磷酸铁锂电池的能量密度。以下是以磷矿石(主要成分 ,还有
,还有 、
、 等杂质)为原料生产白磷(
等杂质)为原料生产白磷( )同时制得刀片电池正极材料
)同时制得刀片电池正极材料 的工艺流程:
的工艺流程:
① 难溶于水,可溶于pH<2的酸性溶液。
难溶于水,可溶于pH<2的酸性溶液。
② 在pH大于2.0时开始产生氢氧化物沉淀,pH为4.0时沉淀完全。
在pH大于2.0时开始产生氢氧化物沉淀,pH为4.0时沉淀完全。
回答下列问题:
(1)白磷( )分子呈正四面体形,难溶于水。白磷是
)分子呈正四面体形,难溶于水。白磷是___________ (填“极性分子”或“非极性分子”)。
(2)“炉渣Ⅰ”主要含有铁单质及铁的磷化物,写出一种分离出铁单质的简单方法___________ 。FeP溶于稀硝酸的离子方程式为___________ 。
(3)“炉渣Ⅱ”的主要成分是一种难溶硅酸盐,其化学式为___________ 。
(4)向“溶液Ⅱ”中通入 控制pH在2.0的原因是
控制pH在2.0的原因是___________ 。
(5)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有___________ 个。 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=___________ 。 中铁元素有+2和+3价。
中铁元素有+2和+3价。 价层电子排布式为
价层电子排布式为___________ 。
 ,还有
,还有 、
、 等杂质)为原料生产白磷(
等杂质)为原料生产白磷( )同时制得刀片电池正极材料
)同时制得刀片电池正极材料 的工艺流程:
的工艺流程: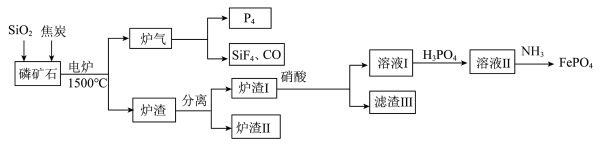
①
 难溶于水,可溶于pH<2的酸性溶液。
难溶于水,可溶于pH<2的酸性溶液。②
 在pH大于2.0时开始产生氢氧化物沉淀,pH为4.0时沉淀完全。
在pH大于2.0时开始产生氢氧化物沉淀,pH为4.0时沉淀完全。回答下列问题:
(1)白磷(
 )分子呈正四面体形,难溶于水。白磷是
)分子呈正四面体形,难溶于水。白磷是(2)“炉渣Ⅰ”主要含有铁单质及铁的磷化物,写出一种分离出铁单质的简单方法
(3)“炉渣Ⅱ”的主要成分是一种难溶硅酸盐,其化学式为
(4)向“溶液Ⅱ”中通入
 控制pH在2.0的原因是
控制pH在2.0的原因是(5)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。
 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有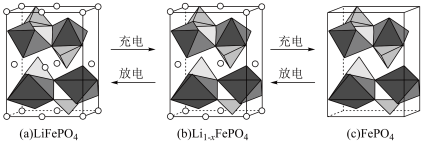
 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x= 中铁元素有+2和+3价。
中铁元素有+2和+3价。 价层电子排布式为
价层电子排布式为
您最近一年使用:0次
名校
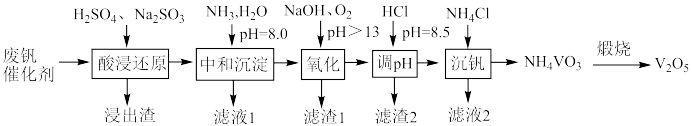
6 . 五氧化二饥广泛用于冶金、化工等行业。某废钒催化剂主要含有 、
、 、CaO、
、CaO、 、
、 、
、 等,采取如下工艺流程回收其中的钒制备
等,采取如下工艺流程回收其中的钒制备 ;
;
回答下列问题:
(1)基态V原子的价电子轨道表示式为________ 。
(2)浸出渣的主要成分是________ ,“酸浸还原”中 ;和
;和 均转化为
均转化为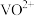 ,写出
,写出 转化为
转化为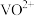 反应的离子方程式为
反应的离子方程式为________ 。
(3)“氧化”中被氧化的元素主要有________ (填元素符号)。
(4)“调pH”中有沉淀生成,写出生成沉淀反应的离子方程式________ 。
(5)“沉钒”中需要加入过量 ,其原因是
,其原因是________ 。 晶体未经洗涤直接进行“煅烧”,将导致
晶体未经洗涤直接进行“煅烧”,将导致 产品中混有
产品中混有________ 杂质。
(6)工艺中可循环利用的物质有________ 。
(7)一定温度下, 溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。
溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。________ 。
②碳化钒晶胞中与碳原子距离最近且相等的碳原子个数为________ 。
③若碳化钒合金的密度为 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则晶胞参数
,则晶胞参数________ nm。
 、
、 、CaO、
、CaO、 、
、 、
、 等,采取如下工艺流程回收其中的钒制备
等,采取如下工艺流程回收其中的钒制备 ;
;
| 金属离子 |  |  |  |  |
开始沉淀时( )的pH )的pH | 12.4 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 13.8 | 4.7 | 3.2 | 9.0 |
(1)基态V原子的价电子轨道表示式为
(2)浸出渣的主要成分是
 ;和
;和 均转化为
均转化为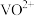 ,写出
,写出 转化为
转化为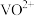 反应的离子方程式为
反应的离子方程式为(3)“氧化”中被氧化的元素主要有
(4)“调pH”中有沉淀生成,写出生成沉淀反应的离子方程式
(5)“沉钒”中需要加入过量
 ,其原因是
,其原因是 晶体未经洗涤直接进行“煅烧”,将导致
晶体未经洗涤直接进行“煅烧”,将导致 产品中混有
产品中混有(6)工艺中可循环利用的物质有
(7)一定温度下,
 溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。
溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。
②碳化钒晶胞中与碳原子距离最近且相等的碳原子个数为
③若碳化钒合金的密度为
 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则晶胞参数
,则晶胞参数
您最近一年使用:0次
7 . 已知元素A、B、C、D、E、F均属前四周期且原子序数依次增大,A的p能级电子数是s能级的一半,C的基态原子 轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能层均排满,且最外层电子数为1。
轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能层均排满,且最外层电子数为1。
请回答下列问题。
(1)C原子基态时电子排布式为______________________________ 。
(2)B、C两种元素第一电离能为__________ >__________(用元素符号表示)。试解释其原因:____________________ 。
(3)任写一种与 离子互为等电子体的离子
离子互为等电子体的离子__________ 。
(4)B与C形成的四原子阴离子的立体构型为__________ ,其中B原子的杂化类型是__________ 。
(5) 难溶于水,易溶于氨水,写出其溶于氨水的离子方程式
难溶于水,易溶于氨水,写出其溶于氨水的离子方程式____________________ 。
(6)D和E形成的化合物的晶胞结构如图,其化学式为____________________ ;
__________ 。已知晶体的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长
,则晶胞边长
_________  。(用
。(用 、
、 的计算式表示)
的计算式表示)
 轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能层均排满,且最外层电子数为1。
轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能层均排满,且最外层电子数为1。请回答下列问题。
(1)C原子基态时电子排布式为
(2)B、C两种元素第一电离能为
(3)任写一种与
 离子互为等电子体的离子
离子互为等电子体的离子(4)B与C形成的四原子阴离子的立体构型为
(5)
 难溶于水,易溶于氨水,写出其溶于氨水的离子方程式
难溶于水,易溶于氨水,写出其溶于氨水的离子方程式(6)D和E形成的化合物的晶胞结构如图,其化学式为

 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长
,则晶胞边长
 。(用
。(用 、
、 的计算式表示)
的计算式表示)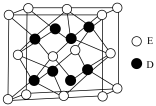
您最近一年使用:0次
解题方法
8 . 砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水[砷主要以亚砷酸(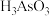 )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
Ⅰ. ;
;
Ⅱ.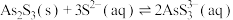 ;
;
Ⅲ.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;
Ⅳ.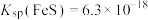 ,
, 。
。
回答下列问题;
(1)“沉砷”时,亚砷酸转化为 的化学方程式为
的化学方程式为_____________________________ 。
(2)“沉砷”时产生的废气可用______________ 溶液吸收处理(填化学式)。
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是_________ (填化学式);此时溶液中存在平衡: ,该反应的平衡常数K=
,该反应的平衡常数K=_____________ (保留2位小数)。
(4)向滤液Ⅱ中通入氧气进行“氧化脱硫”,反应的离子方程式为_____________________ 。
(5)“沉砷”过程中FeS不可用过量的 替换,原因是
替换,原因是 ______________________________ (从平衡移动的角度解释)。
(6)该流程最后一步用 “还原”砷酸,发生反应的化学方程式为
“还原”砷酸,发生反应的化学方程式为____________________ 。
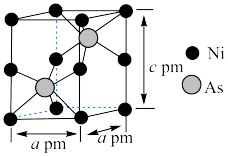
(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为a pm、a pm、c pm,则该晶体的密度为_______  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
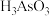 )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下: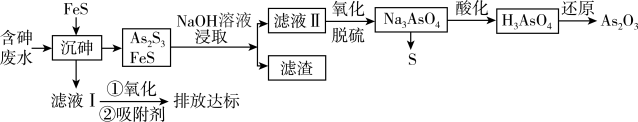
Ⅰ.
 ;
;Ⅱ.
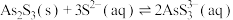 ;
;Ⅲ.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;Ⅳ.
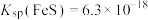 ,
, 。
。回答下列问题;
(1)“沉砷”时,亚砷酸转化为
 的化学方程式为
的化学方程式为(2)“沉砷”时产生的废气可用
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是
 ,该反应的平衡常数K=
,该反应的平衡常数K=(4)向滤液Ⅱ中通入氧气进行“氧化脱硫”,反应的离子方程式为
(5)“沉砷”过程中FeS不可用过量的
 替换,原因是
替换,原因是 (6)该流程最后一步用
 “还原”砷酸,发生反应的化学方程式为
“还原”砷酸,发生反应的化学方程式为(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为a pm、a pm、c pm,则该晶体的密度为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
解题方法
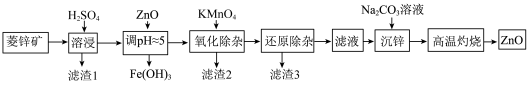
9 . 工业上可由菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示:
②弱酸性溶液中KMnO4氧化Mn2+时,产物中含Mn元素物质只有MnO2。
③氧化性强弱顺序:Ni2+>Cd2+>Zn2+。
④相关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)基态Zn原子的价电子排布式为___________ ,ZnO溶于氨水生成[Zn(NH3)4]2+,1 mol [Zn(NH3)4]2+共有___________ mol的σ键。
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是___________ 。(写一条即可)
②“调pH”时,可替代ZnO的一种含锌化合物是___________ 。(用化学式表示)
③“调pH”时,若pH=5.5,此时溶液中Zn2+的最大浓度c=___________ mol/L。
(3)写出“氧化除杂”时KMnO4溶液与Mn2+反应的离子方程式___________ 。
(4)“还原除杂”除去的离子是___________ ,加入的还原剂是___________ 。
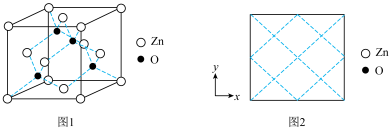
(5)“沉锌”时生成ZnCO3·2Zn(OH)2·2H2O (碱式碳酸锌)沉淀,该沉淀“高温灼烧”后获得ZnO。氧化锌的一种晶体的晶胞是立方晶胞(如图1所示),其中与锌原子距离最近的O原子数有___________ 个,请在图2中画出该晶胞沿z轴方向的平面投影图___________ 。
②弱酸性溶液中KMnO4氧化Mn2+时,产物中含Mn元素物质只有MnO2。
③氧化性强弱顺序:Ni2+>Cd2+>Zn2+。
④相关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ | Mn2+ | Ni2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.0 | 7.4 | 8.1 | 6.9 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.0 | 9.4 | 10.1 | 8.9 |
(1)基态Zn原子的价电子排布式为
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是
②“调pH”时,可替代ZnO的一种含锌化合物是
③“调pH”时,若pH=5.5,此时溶液中Zn2+的最大浓度c=
(3)写出“氧化除杂”时KMnO4溶液与Mn2+反应的离子方程式
(4)“还原除杂”除去的离子是
(5)“沉锌”时生成ZnCO3·2Zn(OH)2·2H2O (碱式碳酸锌)沉淀,该沉淀“高温灼烧”后获得ZnO。氧化锌的一种晶体的晶胞是立方晶胞(如图1所示),其中与锌原子距离最近的O原子数有
您最近一年使用:0次
名校
10 . 铁和硒(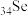 )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,根据要求回答问题。
)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,根据要求回答问题。
 .乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式(图一)和硒在元素周期表中相对位置关系(图二)如图所示。
.乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式(图一)和硒在元素周期表中相对位置关系(图二)如图所示。___________ 。单质硒的熔点为221℃,其晶体类型是___________ 。
(2)乙烷硒啉分子中核磁共振氢普中有___________ 组峰。
(3)根据元素周期律:
①S、As和Se电负性由大到小的顺序:___________ 。
②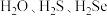 中沸点最高的是:
中沸点最高的是:___________ ,原因是___________ 。
 .黄铁矿是制取硫酸的主要原料,其主要成分为
.黄铁矿是制取硫酸的主要原料,其主要成分为 ,其中铁元素显
,其中铁元素显 价,
价, 晶体的晶胞形状为立方体,晶胞结构如图所示。
晶体的晶胞形状为立方体,晶胞结构如图所示。 ,
, 分子的空间构型为
分子的空间构型为___________ 。
(5)晶胞中与每个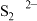 距离最近且相等的
距离最近且相等的 有
有___________ 个。
(6) 晶体的晶胞边长为anm,
晶体的晶胞边长为anm, 的摩尔质量为
的摩尔质量为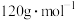 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该
,该 晶体的密度
晶体的密度
___________  (
( 用含a、
用含a、 的代数式表示)
的代数式表示)
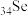 )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,根据要求回答问题。
)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,根据要求回答问题。 .乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式(图一)和硒在元素周期表中相对位置关系(图二)如图所示。
.乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式(图一)和硒在元素周期表中相对位置关系(图二)如图所示。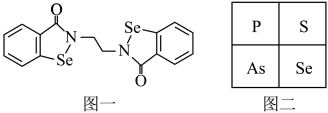
(2)乙烷硒啉分子中核磁共振氢普中有
(3)根据元素周期律:
①S、As和Se电负性由大到小的顺序:
②
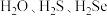 中沸点最高的是:
中沸点最高的是: .黄铁矿是制取硫酸的主要原料,其主要成分为
.黄铁矿是制取硫酸的主要原料,其主要成分为 ,其中铁元素显
,其中铁元素显 价,
价, 晶体的晶胞形状为立方体,晶胞结构如图所示。
晶体的晶胞形状为立方体,晶胞结构如图所示。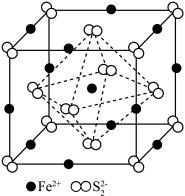
 ,
, 分子的空间构型为
分子的空间构型为(5)晶胞中与每个
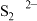 距离最近且相等的
距离最近且相等的 有
有(6)
 晶体的晶胞边长为anm,
晶体的晶胞边长为anm, 的摩尔质量为
的摩尔质量为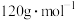 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该
,该 晶体的密度
晶体的密度
 (
( 用含a、
用含a、 的代数式表示)
的代数式表示)
您最近一年使用:0次





