1 . 氮化碳是新发现的高硬度材料,其部分结构如下图所示。下列有关其说法不 正确的是
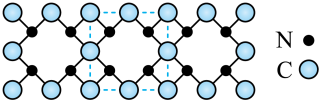
| A.氮化碳属于共价晶体 |
B.氮化碳中碳显 价,氮显 价,氮显 价 价 |
| C.氮化碳的硬度比金刚石略大 |
| D.氮化碳中C原子和N原子的最外层都满足8电子稳定结构 |
您最近一年使用:0次
2 . 周期表中ⅢA族单质及其化合物应用广泛。 极易水解生成
极易水解生成 (
( 在水中完全电离为
在水中完全电离为 和
和 )和硼酸(
)和硼酸( ),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯
),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯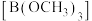 ,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下
,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下 和焦炭在氯气的氛围中获得
和焦炭在氯气的氛围中获得 。
。 的结构与晶体硅类似,是第三代半导体研究的热点。铊(
的结构与晶体硅类似,是第三代半导体研究的热点。铊( )位于元素周期表中第6周期,于1861年发现。下列说法正确的是
)位于元素周期表中第6周期,于1861年发现。下列说法正确的是
 极易水解生成
极易水解生成 (
( 在水中完全电离为
在水中完全电离为 和
和 )和硼酸(
)和硼酸( ),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯
),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯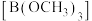 ,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下
,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下 和焦炭在氯气的氛围中获得
和焦炭在氯气的氛围中获得 。
。 的结构与晶体硅类似,是第三代半导体研究的热点。铊(
的结构与晶体硅类似,是第三代半导体研究的热点。铊( )位于元素周期表中第6周期,于1861年发现。下列说法正确的是
)位于元素周期表中第6周期,于1861年发现。下列说法正确的是A. 中存在配位键 中存在配位键 |
B. 分子间能形成氢键 分子间能形成氢键 |
C. 原子基态外围电子排布式为 原子基态外围电子排布式为 |
D. 属于离子晶体 属于离子晶体 |
您最近一年使用:0次
2023-02-10更新
|
844次组卷
|
3卷引用:江苏省苏州市2022-2023学年高三上学期学业质量阳光指标调研化学试题
江苏省苏州市2022-2023学年高三上学期学业质量阳光指标调研化学试题(已下线)专题卷20 《物质结构与性质》选择题分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)广东省湛江市普通高中2023届高三下学期4月模拟考试化学试题
3 . 化学反应过程中既有物质变化,又有能量变化。释放或吸收热量是化学反应中能量变化的主要形式之一
(1)甲烷具有较大的燃烧热( ),是常见燃料。请写出甲烷燃烧的热化学反应方程式
),是常见燃料。请写出甲烷燃烧的热化学反应方程式_______ 。
(2)①工业上高纯硅可通过下列反应制取: 该反应的反应热
该反应的反应热
_______  。
。
已知:
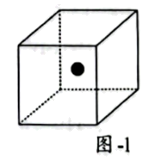
②硅晶体结构与金刚石类似。题图-1所示立方体体心的“●”表示晶体中的一个Si原子,请在立方体的顶点用“●”表示出与之紧邻的所有硅原子。________
(3)自发热材料在生活中的应用日益广泛。某实验小组为探究“CaO-Al- ”体系的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值(
”体系的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值( )随时间(t)的变化曲线,如图-2所示。
)随时间(t)的变化曲线,如图-2所示。
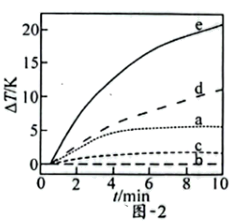
已知:I.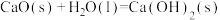
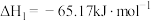
II.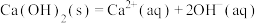
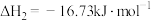
III.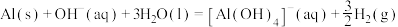
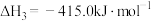
①实验b中, 的变化说明Al粉与
的变化说明Al粉与 在该条件下
在该条件下_______ (填“反应”或“不反应”)。
②实验c中,前3min的 有变化,其原因是
有变化,其原因是_______ ;3min后 基本不变,其原因是
基本不变,其原因是_______ 。
③实验d在10min内温度持续升高的原因是_______ 。
④实验e中发生的总反应可表示为: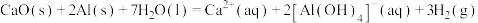 ,其
,其
_______ 。
五组实验对比,e放热效果最好。
(1)甲烷具有较大的燃烧热(
 ),是常见燃料。请写出甲烷燃烧的热化学反应方程式
),是常见燃料。请写出甲烷燃烧的热化学反应方程式(2)①工业上高纯硅可通过下列反应制取:
 该反应的反应热
该反应的反应热
 。
。已知:
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
键能/ | 360 | 436 | 431 | 176 |
②硅晶体结构与金刚石类似。题图-1所示立方体体心的“●”表示晶体中的一个Si原子,请在立方体的顶点用“●”表示出与之紧邻的所有硅原子。

(3)自发热材料在生活中的应用日益广泛。某实验小组为探究“CaO-Al-
 ”体系的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值(
”体系的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值( )随时间(t)的变化曲线,如图-2所示。
)随时间(t)的变化曲线,如图-2所示。| 实验编号 | 反应物组成 |
| a | 0.20gCaO粉末、5.0mL |
| b | 0.15gAl粉、5.0mL |
| c | 0.15gAl粉、5.0mL饱和石灰水 |
| d | 0.15gAl粉、5.0mL石灰乳 |
| e | 0.15gAl粉、0.20gCaO粉末 5.0mL |

已知:I.
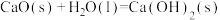
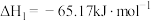
II.
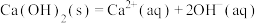
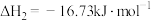
III.
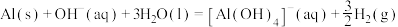
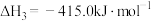
①实验b中,
 的变化说明Al粉与
的变化说明Al粉与 在该条件下
在该条件下②实验c中,前3min的
 有变化,其原因是
有变化,其原因是 基本不变,其原因是
基本不变,其原因是③实验d在10min内温度持续升高的原因是
④实验e中发生的总反应可表示为:
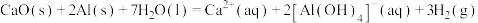 ,其
,其
五组实验对比,e放热效果最好。
您最近一年使用:0次
解题方法
4 . 下列说法中错误的是


A.从CH4、 、 、 为正四面体结构,可推测 为正四面体结构,可推测 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.金属能导电是因为内部的自由电子在外加电场作用下可发生定向移动 |
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
5 . 下列各组物质的晶体类型相同,物质发生状态变化所克服的相互作用也相同的是
| A.SO2和HCl | B.KCl和Mg | C.CCl4和SiO2 | D.NaCl和H2O |
您最近一年使用:0次
2022-04-21更新
|
123次组卷
|
7卷引用:江苏省苏州市相城区陆慕高级中学2021-2022学年高二下学期第一次月考化学试题
江苏省苏州市相城区陆慕高级中学2021-2022学年高二下学期第一次月考化学试题(已下线)2010—2011学年浙江省杭州二中高一下学期期中考试化学试卷江苏宿迁泗阳县众兴中学2021届高三上学期调研考试化学试题(已下线)第38讲 晶体结构与性质(精讲)-2022年一轮复习讲练测(已下线)专题4.3.2 共价键(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)河南省郑州市十校2021-2022学年高二下学期期中联考化学试题黑龙江省绥化市第九中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
6 . 下面的排序不正确的是
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al |
| D.晶格能由大到小:NaF>NaCl>NaBr>NaI |
您最近一年使用:0次
2021-05-29更新
|
576次组卷
|
29卷引用:江苏省苏州市新区实验中学2020-2021学年高二上学期12月月考化学试题
江苏省苏州市新区实验中学2020-2021学年高二上学期12月月考化学试题(已下线)2011-2012学年福建省晋江市季延中学高二上学期期末考试化学试卷(已下线)2012-2013学年福建省莆田一中高二下学期第一学段考试化学试卷2014-2015学年辽宁实验中学等五校高二下期末化学试卷2015-2016学年四川省雅安市高二上学期期末考试化学试卷2015-2016学年福建省福安八中高二下第二次月考化学试卷2015-2016学年福建省四地六校高二下第二次联考化学试卷2015-2016学年宁夏银川一中高二下期末化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷福建省莆田市第一中学2016-2017学年高二下学期期中考试化学试题福建省莆田市仙游县第二中学2019-2020学年高二下学期期中考试化学试题辽宁省大连市普兰店市第三十八中学2021届高三第一学期开学考试化学试题福建省龙岩市武平县第一中学2020-2021学年高二上学期10月月考化学试题湖北省黄梅国际育才高级中学2020-2021学年高二下学期3月月考化学试题辽宁省海城市高中教育集团2019-2020学年高二下学期6月联考化学试题新疆新源县第二中学2018-2019学年高二下学期期末考试化学试题福建省仙游县枫亭中学2020-2021学年高二下学期期中考试化学试题陕西省宝鸡市渭滨区2020-2021学年高二下学期期末考试化学试题河南省驻马店市新蔡县第一高级中学2021-2022学年高二下学期5月半月考化学试题福建省福州第一中学2021-2022学年高二下学期期中考试化学试题新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题福建省泉州市泉港区第五中学等校2021-2022学年高二下学期期末联考化学试题福建省泉州市泉港区第五中学等校2021-2022学年高二下学期期末联考化学试题江苏省盐城市田家炳中学2021-2022学年高二下学期期中考试化学试题天津市滨海新区塘沽第一中学2023届高三第一次月考化学试题(已下线)化学(上海B卷)-学易金卷:2023年高考第一次模拟考试卷四川省盐亭中学2022-2023学年高二上学期期中教学质量监测(理科)化学试题江苏省常州高级中学2023-2024学年高二上学期期末质量检查化学试题(已下线)热点08 金属晶体和离子晶体
解题方法
7 . 下列判断错误的是
| A.碳碳键的键长:C2H4>C2H2 |
| B.晶体的熔点:SiO2>CO2 |
| C.晶格能的大小:NaF>MgO |
| D.金属键的强弱:Li>K |
您最近一年使用:0次
解题方法
8 . 原子序数依次增大的A、B、C、D、E、F、G七种元素。其中A的原子有5种不同运动状态的电子;B的基态原子有3个不同的能级,各能级中的电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;E为它所在周期中原子半径最大的主族元素;F和D位于同一主族,G的原子序数为29。
(1)基态G原子的价电子排布式为__ 。
(2)元素B、C的简单气态氢化物的沸点较高的是__ (用化学式表示)。
(3)A晶体熔点为2300℃,则其为__ 晶体。
(4)GD在加热条件下容易转化为G2D,从原子结构的角度解释原因__ 。
(5)G与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸盐,为将生成的两种气体(气体相对分子质量均小于50)完全转化为最高价含氧酸盐,消耗了1molO2和1L2.2mol/LNaOH溶液。则两种气体的分子式及物质的量分别为__ ,生成硫酸铜物质的量为__ 。
(1)基态G原子的价电子排布式为
(2)元素B、C的简单气态氢化物的沸点较高的是
(3)A晶体熔点为2300℃,则其为
(4)GD在加热条件下容易转化为G2D,从原子结构的角度解释原因
(5)G与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸盐,为将生成的两种气体(气体相对分子质量均小于50)完全转化为最高价含氧酸盐,消耗了1molO2和1L2.2mol/LNaOH溶液。则两种气体的分子式及物质的量分别为
您最近一年使用:0次
2020-07-18更新
|
77次组卷
|
2卷引用:江苏省苏州市园区苏大附中2020-2021学年高二上学期10月月考化学试题
9 . 下列关于C、Si及其化合物结构与性质的论述错误的是
A.键能 、 、 ,因此C2H6稳定性大于Si2H6 ,因此C2H6稳定性大于Si2H6 |
| B.立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度 |
| C.SiH4中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH4 |
D.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成 键 键 |
您最近一年使用:0次
2020-07-11更新
|
7497次组卷
|
37卷引用:江苏省苏州市2022-2023学年高二上学期期中调研化学试卷
江苏省苏州市2022-2023学年高二上学期期中调研化学试卷2020年山东省高考化学试卷(新高考)(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编河南省长葛市第一高级中学2021届高三上学期10月阶段性测试化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题四川省乐山十校2020-2021学年高二上学期半期联考化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)河北省石家庄市第二十四中学2021届高三上学期月考化学试卷(人教版2019)选择性必修2 第三章 晶体结构与性质 C 高考挑战区(已下线)热点4 物质结构与性质(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练山东省夏津第一中学2020-2021学年高二下学期3月月考化学试题(已下线)押山东卷第04题 物质结构与性质选择题-备战2021年高考化学临考题号押题(山东卷)福建省福州第一中学2020-2021学年高二下学期期中考试化学试题(已下线)考点35 晶体结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题13 物质结构与性质基础-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)福建省厦门集美中学2021-2022学年高二下学期第一次月考化学试题(已下线)卷14 物质结构与性质选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷08题 物质结构与性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)卷03 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)2020年山东卷化学高考真题变式题1-10抚顺市第一中学2021-2022学年高二下学期开学考试化学试题河南省南阳市第六完全学校高级中学2021-2022学年高二下学期4月月考化学试题四川省安岳县兴隆中学2021-2022学年高二上学期期中测试化学试题江西省景德镇一中2022-2023学年高二上学期期中考试化学试题四川省乐山沫若中学2022-2023学年高二上学期第二次月考(期中考试)化学试题福建省厦门市湖滨中学2022-2023学年高三上学期期中考试化学试题山东省菏泽市单县二中2021-2022学年高二下学期开学考试 化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第五章 物质结构与性质 元素周期律 第31讲 晶体结构与性质北京市第八十中学2023届高三下学期二模适应考试化学试题广东广雅中学2022-2023学年高二下学期期中考试化学试题广东省湛江市第二中学2021-2022学年高二下学期第17周(6.11)周练化学试题(已下线)第3讲 化学键 共价键的类型及键参数宁夏回族自治区银川市贺兰县第一中学2023-2024学年高三第三阶段化学考试
10 . 有关晶体的叙述正确的是( )
| A.在24 g石墨中,含C-C共价键键数为3 mol |
| B.在12 g金刚石中,含C-C共价键键数为4 mol |
| C.在60 g二氧化硅中,含Si-O共价键键数为4 mol |
| D.在NaCl晶体中,与Na+最近且距离相等的Na+有6个 |
您最近一年使用:0次



