名校
解题方法
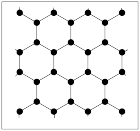
1 . 石墨烯是一种由碳原子构成的正六边形呈蜂巢晶格的二维碳纳米材料,其厚度为单原子量级,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。( 为阿伏加德罗常数的数值)
为阿伏加德罗常数的数值)
(1)写出基态碳原子的电子排布式_______ ,石墨烯中C的杂化类型为_______ 。
(2)在下图中画出石墨烯的最小重复结构单元_______ 。12 g的石墨烯中由 原子连接成的六元环的数目为
原子连接成的六元环的数目为_______ 。
(3)石墨烯加氢制得的石墨烷,可用 表示。下列有关叙述正确的是
表示。下列有关叙述正确的是_______ 。
a.石墨烯属于烯烃 b.石墨烯中所有碳原子共平面
c.石墨烷可以发生加成反应 d.石墨烷难溶于水
(4)电负性数值如下表
① 与
与 结构相似,分子的空间结构均为
结构相似,分子的空间结构均为_______ ,但性质不同:前者不易与水反应但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:_______ 。
② 的晶体结构与金刚石类似。
的晶体结构与金刚石类似。 的晶体类型为
的晶体类型为_______ ,晶体中 原子与
原子与 键的数目之比为
键的数目之比为_______ 。
③石墨烯可由加热 晶体脱除
晶体脱除 的方法制得,该过程属于
的方法制得,该过程属于_______ 。
a.物理变化 b.分解反应 c.氧化还原反应
 为阿伏加德罗常数的数值)
为阿伏加德罗常数的数值)(1)写出基态碳原子的电子排布式
(2)在下图中画出石墨烯的最小重复结构单元
 原子连接成的六元环的数目为
原子连接成的六元环的数目为
(3)石墨烯加氢制得的石墨烷,可用
 表示。下列有关叙述正确的是
表示。下列有关叙述正确的是a.石墨烯属于烯烃 b.石墨烯中所有碳原子共平面
c.石墨烷可以发生加成反应 d.石墨烷难溶于水
(4)电负性数值如下表
| 元素 | H | C | Si |
| 电负性 | 2.1 | 2.5 | 1.8 |
 与
与 结构相似,分子的空间结构均为
结构相似,分子的空间结构均为②
 的晶体结构与金刚石类似。
的晶体结构与金刚石类似。 的晶体类型为
的晶体类型为 原子与
原子与 键的数目之比为
键的数目之比为③石墨烯可由加热
 晶体脱除
晶体脱除 的方法制得,该过程属于
的方法制得,该过程属于a.物理变化 b.分解反应 c.氧化还原反应
您最近一年使用:0次
名校
解题方法
2 . 碳化物衍生碳以其独特的性能被广泛应用在超级电容器、催化剂载体等方面。常用氯气刻蚀法制备。该方法通过高温氯化2小时在SiC表面制备碳涂层(已知: 的沸点是59℃,极易水解),其方法如图:
的沸点是59℃,极易水解),其方法如图:

(1)圆底烧瓶A中为氯酸钾固体,仪器a中的试剂是______________________ ,A中发生反应的化学方程式为__________________ 。
(2)仪器C中所盛物质为_______________ 。
(3)高温环境氯气与氩气混合气氛中氯气与SiC反应,将Si原子从SiC中刻蚀掉形成碳层,反应的化学方程式为__________________ ,如果温度超过1175℃,涂层上的碳结构发生如下变化:碳→骨架碳→非晶碳→石墨碳,则碳涂层硬度会______________ (填“逐渐变高”或“逐渐变低”),SiC熔点远高于 的原因是
的原因是__________________ 。
(4)装置F的作用是__________________ ,NaOH溶液中生成的盐除了NaCl外,还有__________________ 。
 的沸点是59℃,极易水解),其方法如图:
的沸点是59℃,极易水解),其方法如图:
(1)圆底烧瓶A中为氯酸钾固体,仪器a中的试剂是
(2)仪器C中所盛物质为
(3)高温环境氯气与氩气混合气氛中氯气与SiC反应,将Si原子从SiC中刻蚀掉形成碳层,反应的化学方程式为
 的原因是
的原因是(4)装置F的作用是
您最近一年使用:0次
2022-11-19更新
|
367次组卷
|
2卷引用:重庆市第八中学2023届高三上学期适应性月考卷(三)化学试题
2022高三·全国·专题练习
解题方法
3 . 填空。
(1)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为_______ ,微粒间存在的作用力是_______ ,SiC和晶体Si的熔、沸点高低顺序是_______ 。
(2)氧化物MO的电子总数与SiC的相等,则M为_______ (填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是_______ 。
(3)C、Si为同一主族的元素,CO2和SiO2的化学式相似,但结构和性质有很大的不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成π键。从原子半径大小的角度分析,C、O原子间能形成π键,而Si、O原子间不能形成π键的原因是____ 。SiO2属于___ 晶体,CO2属于_____ 晶体,所以熔点:CO2_______ SiO2(填“<”“=”或“>”)。
(4)金刚石、晶体硅、二氧化硅、CO2 4种晶体的构成微粒种类分别是_______ ,熔化时克服的微粒间的作用力分别是_______ 。
(1)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为
(2)氧化物MO的电子总数与SiC的相等,则M为
(3)C、Si为同一主族的元素,CO2和SiO2的化学式相似,但结构和性质有很大的不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成π键。从原子半径大小的角度分析,C、O原子间能形成π键,而Si、O原子间不能形成π键的原因是
(4)金刚石、晶体硅、二氧化硅、CO2 4种晶体的构成微粒种类分别是
您最近一年使用:0次
4 . 下列为几种晶体或晶胞的示意图:


请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成晶体的是_______ 。
(2)冰、金刚石、干冰3种晶体的熔点由高到低的顺序为_______ 。晶体硅的结构与金刚石非常相似。金刚石、晶体硅和金刚砂(碳化硅)的熔点由高到低的顺序为_______ (填化学式)。
(3)每个Cu晶胞中实际占有_______ 个 Cu原子,1 mol金刚石中含有C-C单键的数目约是_______ NA。
(4)观察干冰晶胞结构,每个CO2分子周围有_______ 个与之紧邻且等距的CO2分子;金刚石晶体中,碳原子的杂化类型为_______ 。
(5)若干冰分子的摩尔质量为M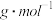 ,晶体的密度为
,晶体的密度为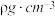 ,阿伏加德罗常数为
,阿伏加德罗常数为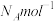 ,则该晶体晶胞的边长为
,则该晶体晶胞的边长为_______ cm。


请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成晶体的是
(2)冰、金刚石、干冰3种晶体的熔点由高到低的顺序为
(3)每个Cu晶胞中实际占有
(4)观察干冰晶胞结构,每个CO2分子周围有
(5)若干冰分子的摩尔质量为M
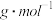 ,晶体的密度为
,晶体的密度为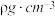 ,阿伏加德罗常数为
,阿伏加德罗常数为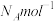 ,则该晶体晶胞的边长为
,则该晶体晶胞的边长为
您最近一年使用:0次
5 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
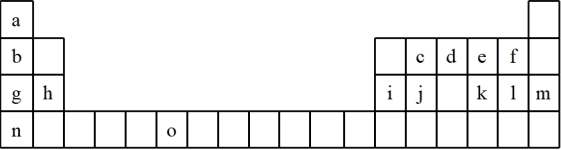
(1)请写出元素“o”的基态原子的价电子排布式_______ 。
(2)k在空气中燃烧产物的分子构型为_______ ,中心原子的杂化形式为_______ ,该分子是_______ (填“极性”或“非极性”)分子。
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是(写化学式)_______ ,试从结构角度加以解释_______ 。
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①晶胞中i原子的配位数为_______ 。
②该晶体的密度为_______ g/cm3。

(1)请写出元素“o”的基态原子的价电子排布式
(2)k在空气中燃烧产物的分子构型为
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是(写化学式)
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①晶胞中i原子的配位数为
②该晶体的密度为
您最近一年使用:0次
解题方法
6 . N、P、As及其化合物在工农业生产中用途非常广泛。回答下列问题:
(1)写出基态N原子的核外电子排布式___________ , 与N同周期的主族元素中,第一电离能比N大的元素是___________ (填元素符号) 。
(2)NH3是制造HNO3、化肥、炸药的重要原料,还可用于制冷。NH3的立体构型为___________ , 在工业合成NH3 (N2 + 3H2 2NH3)的反应所涉及的3种物质中,沸点从高到低的顺序为
2NH3)的反应所涉及的3种物质中,沸点从高到低的顺序为___________ , 原因是___________ 。
(3)H3PO2是一种重要的化工原料。已知:无机含氧酸分子中非羟基氧越多,酸性越强。1个非羟基氧是中强酸,2个非羟基氧是强酸。如H3PO4为中强酸,其结构简式为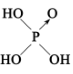 ;H3PO2也是一种中强酸,则H3PO2的结构简式为
;H3PO2也是一种中强酸,则H3PO2的结构简式为___________ ,写出H3PO2与足量NaOH溶液反应的化学方程式____________ 。
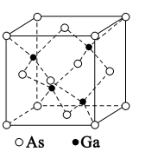
(4)GaAs 的熔点为1 238 °C,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为___________ 。已知:阿伏加德罗常数的值为NA,GaAs的摩尔质量为145g·mol-1,则GaAs的晶胞边长为___________ pm。
(1)写出基态N原子的核外电子排布式
(2)NH3是制造HNO3、化肥、炸药的重要原料,还可用于制冷。NH3的立体构型为
 2NH3)的反应所涉及的3种物质中,沸点从高到低的顺序为
2NH3)的反应所涉及的3种物质中,沸点从高到低的顺序为(3)H3PO2是一种重要的化工原料。已知:无机含氧酸分子中非羟基氧越多,酸性越强。1个非羟基氧是中强酸,2个非羟基氧是强酸。如H3PO4为中强酸,其结构简式为
 ;H3PO2也是一种中强酸,则H3PO2的结构简式为
;H3PO2也是一种中强酸,则H3PO2的结构简式为(4)GaAs 的熔点为1 238 °C,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为

您最近一年使用:0次
名校
7 . 回答下列问题:
(1)SiC晶体结构同金刚石相似,SiC晶体熔点_______ (填“高于”或“低于”)金刚石熔点,SiC晶体中最小环上有_______ 个C原子。
(2)PCl3分子的空间构型为_______ ,其中心原子的杂化方式为_______ 。
(3)用一种试剂鉴别苯酚溶液、乙醛溶液、己烷、己烯四种无色液体,该试剂为_______ (填名称)。
(4)短周期元素X、Y、Z原子序数依次增大。X是周期表中原子半径最小的元素。Y原子核外电子有六种不同的运动状态。Z基态原子核外L层有2个未成对的电子,则由X、Y、Z能组成的化合物可能为_______。
(5) 的结构如图:
的结构如图:

① 中S—O—O
中S—O—O_______ (填“是”或“不是”)在一条直线上。
② 中的O—O比H2O2中的更
中的O—O比H2O2中的更_______ (填“难”或“易”)断裂。
(1)SiC晶体结构同金刚石相似,SiC晶体熔点
(2)PCl3分子的空间构型为
(3)用一种试剂鉴别苯酚溶液、乙醛溶液、己烷、己烯四种无色液体,该试剂为
(4)短周期元素X、Y、Z原子序数依次增大。X是周期表中原子半径最小的元素。Y原子核外电子有六种不同的运动状态。Z基态原子核外L层有2个未成对的电子,则由X、Y、Z能组成的化合物可能为_______。
| A.X2YZ | B.X2YZ4 | C.X2Y2Z4 | D.XYZ3 |
 的结构如图:
的结构如图:
①
 中S—O—O
中S—O—O②
 中的O—O比H2O2中的更
中的O—O比H2O2中的更
您最近一年使用:0次
解题方法
8 . 碳族元素中的碳、硅、锗及其化合物在诸多领域有重要用途。
(1)碳族元素位于周期表_______ 区,基态锗原子外围电子的轨道表示式为_______ ,基态锗原子核外有_______ 种空间运动状态不同的电子。
(2)科学家以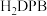 、
、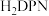 等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。
等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。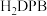 和
和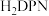 结构中含氮碳环均为平面结构,则N的杂化方式是
结构中含氮碳环均为平面结构,则N的杂化方式是_______ 。
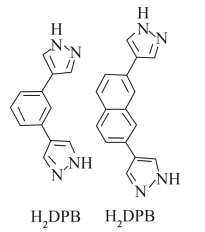
(3)金刚石(甲)、石墨(乙)、C60(丙)的结构如下图所示:
①12g金刚石和石墨中含有的σ键数目之比为_______ 。
②金刚石的熔点高于C60,但低于石墨,原因是_______ 。
③C60的晶胞呈分子密堆积,下列晶体中,与C60具有相同晶体结构的是_______ 。
A.CO2 B.冰 C.Zn D.Ag E.NaCl
(4)一种低温超导体立方晶胞结构如下图所示:
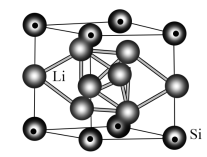
①该晶体的化学式为_______ 。
②若晶胞参数为apm,该晶体的密度ρ=_______  。(列出计算式即可,设NA表示阿伏加德罗常数的值)
。(列出计算式即可,设NA表示阿伏加德罗常数的值)
(1)碳族元素位于周期表
(2)科学家以
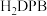 、
、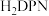 等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。
等双吡唑有机物为原料,制备了可去除痕量苯的吸附剂。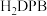 和
和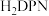 结构中含氮碳环均为平面结构,则N的杂化方式是
结构中含氮碳环均为平面结构,则N的杂化方式是
(3)金刚石(甲)、石墨(乙)、C60(丙)的结构如下图所示:

①12g金刚石和石墨中含有的σ键数目之比为
②金刚石的熔点高于C60,但低于石墨,原因是
③C60的晶胞呈分子密堆积,下列晶体中,与C60具有相同晶体结构的是
A.CO2 B.冰 C.Zn D.Ag E.NaCl
(4)一种低温超导体立方晶胞结构如下图所示:

①该晶体的化学式为
②若晶胞参数为apm,该晶体的密度ρ=
 。(列出计算式即可,设NA表示阿伏加德罗常数的值)
。(列出计算式即可,设NA表示阿伏加德罗常数的值)
您最近一年使用:0次
解题方法
9 . 单质硼的硬度近似于金刚石,有很高的电阻。但它的导电率随温度的升高而增大,高温时为良导体。硼在自然界中主要以硼酸和硼酸盐的形式存在。
(1)基态硼原子的价电子排布式为_______ ,晶体硼的熔沸点_______ (填“高于”或“低于”)金刚石,原因是_______ 。
(2)硼酸与氢氧化钠在一定条件下可以生成四硼酸钠,结构如图所示,四硼酸钠中含有的化学键类型为_______ ,O原子的杂化类型为_______ ,B原子与相连的3个O原子围成的图形为_______ ,第一电离能介于硼元素和氧元素之间的第二周期元素有_______ 种。

(3)硼和氮可以构成多种类型的晶体,其中一种晶体的晶胞如图所示,晶胞上下底面均为菱形,晶胞参数如图所示,该晶体的化学式为_______ ,晶胞密度为_______ (写出表达式即可)。

(1)基态硼原子的价电子排布式为
(2)硼酸与氢氧化钠在一定条件下可以生成四硼酸钠,结构如图所示,四硼酸钠中含有的化学键类型为

(3)硼和氮可以构成多种类型的晶体,其中一种晶体的晶胞如图所示,晶胞上下底面均为菱形,晶胞参数如图所示,该晶体的化学式为

您最近一年使用:0次
解题方法
10 . 过渡金属在生产、生活、科技等方面有着广泛的应用。例如仿生簇化合物Mn4XO4(X=Ca2+/Y3+/Gd3+)有望为实现利用太阳能和水获取清洁能源(氢能)开辟新途径,MnOx·Na2WO4·SiO2、钴(Co)的合金及其化合物材料等广泛应用于化工催化剂等领域。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为_______ 。
(2)基态Co原子核外有_______ 种运动状态不同的电子,其3d能级上有_______ 对成对电子。
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。已知:[Co(CN)6]4-是强还原剂,与水反应能生成[Co(CN)6]3-。[Co(CN)6]4-中含有σ键与π键的数目之比为_______ ,[Co(CN)6]3-中C的杂化方式为_______ 。
(4)[Mn(NH3)2]2+中配体分子的立体构型是_______ 。[Mn(NH3)2]2+中键角∠HNH_______ (填“大于” 、“小于”或“等于”)NH3中键角∠HNH。
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是_______ 。
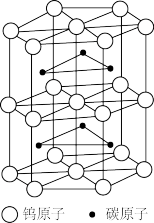
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是_______ ;已知:碳化钨晶体的密度为ρg·cm-3,NA为阿伏加德罗常数的值,六棱柱高为a cm,则底边长为_______ (用含ρ、a、N的表达式表示)nm。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为
(2)基态Co原子核外有
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是
(4)[Mn(NH3)2]2+中配体分子的立体构型是
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是

您最近一年使用:0次
2022-05-27更新
|
409次组卷
|
5卷引用:河北省秦皇岛市2022届高三三模化学试题
河北省秦皇岛市2022届高三三模化学试题(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编河南省2022届高三下学期仿真模拟大联考理科综合化学试题(已下线)新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷广东省部分学校2022届高三下学期高考冲刺化学试题



