名校
解题方法
1 . 通过下列实验以印刷线路板碱性蚀刻废液(主要成分为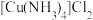 )为原料制备CuCl。下列说法正确的是
)为原料制备CuCl。下列说法正确的是
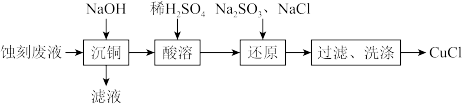
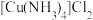 )为原料制备CuCl。下列说法正确的是
)为原料制备CuCl。下列说法正确的是

| A.铜元素位于周期表中d区 |
B. 中配位原子是N 中配位原子是N |
C.“还原”时离子方程式为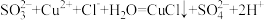 |
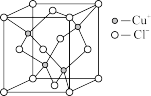
D.CuCl晶胞如图所示,与 等距离且最近的 等距离且最近的 有2个 有2个 |
您最近一年使用:0次
解题方法
2 . NiO晶体与NaCl具有相同晶胞结构。在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如图所示),可以认为 作密置单层排列,
作密置单层排列, 填充其中。设
填充其中。设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 半径为r pm。下列说法错误的是
半径为r pm。下列说法错误的是
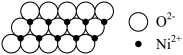
 作密置单层排列,
作密置单层排列, 填充其中。设
填充其中。设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 半径为r pm。下列说法错误的是
半径为r pm。下列说法错误的是
| A.Ni位于元素周期表第4周期第Ⅷ族 |
B.NiO晶体中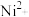 、 、 的配位数均为6 的配位数均为6 |
| C.NiO晶胞中八面体空隙与四面体空隙比为1:2 |
D.该“单分子层”面积密度为 |
您最近一年使用:0次
2022-07-25更新
|
984次组卷
|
3卷引用:山东省青岛市黄岛区2021-2022学年高二下学期期末考试化学试题
解题方法
3 . 硒( )在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。
)在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。
(1)单质硒的熔点为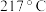 ,它属于
,它属于___________ 晶体。
(2)基态硒原子中,核外电子占据的最高能级的符号是___________ 。
(3)与硒元素相邻的同周期元素有砷和溴,这三种元素的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(4) 的立体构型是
的立体构型是___________ ;与 互为等电子体的分子有
互为等电子体的分子有___________ (写一种物质的化学式即可)。
(5) 水溶液比
水溶液比 水溶液的酸性强,原因是
水溶液的酸性强,原因是___________ 。
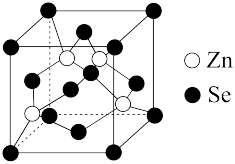
(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ 。
 )在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。
)在电子工业中可用于光电管、太阳能电池,硒元素可形成多种化合物。(1)单质硒的熔点为
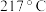 ,它属于
,它属于(2)基态硒原子中,核外电子占据的最高能级的符号是
(3)与硒元素相邻的同周期元素有砷和溴,这三种元素的第一电离能由小到大的顺序为
(4)
 的立体构型是
的立体构型是 互为等电子体的分子有
互为等电子体的分子有(5)
 水溶液比
水溶液比 水溶液的酸性强,原因是
水溶液的酸性强,原因是(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

您最近一年使用:0次
解题方法
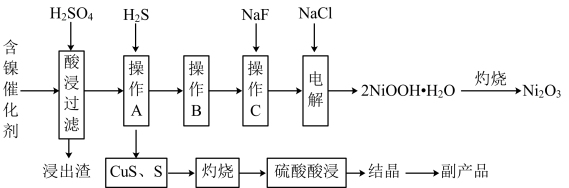
4 . 为回收利用废镍催化剂(主要成分为NiO,另含 、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
请回答下列问题:
(1)加快酸浸速率的常用措施有_______ (任写一条即可)。
(2)“浸出渣”主要成分为 和
和_______ 两种物质。
(3)“操作B”的过程是,先在40~50℃温度下加入 ,其作用是
,其作用是_______ (用离子方程式表示);再调pH至3.7~7.7,操作B可除去溶液中的_______ 元素(填元素名称)。
(4)在碱性条件下,电解产生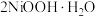 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生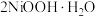 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到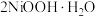 沉淀的离子方程式
沉淀的离子方程式_______ 。
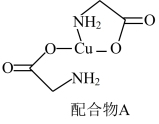
(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(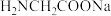 )即可得到它。N、O、S三种元素的第一电离能从大到小的顺序为
)即可得到它。N、O、S三种元素的第一电离能从大到小的顺序为_______ (填元素符号),配合物A中的配位原子是_______ 。
 、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
请回答下列问题:
(1)加快酸浸速率的常用措施有
(2)“浸出渣”主要成分为
 和
和(3)“操作B”的过程是,先在40~50℃温度下加入
 ,其作用是
,其作用是(4)在碱性条件下,电解产生
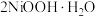 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生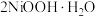 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到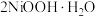 沉淀的离子方程式
沉淀的离子方程式(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(
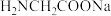 )即可得到它。N、O、S三种元素的第一电离能从大到小的顺序为
)即可得到它。N、O、S三种元素的第一电离能从大到小的顺序为
您最近一年使用:0次
解题方法
5 . 我国科学家在相当于110万大气压下合成了一种稳定的氦钠化合物,结构如图所示:小球代表Na,正方体代表He,小正方体代表共用电子,共用电子被迫集中在晶体结构的立方空间内。下列说法错误的是


| A.该物质的化学式为Na2He | B.极高的压力,可以影响He的化学性质 |
| C.该物质固态时能够导电 | D.Na的配位数为4 |
您最近一年使用:0次
名校
6 . 某镁铝尖晶石的晶胞由立方体M区和N区组成,结构如图。
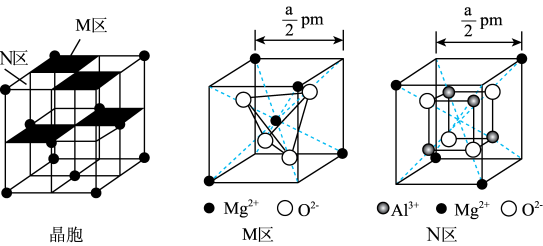
下列说法正确的是

下列说法正确的是
A.该晶胞的体积为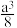 ×10-30cm3 ×10-30cm3 |
| B.与O2-最邻近的Al3+离子数为4 |
C.Mg2+和Mg2+之间的最短距离为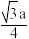 pm pm |
| D.该物质的化学式为MgAl2O4 |
您最近一年使用:0次
2022-07-11更新
|
229次组卷
|
3卷引用:山东省日照市2021-2022学年高二下学期期末考试化学试题
解题方法
7 . 第VIII族元素(Fe、Co、Ni等)在生产、生活中用途广泛。回答下列问题:
(1)第四周期基态原子与基态Ni3+未成对电子数相同的元素有_______ 种。
(2)邻二氮菲(phen,结构如图)能通过N原子与Fe2+形成稳定的配合物[Fe(phen)3]2+,该配合物的特征颜色可用于测定Fe2+的浓度。[Fe(phen)3]2+中Fe2+的配位数为_______ ;实验表明,邻二氮菲检验Fe2+的适宜pH范围是2~9,其原因是_______ 。

(3)草酸亚铁是生产磷酸铁锂动力电池的原料,可由草酸与硫酸亚铁铵反应制得。草酸与甲酸酸性相对强弱:草酸_______ 甲酸(填“>”“<”或“=”),其原因是_______ 。
(4)Fe3O4晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以看作是由4个A型和4个B型小单元交替并置而成。

①Fe3+填充在O2-围成的_______ 空隙处(填“正四面体”或“正八面体”)。
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比例是重要的影响因素。假设某Fe3O4纳米颗粒恰好是一个Fe3O4晶胞,该颗粒表面离子与总离子数的最简整数比为_______ 。
(1)第四周期基态原子与基态Ni3+未成对电子数相同的元素有
(2)邻二氮菲(phen,结构如图)能通过N原子与Fe2+形成稳定的配合物[Fe(phen)3]2+,该配合物的特征颜色可用于测定Fe2+的浓度。[Fe(phen)3]2+中Fe2+的配位数为

(3)草酸亚铁是生产磷酸铁锂动力电池的原料,可由草酸与硫酸亚铁铵反应制得。草酸与甲酸酸性相对强弱:草酸
(4)Fe3O4晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以看作是由4个A型和4个B型小单元交替并置而成。

①Fe3+填充在O2-围成的
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比例是重要的影响因素。假设某Fe3O4纳米颗粒恰好是一个Fe3O4晶胞,该颗粒表面离子与总离子数的最简整数比为
您最近一年使用:0次
8 . 氧化锌晶体常用于液晶显示器中,该晶体可用醋酸锌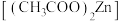 为原料在高温下分解制得。下列说法正确的是
为原料在高温下分解制得。下列说法正确的是
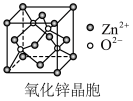
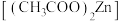 为原料在高温下分解制得。下列说法正确的是
为原料在高温下分解制得。下列说法正确的是
A.ZnO中 的配位数为6 的配位数为6 |
| B.ZnO、ZnS均为离子晶体,ZnO的熔点低于ZnS |
C.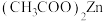 中非金属元素电负性:O>C>H 中非金属元素电负性:O>C>H |
D.若氧化锌晶胞参数为a,则两个 的最近距离为 的最近距离为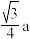 |
您最近一年使用:0次
9 . 下面有关晶体的叙述中,不正确的是
| A.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
| B.氯化铯晶体中,每个Cs+周围紧邻8个C1- |
| C.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 |
| D.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
您最近一年使用:0次
2022-06-02更新
|
150次组卷
|
3卷引用:新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题
名校
10 . 已知某离子晶体的晶胞示意图如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,晶体的密度为dg/cm3,下列说法中正确的是
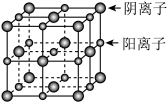

| A.晶体晶胞中阴、阳离子的个数都为1 |
| B.晶体中阴、阳离子的配位数都是4 |
| C.该晶胞可能是CsCl的晶胞 |
D.该晶体中两个距离最近的阳离子的核间距为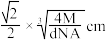 |
您最近一年使用:0次



