1 . 某些晶体或晶胞结构示意图如下。下列说法正确的是


| A.图 1 所示金刚石晶体中,碳原子与碳碳键个数比为 1:4 |
| B.图 2 所示 CsCl 晶胞中,Cs+的配位数为 6 |
| C.图 3 所示 CaF2晶胞中,含有 4 个 Ca2+ |
| D.图 4 所示干冰晶体中1个 CO2分子周围紧邻 8 个 CO2分子 |
您最近一年使用:0次
2021-01-28更新
|
101次组卷
|
2卷引用:湖北省十堰市2020-2021学年高二上学期期末考试化学试题
2 . 模型在科学认识中具有描述、解释和预测等功能。下列有关化学模型的说法错误的是
| A.金属晶体的简单立方堆积是密置层得到的一种堆积方式 |
| B.氯化钠和氯化铯晶体中氯离子的配位数不同可用阳离子与阴离子的半径比不同解释 |
| C.由NH3和BF3易化合生成H3NBF3可预测H3NBF3中含有配位键 |
D.根据VSEPR理论可推测BF3的键角大于BF |
您最近一年使用:0次
解题方法
3 . 下列关于Na、Cs的化合物结构与性质的说法错误的是
| A.NaCl为离子化合物,可推知CsCl也为离子化合物 |
| B.NaCl与CsCl相比,熔点更高 |
| C.NaCl与CsCl晶胞中Cl-的配位数均为8 |
| D.Cs+容易形成配合物而Na+一般不会形成配合物的原因与微粒半径有关 |
您最近一年使用:0次
4 . 钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞的结构如图所示,下列有关说法中正确的是


| A.该晶体属于离子晶体 |
| B.晶体的化学式为Ba2O2 |
| C.该晶体的晶胞结构与CsCl相似 |
| D.与每个Ba2+距离相等且最近的Ba2+共有8个 |
您最近一年使用:0次
2021-01-26更新
|
296次组卷
|
4卷引用:新疆乌鲁木齐高级中学2021-2022学年高二上学期期末考试化学试题
解题方法
5 . 铁的硫化物被认为是有前景的锂电池材料,但导电性较差,放电时易膨胀。
(1)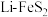 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。
①水热法合成 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为___________ 。
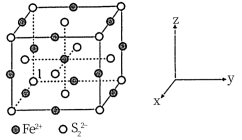
② 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为___________ (任写一个),每个 周围距离最近且相等的
周围距离最近且相等的 有
有___________ 个。
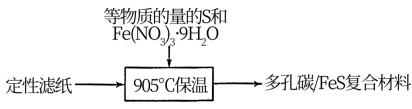
(2)①将 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且___________ 。多孔碳/ 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和___________ 。
②分别取多孔碳、多孔碳/ 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。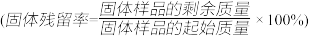
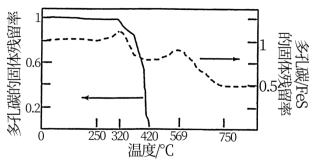
420℃~569℃时,多孔碳/ 固体残留率增大的原因是
固体残留率增大的原因是___________ 。
③ 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: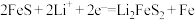
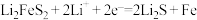
该多孔碳/ 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子___________  。(写出计算过程)
。(写出计算过程)
(1)
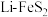 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。①水热法合成
 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为②
 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为 周围距离最近且相等的
周围距离最近且相等的 有
有
(2)①将
 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和
②分别取多孔碳、多孔碳/
 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。

420℃~569℃时,多孔碳/
 固体残留率增大的原因是
固体残留率增大的原因是③
 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: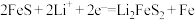
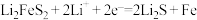
该多孔碳/
 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子 。(写出计算过程)
。(写出计算过程)
您最近一年使用:0次
6 . 下列不属于影响离子晶体结构的因素的是
| A.晶体中阴、阳离子的半径比 |
| B.离子晶体的晶格能 |
| C.晶体中阴、阳离子的电荷比 |
| D.离子键的纯粹程度 |
您最近一年使用:0次
2020-12-22更新
|
135次组卷
|
2卷引用:宁夏海原第一中学2020-2021学年高二下学期期末考试化学试题
7 . 下列对结构与性质的大小排序不正确的是
| A.键角:NH3>H2O>P4 | B.阴离子配位数:CsCl>NaCl>CaF2 |
| C.第一电离能:Se>As>Ge | D.酸性:H2SO4>H2SO3>HClO |
您最近一年使用:0次
2020-12-02更新
|
325次组卷
|
4卷引用:四川省乐山市2020-2021学年高二上学期期末考试化学试题
8 . 第四周期过渡元素Mn,Fe,Ti可与C,H,O形成多种化合物.
(1)H,C,O,N四种元素的电负性由小到大的顺序为___ 。
(2)Mn基态原子的电子排布式可表示为___ ,CO 的空间构型
的空间构型___ (用文字表述)。
(3)下列叙述正确的是___ (填字母)。
A.CH2O与水分子间能形成氢键
B.CH3COOH和苯分子中的碳原子均采用sp2杂化
C.CH2=CH-CHO分子中含有7个σ键和2个π键
D.CO的结构式可表示为:C=O
E.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(4)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为___ 。

(1)H,C,O,N四种元素的电负性由小到大的顺序为
(2)Mn基态原子的电子排布式可表示为
 的空间构型
的空间构型(3)下列叙述正确的是
A.CH2O与水分子间能形成氢键
B.CH3COOH和苯分子中的碳原子均采用sp2杂化
C.CH2=CH-CHO分子中含有7个σ键和2个π键
D.CO的结构式可表示为:C=O
E.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(4)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为

您最近一年使用:0次
名校
解题方法
9 .  的晶体结构与
的晶体结构与 相似,
相似, 可以看作是
可以看作是 的位置用
的位置用 代替,
代替, 的位置用
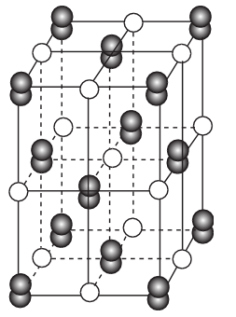
的位置用 代替(如图),晶体中含有的哑铃形
代替(如图),晶体中含有的哑铃形 使晶胞沿一个方向拉长。下列对于
使晶胞沿一个方向拉长。下列对于 晶体结构的描述正确的是
晶体结构的描述正确的是
 的晶体结构与
的晶体结构与 相似,
相似, 可以看作是
可以看作是 的位置用
的位置用 代替,
代替, 的位置用
的位置用 代替(如图),晶体中含有的哑铃形
代替(如图),晶体中含有的哑铃形 使晶胞沿一个方向拉长。下列对于
使晶胞沿一个方向拉长。下列对于 晶体结构的描述正确的是
晶体结构的描述正确的是
A.一个 晶胞的质量为 晶胞的质量为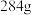 | B. 的熔点比 的熔点比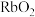 的熔点低 的熔点低 |
C.与 距离最近且相等的 距离最近且相等的 有12个 有12个 | D.与 距离最近且相等的 距离最近且相等的 共有4个 共有4个 |
您最近一年使用:0次
2020-09-29更新
|
332次组卷
|
5卷引用:辽宁省部分中学2021-2022学年高二下学期期末检测化学试题
名校
解题方法
10 . 下列有关晶体的叙述中,不正确的是( )
| A.氯化钠和氯化铯晶体中,阳离子的配位数均为6 |
| B.金刚石为三维网状结构,由碳原子以sp3杂化轨道形成共价键 |
| C.金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8 |
| D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
您最近一年使用:0次
2020-09-29更新
|
177次组卷
|
7卷引用:2016-2017学年四川省资阳市高二上学期期末化学试卷
2016-2017学年四川省资阳市高二上学期期末化学试卷2016-2017学年四川省雅安中学高二下学期开学考试化学试卷河北省保定市保定三中2016-2017学年度第二学期3月月考高二化学试题第3章 物质的聚集状态与物质性质——B拓展区综合拓展(鲁科版选修3)内蒙古开鲁县第一中学2019-2020学年高二下学期期中考试化学试题辽宁省大连市普兰店市第三十八中学2021届高三第一学期开学考试化学试题(已下线)第三单元 物质的聚集状态性质与物质性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)



