1 . 下列有关实验的叙述,正确的是___ (填序号)。
A.用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B.分馏石油时,温度计的末端必须插入液面下
C.用分液漏斗分离环己烷和水的混合液体
D.用氨水洗涤做过银镜反应的试管
E.配制银氨溶液时,将稀氨水逐滴加到稀硝酸银溶液中,至产生的沉淀刚好溶解
F.蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖
G.配制混酸,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
H.不慎将苯酚溶液沾到皮肤上,立即用氢氧化钠溶液清洗
A.用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B.分馏石油时,温度计的末端必须插入液面下
C.用分液漏斗分离环己烷和水的混合液体
D.用氨水洗涤做过银镜反应的试管
E.配制银氨溶液时,将稀氨水逐滴加到稀硝酸银溶液中,至产生的沉淀刚好溶解
F.蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖
G.配制混酸,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
H.不慎将苯酚溶液沾到皮肤上,立即用氢氧化钠溶液清洗
您最近一年使用:0次
名校
2 . 现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

已知反应I为:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl
(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中___________ ,过滤;
c.向滤液中___________ ,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(2)反应II的化学方程式是___________ 。
(3)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2.则样品中纯碱的质量分数是___________ %(保留1位小数)。

已知反应I为:NaCl+CO2+NH3+H2O
 NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO
 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中
c.向滤液中
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(2)反应II的化学方程式是
(3)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2.则样品中纯碱的质量分数是
您最近一年使用:0次
解题方法
3 . 按要求填空
(1)向CuCl2溶液中滴加NaOH溶液,现象:_________ ,离子方程式:_____ ,
(2)向NaHCO3溶液中滴加稀硫酸,现象:_____ ,离子方程式:_______ ;
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂_____ ,离子方程式;_____ 。
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂________ ,离子方程式__________ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀硫酸,现象:
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂
您最近一年使用:0次
2021-01-09更新
|
1981次组卷
|
5卷引用:贵州省安顺市大洋实验学校2020-2021学年高一上学期期中考试化学试题
名校
解题方法
4 . 铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
请回答下列问题:
(1)加入氧化剂的目的是______ 。
(2)最适合作氧化剂X的是___ 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是_____ 。
(4)若不用物质Y而是直接用碱则不能达到目的,试解释原因____ 。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? 该如何操作?_____ 。

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
(1)加入氧化剂的目的是
(2)最适合作氧化剂X的是
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是
(4)若不用物质Y而是直接用碱则不能达到目的,试解释原因
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? 该如何操作?
您最近一年使用:0次
名校
5 . (1)除去 Na2CO3 溶液中混有的 NaHCO3 应加入_____ (填化学式)溶液。
(2)中国的瓷器驰名世界,制备陶瓷是以黏土[主要成分 Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为:____ 。
(3)______ 是制造光导纤维重要原料。
(4)漂白粉或漂粉精的有效成分是_____ (填化学式)。
(5)NO2 是___ 色有毒气体,NO2 与水反应的方程式为___ ,标准状况下 67.2LNO2 与水反应转移电子为__ mol。
(6)蔗糖与浓硫酸发生反应,形成“黑面包”,体现了浓硫酸的_______ 性。
(2)中国的瓷器驰名世界,制备陶瓷是以黏土[主要成分 Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为:
(3)
(4)漂白粉或漂粉精的有效成分是
(5)NO2 是
(6)蔗糖与浓硫酸发生反应,形成“黑面包”,体现了浓硫酸的
您最近一年使用:0次
6 . CuO是某种无机胶黏剂的组分之一,制备的部分流程如图。
已知:CuO难溶于水。
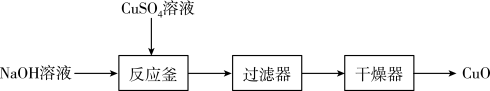
(1)反应釜中发生的化学方程式:_________________ ,基本反应类型分别是_________________________
(2)过滤器分离出的滤液中一定含有的溶质是___________________ 。
(3)Na2SO4中硫、氧元素的质量比为______________________
已知:CuO难溶于水。

(1)反应釜中发生的化学方程式:
(2)过滤器分离出的滤液中一定含有的溶质是
(3)Na2SO4中硫、氧元素的质量比为
您最近一年使用:0次
解题方法
7 . I.除去括号中的杂质(填试剂)
(1)CuCl2溶液(FeCl3)_________________________ ;
(2)Fe2(SO4) 3溶液( FeSO4)_______________________ ;
(3)NaHCO3溶液(Na2CO3)___________________ ;
(4)CO2(HCl)_________________________ ;
Ⅱ写出下列反应的离子方程式
(5)二氧化硫使溴水褪色的原理_________________________________ ;
(6)将NaHCO3溶液与澄清石灰水等物质的量混合_________________________________ ;
(7)向NaAlO2溶液中通入过量CO2气体__________________________________________ ;
(8)FeBr2溶液和等物质的量的Cl2反应_________________________________________ 。
(1)CuCl2溶液(FeCl3)
(2)Fe2(SO4) 3溶液( FeSO4)
(3)NaHCO3溶液(Na2CO3)
(4)CO2(HCl)
Ⅱ写出下列反应的离子方程式
(5)二氧化硫使溴水褪色的原理
(6)将NaHCO3溶液与澄清石灰水等物质的量混合
(7)向NaAlO2溶液中通入过量CO2气体
(8)FeBr2溶液和等物质的量的Cl2反应
您最近一年使用:0次
名校
解题方法
8 . 如图是某小组设计的用粗盐(杂质为泥沙、硫酸镁、硫酸钙)制备氯化钠晶体的流程,请完成下面小题。

1. 完成“步骤I”不需要的行为或操作是( )
A. 称量粗盐的质量
B. 量取一定量的水
C. 查阅氯化钠的溶解度
D. 充分溶解后,过滤
2. 对于“步骤II”的分析错误的是( )
A. 加入的试剂应足量或过量
B. 可依次加入氢氧化钡、碳酸钠
C. 得到的溶液中含有四种溶质
D. 发生若干个复分解反应
3. 对于“步骤III”和“步骤IV”的分析正确的是( )
A. 加入的盐酸一定不能过量
B. III中只发生中和反应
C. 操作IV是蒸发结晶
D. 若不考虑损失,理论上最终得到的氯化钠的质量等于粗盐中氯化钠的质量

1. 完成“步骤I”不需要的行为或操作是
A. 称量粗盐的质量
B. 量取一定量的水
C. 查阅氯化钠的溶解度
D. 充分溶解后,过滤
2. 对于“步骤II”的分析错误的是
A. 加入的试剂应足量或过量
B. 可依次加入氢氧化钡、碳酸钠
C. 得到的溶液中含有四种溶质
D. 发生若干个复分解反应
3. 对于“步骤III”和“步骤IV”的分析正确的是
A. 加入的盐酸一定不能过量
B. III中只发生中和反应
C. 操作IV是蒸发结晶
D. 若不考虑损失,理论上最终得到的氯化钠的质量等于粗盐中氯化钠的质量
您最近一年使用:0次
解题方法
9 . 溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_________________ 。
②A、B、C三种物质中,溶解度随温度升高而减小的是____ 。
③t2℃时,完全溶解agA物质最少需要水的质量是_____ g。
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、____ 和滤纸。
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是____ g.

(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是
②A、B、C三种物质中,溶解度随温度升高而减小的是
③t2℃时,完全溶解agA物质最少需要水的质量是
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是

您最近一年使用:0次
10 . 根据下图回答相关问题:
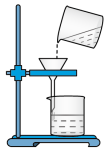
(1)该图所示进行的是过滤操作,图中还缺少的仪器是____ ,其作用是___ 。
(2)添加该仪器后,一名学生用此装置对浑浊的河水进行过滤,过滤两次后,发现滤液仍然浑浊,可能的原因是_______ (写出一点即可)。

(1)该图所示进行的是过滤操作,图中还缺少的仪器是
(2)添加该仪器后,一名学生用此装置对浑浊的河水进行过滤,过滤两次后,发现滤液仍然浑浊,可能的原因是
您最近一年使用:0次



