真题
解题方法
1 . (1)已知3种原子晶体的熔点数据如下表:
金刚石熔点比晶体硅熔点高的原因是_______ 。
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是_______ 。
| 金刚石 | 碳化硅 | 晶体硅 | |
| 熔点/℃ | >3550 | 2600 | 1415 |
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是
您最近一年使用:0次
2021-06-15更新
|
3660次组卷
|
9卷引用:解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)2021年6月新高考浙江化学高考真题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题08.微粒间相互作用力-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)2021年6月浙江高考化学试题变式题26-31(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
2 . 铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
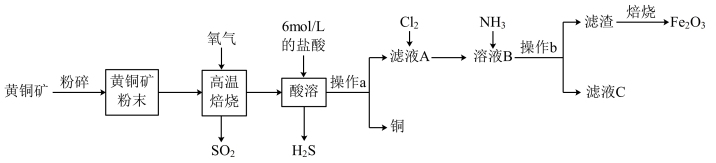
(1)将黄铜矿粉碎的目的是____ 。
(2)高温熔烧时发生的反应是CuFeS2+O2 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子____ mol。
(3)操作a为____ 。
(4)向滤液A中通入Cl2的目的是____ 。
(5)向溶液B中通入NH3后发生反应的离子方程式为____ 。
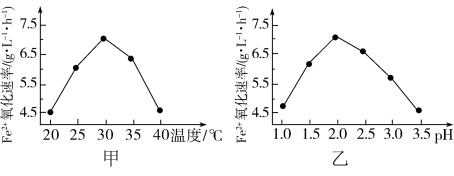
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
由图甲和图乙判断使用硫杆菌的最佳条件为___ ,若反应温度过高,反应速率下降,其原因是___ 。

(1)将黄铜矿粉碎的目的是
(2)高温熔烧时发生的反应是CuFeS2+O2
 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3后发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
2022-06-16更新
|
1326次组卷
|
5卷引用:北京市第一七一中学2021-2022学年高一下学期6月月考化学试题
北京市第一七一中学2021-2022学年高一下学期6月月考化学试题河南省项城市第三高级中学2021-2022学年高二下学期期末考试化学试题(已下线)模拟卷02-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)模拟卷06-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)模拟卷05-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
3 . 养殖业废水中含有一定量的氨氮(以 形式存在)污染物,通过沉淀法或折点氯化法处理后可使水中氨氮达到国家规定的排放标准。
形式存在)污染物,通过沉淀法或折点氯化法处理后可使水中氨氮达到国家规定的排放标准。
(1)沉淀法:向酸性废水中加入一定比例的 和
和 ,将氨氮转化为
,将氨氮转化为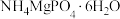 沉淀除去。
沉淀除去。
①该反应的离子方程式为___________ 。
②增大废水的 ,除生成
,除生成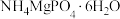 沉淀和
沉淀和 沉淀外,还可能生成另一沉淀的化学式为
沉淀外,还可能生成另一沉淀的化学式为___________ 。
(2)折点氯化法:向废水中加入 溶液,将氨氮最终转化为
溶液,将氨氮最终转化为 除去。
除去。 时,
时, 投加量
投加量 [即
[即 ]与水中余氯(即氧化性的氯,包括
]与水中余氯(即氧化性的氯,包括 、
、 、
、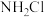 、
、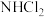 等)含量关系如图-1所示。
等)含量关系如图-1所示。

① 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
②废水的 对氨氮去除率的影响如图-2所示。氨氮去除率在
对氨氮去除率的影响如图-2所示。氨氮去除率在 后迅速下降、
后迅速下降、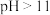 后下降变缓,其原因可能是
后下降变缓,其原因可能是___________ 。
(3)由于 不稳定,实验前需测定试剂
不稳定,实验前需测定试剂 溶液中有效氯含量(即单位体积溶液中含氯化合物作为消毒剂时,氧化能力相当的
溶液中有效氯含量(即单位体积溶液中含氯化合物作为消毒剂时,氧化能力相当的 的质量,单位
的质量,单位 )。取
)。取 市售待测
市售待测 溶液,加水稀释至
溶液,加水稀释至 ,用乙酸-乙酸钠溶液控制稀释液
,用乙酸-乙酸钠溶液控制稀释液 为3.5~4.2;加入过量
为3.5~4.2;加入过量 溶液充分反应后,滴加2~3滴淀粉溶液,用
溶液充分反应后,滴加2~3滴淀粉溶液,用 的标准
的标准 溶液滴定至终点,共消耗标准
溶液滴定至终点,共消耗标准 溶液
溶液 (已知:
(已知: )。计算该市售
)。计算该市售 溶液中有效氯含量
溶液中有效氯含量___________ (写出计算过程)。
 形式存在)污染物,通过沉淀法或折点氯化法处理后可使水中氨氮达到国家规定的排放标准。
形式存在)污染物,通过沉淀法或折点氯化法处理后可使水中氨氮达到国家规定的排放标准。(1)沉淀法:向酸性废水中加入一定比例的
 和
和 ,将氨氮转化为
,将氨氮转化为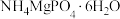 沉淀除去。
沉淀除去。①该反应的离子方程式为
②增大废水的
 ,除生成
,除生成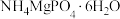 沉淀和
沉淀和 沉淀外,还可能生成另一沉淀的化学式为
沉淀外,还可能生成另一沉淀的化学式为(2)折点氯化法:向废水中加入
 溶液,将氨氮最终转化为
溶液,将氨氮最终转化为 除去。
除去。 时,
时, 投加量
投加量 [即
[即 ]与水中余氯(即氧化性的氯,包括
]与水中余氯(即氧化性的氯,包括 、
、 、
、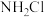 、
、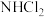 等)含量关系如图-1所示。
等)含量关系如图-1所示。
①
 时发生反应的离子方程式为
时发生反应的离子方程式为②废水的
 对氨氮去除率的影响如图-2所示。氨氮去除率在
对氨氮去除率的影响如图-2所示。氨氮去除率在 后迅速下降、
后迅速下降、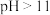 后下降变缓,其原因可能是
后下降变缓,其原因可能是(3)由于
 不稳定,实验前需测定试剂
不稳定,实验前需测定试剂 溶液中有效氯含量(即单位体积溶液中含氯化合物作为消毒剂时,氧化能力相当的
溶液中有效氯含量(即单位体积溶液中含氯化合物作为消毒剂时,氧化能力相当的 的质量,单位
的质量,单位 )。取
)。取 市售待测
市售待测 溶液,加水稀释至
溶液,加水稀释至 ,用乙酸-乙酸钠溶液控制稀释液
,用乙酸-乙酸钠溶液控制稀释液 为3.5~4.2;加入过量
为3.5~4.2;加入过量 溶液充分反应后,滴加2~3滴淀粉溶液,用
溶液充分反应后,滴加2~3滴淀粉溶液,用 的标准
的标准 溶液滴定至终点,共消耗标准
溶液滴定至终点,共消耗标准 溶液
溶液 (已知:
(已知: )。计算该市售
)。计算该市售 溶液中有效氯含量
溶液中有效氯含量
您最近一年使用:0次
2022高三·全国·专题练习
4 . 废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为CuIn0.5Ga0.5Se2。某探究小组回收处理流程如图:

回答下列问题:
(1)“酸浸氧化”发生的主要氧化还原反应的化学方程式为_______ 。
(2)“高温气相沉积”过程中发生的化学反应方程式为_______ 。

回答下列问题:
(1)“酸浸氧化”发生的主要氧化还原反应的化学方程式为
(2)“高温气相沉积”过程中发生的化学反应方程式为
您最近一年使用:0次
解题方法
5 . 按要求填空
(1)向CuCl2溶液中滴加NaOH溶液,现象:_________ ,离子方程式:_____ ,
(2)向NaHCO3溶液中滴加稀硫酸,现象:_____ ,离子方程式:_______ ;
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂_____ ,离子方程式;_____ 。
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂________ ,离子方程式__________ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀硫酸,现象:
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂
您最近一年使用:0次
2021-01-09更新
|
1981次组卷
|
5卷引用:河北省沧州市部分学校2021-2022学年高一下学期开年摸底考试联考化学试题
名校
6 . 选择下列实验方法分离、提纯物质,将分离、提纯方法的字母填在横线上。
A.萃取 B.重结晶 C.分液 D.蒸馏 E.过滤 F.洗气
(1)分离水和汽油的混合物:___________ 。
(2)分离四氯化碳 (沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物:___________ 。
(3)提取碘水中的碘:___________ 。
(4)除去混在乙烷中的乙烯:___________ 。
(5)从硝酸钾和氯化钠的混合溶液中获得硝酸钾:___________ 。
A.萃取 B.重结晶 C.分液 D.蒸馏 E.过滤 F.洗气
(1)分离水和汽油的混合物:
(2)分离四氯化碳 (沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物:
(3)提取碘水中的碘:
(4)除去混在乙烷中的乙烯:
(5)从硝酸钾和氯化钠的混合溶液中获得硝酸钾:
您最近一年使用:0次
2022-02-14更新
|
1690次组卷
|
5卷引用:课前-1.2.1 有机化合物的分离、提纯-人教2019选择性必修3
课前-1.2.1 有机化合物的分离、提纯-人教2019选择性必修3(已下线)第03讲 有机物的分离、提纯(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)安徽省安庆市第七中学2021-2022学年高二下学期3月阶段性考试化学试题2016-2017学年内蒙古集宁一中高二下月考二化学卷(已下线)【知识图鉴】单元讲练测选择性必修3第1单元01讲核心
名校
7 . 工业废水中的重金属离子会导致环境污染危害人体健康,可用多种方法去除。
I.臭氧法
络合态的金属离子难以直接去除。O3与水反应产生的·OH(羟基自由基)可以氧化分解金属配合物[mRa+ ·nX]中的有机配体,使金属离子游离到水中,反应原理为:
·OH+[mRa+·nX] →mRa++CO2+H2O (Ra+表示金属离子,X表示配体)
·OH同时也能与溶液中的 、
、 反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。
反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。
(1)基态Ni2+的核外电子排布式为_______ 。
(2)加入的Ca(OH)2的作用是_______ 。
Ⅱ.纳米零价铝法
纳米铝粉有很强的吸附性和还原性,水中溶解的氧在纳米铝粉表面产生·OH(羟基自由基),可将甘氨酸铬中的有机基团降解,释放出的铬(VI)被纳米铝粉去除。
(3)向AlCl3溶液中滴加碱性NaBH4溶液,溶液中BH (B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH)
(B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH) ,其离子方程式为
,其离子方程式为 _______ 。
(4)向含有甘氨酸铬的废水中加入纳米铝粉,研究溶液中总氮含量[ ]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是 _______ 。

Ⅲ.金属炭法
其他条件相同,分别取铝炭混合物和铁炭混合物,与含Zn2+的废水反应相同时间,Zn2+去除率与废水pH的关系如图所示。

(5)废水pH为3时,铝炭混合物对Zn2+去除率远大于铁炭混合物的主要原因是_______ 。
(6)废水pH大于6,随着pH增大,铝炭混合物对Zn2+去除率增大的原因是_______ 。
I.臭氧法
络合态的金属离子难以直接去除。O3与水反应产生的·OH(羟基自由基)可以氧化分解金属配合物[mRa+ ·nX]中的有机配体,使金属离子游离到水中,反应原理为:
·OH+[mRa+·nX] →mRa++CO2+H2O (Ra+表示金属离子,X表示配体)
·OH同时也能与溶液中的
 、
、 反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。
反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。(1)基态Ni2+的核外电子排布式为
(2)加入的Ca(OH)2的作用是
Ⅱ.纳米零价铝法
纳米铝粉有很强的吸附性和还原性,水中溶解的氧在纳米铝粉表面产生·OH(羟基自由基),可将甘氨酸铬中的有机基团降解,释放出的铬(VI)被纳米铝粉去除。
(3)向AlCl3溶液中滴加碱性NaBH4溶液,溶液中BH
 (B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH)
(B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH) ,其离子方程式为
,其离子方程式为 (4)向含有甘氨酸铬的废水中加入纳米铝粉,研究溶液中总氮含量[
 ]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是 
Ⅲ.金属炭法
其他条件相同,分别取铝炭混合物和铁炭混合物,与含Zn2+的废水反应相同时间,Zn2+去除率与废水pH的关系如图所示。

(5)废水pH为3时,铝炭混合物对Zn2+去除率远大于铁炭混合物的主要原因是
(6)废水pH大于6,随着pH增大,铝炭混合物对Zn2+去除率增大的原因是
您最近一年使用:0次
2022-05-07更新
|
916次组卷
|
3卷引用:江苏省苏锡常镇四市2022届高三下学期教学情况调研(二)化学试题
8 . 电镀废液中含有Cu2+、Mg2+、Ca2+、Ni2+和Fe3+,某专利申请用下列方法从该类废液中制备高纯度的铜粉。

已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
回答下列问题:
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥_______ (结果保留两位小数)。分离固液混合物时,需要用真空抽滤的方法提高过滤的速度和效果,其原因是_______ 。
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及其浓度相关,实验测得Cu2+与SO2反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
①由此可知,制备过程中进行电位检测时,要把溶液的氧化还原电位控制在_______ mV左右。
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是Cu2+直接被还原为Cu的原因是_______ 。反应生成Cu+的离子方程式是_______ 。
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有_______ 。为了使这些离子均除去,使水得到进一步的净化,应该在调节溶液pH使其他杂质离子沉淀后,再使Ca2+转化为_______ (填化学式)而除去。

已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
| Fe3+/Fe2+ | Cu2+/Cu+ | Cu2+/Cu |  /SO2 /SO2 | Fe2+/Fe | Ni2+/Ni | Mg2+/Mg | Ca2+/Ca |
| 0.77 | 0.52 | 0.34 | 0.17 | -0.44 | -0.23 | -2.38 | -2.76 |
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及其浓度相关,实验测得Cu2+与SO2反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
| 反应液的电位(mV) | 360 | 340 | 320 | 300 | 280 | 260 |
| 铜粉的回收率(%) | 86.5 | 90.2 | 95.6 | 97.2 | 97.3 | 97.4 |
| 产品的纯度(%) | 99.9 | 99.9 | 99.9 | 99.9 | 99.9 | 99.9 |
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是Cu2+直接被还原为Cu的原因是
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有
您最近一年使用:0次
9 . 从铜氨废液含[Cu(NH3)3·CO]+、[Cu(NH3)2]2+、[Cu(NH3)4]2+、NH3、CH3COO−、 等中回收铜的工艺流程如图:
等中回收铜的工艺流程如图:
(1)步骤(Ⅰ)中被氧化的元素是_____________ ,由步骤(Ⅱ)可确定NH3与H+的结合能力比与Cu2+的_____________ (填“强”或“弱”)。
(2)步骤(Ⅲ)“沉铜”时,发生的主要反应的离子方程式为_______________________ ,利用Na2S溶液而不选用NaOH溶液“沉铜”的优点是_______________________ 。
(3)步骤(Ⅳ)反应中,氧化剂与还原剂的物质的量之比为_____________ 。
(4)该流程中可以循环利用的物质是__________________________ (填化学式)。
(5)碱式氯化铜在400℃时能完全分解为CuO、H2O和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为__________________________ 。
 等中回收铜的工艺流程如图:
等中回收铜的工艺流程如图: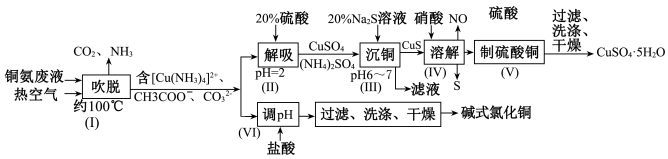
(1)步骤(Ⅰ)中被氧化的元素是
(2)步骤(Ⅲ)“沉铜”时,发生的主要反应的离子方程式为
(3)步骤(Ⅳ)反应中,氧化剂与还原剂的物质的量之比为
(4)该流程中可以循环利用的物质是
(5)碱式氯化铜在400℃时能完全分解为CuO、H2O和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为
您最近一年使用:0次
2021-01-06更新
|
1939次组卷
|
4卷引用:模拟卷01-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
(已下线)模拟卷01-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)山东省潍坊市临朐县实验中学2021届高三上学期12月阶段性学情检测化学试题(已下线)2021年高考全国甲卷化学试题变式题2024届广西桂林市高三下学期4月月考化学试卷
名校
解题方法
10 . 经检测,某化工厂排出的废水呈酸性,且其中含有大量  、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:
(1)下列离子中,能大量存在于该废水中的是_______ 填标号
填标号
(2)取 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、____  用离子符号表示
用离子符号表示 。
。
(3)某化学社团小组成员欲除去废水样品中的 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:

 试剂
试剂 为
为_______  写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、________ 。
 “分离操作”的名称是
“分离操作”的名称是______ ,需用到的玻璃仪器主要有______ 。
 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为______ 。
 、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:(1)下列离子中,能大量存在于该废水中的是_______
 填标号
填标号
A. | B. | C. | D. |
 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、 用离子符号表示
用离子符号表示 。
。(3)某化学社团小组成员欲除去废水样品中的
 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:
 试剂
试剂 为
为 写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、 “分离操作”的名称是
“分离操作”的名称是 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为
您最近一年使用:0次
2023-07-30更新
|
533次组卷
|
8卷引用:第一章 物质及其变化



