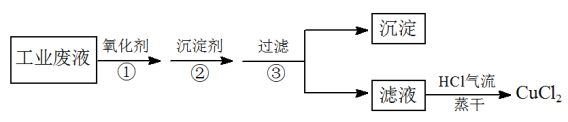
1 . 电子工业常用FeCl3溶液腐蚀印刷电路板上不需要的铜箔,最后得到含FeCl3、FeCl2杂质的CuCl2溶液。某化学兴趣小组设计下列方案,从该废液中 除去FeCl3、FeCl2杂质,制取纯净的CuCl2。
请回答下列问题:
(1)在①步操作中使用了氧化剂,下列氧化剂中一定不能使用的是_______ 。
A.Cl2 B.NaClO C.H2O2 D.KMnO4 E.O3
(2)②步操作中的“沉淀剂”可以是下列中的_______ 。
A.NaOH B.NH3·H2O C.CuO D.Cu2(OH)2CO3 E.Fe2O3
用一种你选择的沉淀剂,分步写出除去杂质的离子方程式:_______ 。
(3)最后将滤液在HCl气流中蒸干,其目的是_______ ,如果将滤液直接加热蒸干,最后得到的固体可能是_______ 。
(4)设常温下各沉淀的溶度积近似为:Ksp[Cu(OH)2]=10-20、Ksp[Fe(OH)3]=10-38、Ksp[Fe(OH)2]=10-16;通常,人们把浓度小于10-5mol/L的离子视为“不存在”。根据所给条件,完成下列问题:
①如果该废液中CuCl2的浓度为1 mol/L,在加沉淀剂时应调节溶液的pH值范围为:_______ 。
②如果对废液不先用氧化剂,而是直接加入沉淀剂,带来的后果是:_______ 。

请回答下列问题:
(1)在①步操作中使用了氧化剂,下列氧化剂中一定不能使用的是
A.Cl2 B.NaClO C.H2O2 D.KMnO4 E.O3
(2)②步操作中的“沉淀剂”可以是下列中的
A.NaOH B.NH3·H2O C.CuO D.Cu2(OH)2CO3 E.Fe2O3
用一种你选择的沉淀剂,分步写出除去杂质的离子方程式:
(3)最后将滤液在HCl气流中蒸干,其目的是
(4)设常温下各沉淀的溶度积近似为:Ksp[Cu(OH)2]=10-20、Ksp[Fe(OH)3]=10-38、Ksp[Fe(OH)2]=10-16;通常,人们把浓度小于10-5mol/L的离子视为“不存在”。根据所给条件,完成下列问题:
①如果该废液中CuCl2的浓度为1 mol/L,在加沉淀剂时应调节溶液的pH值范围为:
②如果对废液不先用氧化剂,而是直接加入沉淀剂,带来的后果是:
您最近一年使用:0次
2 . 下列如图所示装置不能达到实验目的的是
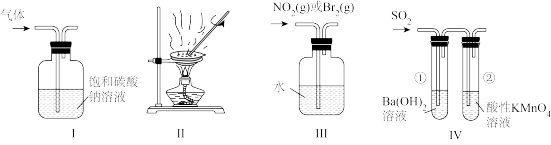

A.用装置Ⅰ除去 中的草酸蒸气 中的草酸蒸气 |
B.用装置Ⅱ蒸发 溶液得到 溶液得到 晶体 晶体 |
| C.用装置Ⅲ鉴别Br2(g)和NO2(g) |
D.用装置Ⅳ验证 的性质 的性质 |
您最近一年使用:0次
3 . 下列实验设计思路正确的是
A.用湿润的pH试纸检验 是否为酸性气体 是否为酸性气体 |
| B.直接加热饱和氯化铁溶液制氢氧化铁胶体 |
| C.除去氨气中混有的氢气,将混合气体通过灼热的氧化铜 |
| D.检验铜和浓硫酸在加热条件下是否生成铜离子,往混合溶液中加入水,观察溶液颜色是否变蓝 |
您最近一年使用:0次
名校
解题方法
4 . I.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
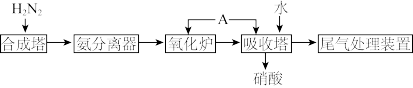
(1)写出氧化炉中的化学反应方程式_______ 。
(2)向吸收塔中通入A的作用_______ 。
(3)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用_______ (填化学式)溶液吸收。
II.为除去KCl溶液中少量的Mg2+、 ,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
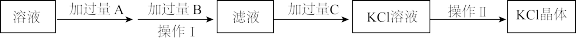
(4)上述试剂中,A是_______ ,C是_______ 。(填化学式)
(5)操作I的名称是_______ 。
(6)加过量A时发生有关反应的离子方程式为_______ 、_______ 。
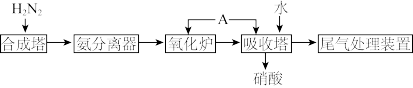
(1)写出氧化炉中的化学反应方程式
(2)向吸收塔中通入A的作用
(3)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用
II.为除去KCl溶液中少量的Mg2+、
 ,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作: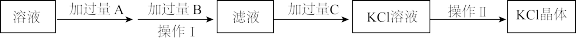
(4)上述试剂中,A是
(5)操作I的名称是
(6)加过量A时发生有关反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 重钢集团含钛高炉渣(主要成分为 ,还含有少量
,还含有少量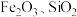 )可以用于生产
)可以用于生产 ,其工艺流程有如下两种:
,其工艺流程有如下两种:
流程Ⅰ:
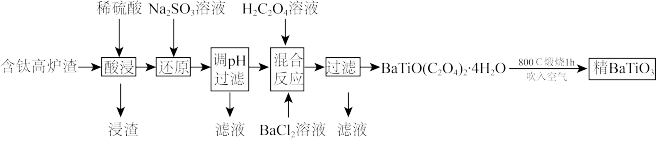
已知:a.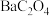 难溶于水,能溶于强酸;
难溶于水,能溶于强酸;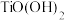 难溶于水,具有两性,溶于草酸生成
难溶于水,具有两性,溶于草酸生成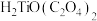 ;
;
b.相关离子[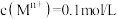 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如下表:
范围如下表:
(1)“浸渣”的成分主要是_______ 。
(2)“酸浸”后 以
以 形式存在,该反应的离子方程式为
形式存在,该反应的离子方程式为_______ 。
(3)“还原”的最终目的是_______ 。
(4)“混合反应”时,试剂添加顺序合理的是_______ (填序号)。
A.先加入过量 溶液,再加入适量
溶液,再加入适量 溶液
溶液
B.先加入过量 溶液,再加入适量
溶液,再加入适量 溶液
溶液
C.先按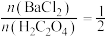 混合后,再加入反应体系中
混合后,再加入反应体系中
流程Ⅱ:
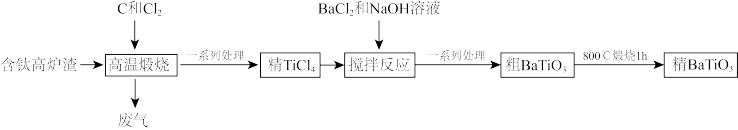
(5)实验测得,粗 的纯度为
的纯度为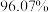 ,其中含
,其中含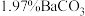 、
、 杂质,煅烧
杂质,煅烧 后,最终产品的产率和纯度(仅含微量
后,最终产品的产率和纯度(仅含微量 杂质)均明显提高。试回答下列问题:
杂质)均明显提高。试回答下列问题:
①用化学方程式解释“800℃煅烧”时产率提高的原因:_______ 。
②最终产品的纯度为_______ %(保留1位小数)。
(6)流程Ⅰ_______ (填“优于”或“劣于”)流程Ⅱ,理由是_______ 。
 ,还含有少量
,还含有少量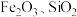 )可以用于生产
)可以用于生产 ,其工艺流程有如下两种:
,其工艺流程有如下两种:流程Ⅰ:

已知:a.
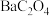 难溶于水,能溶于强酸;
难溶于水,能溶于强酸;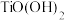 难溶于水,具有两性,溶于草酸生成
难溶于水,具有两性,溶于草酸生成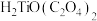 ;
;b.相关离子[
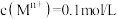 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如下表:
范围如下表:| 离子 |  |  |  |
开始沉淀的 | 0.5 | 6.3 | 1.5 |
完全沉淀的 | 2.5 | 8.3 | 2.8 |
(1)“浸渣”的成分主要是
(2)“酸浸”后
 以
以 形式存在,该反应的离子方程式为
形式存在,该反应的离子方程式为(3)“还原”的最终目的是
(4)“混合反应”时,试剂添加顺序合理的是
A.先加入过量
 溶液,再加入适量
溶液,再加入适量 溶液
溶液B.先加入过量
 溶液,再加入适量
溶液,再加入适量 溶液
溶液C.先按
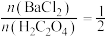 混合后,再加入反应体系中
混合后,再加入反应体系中流程Ⅱ:

(5)实验测得,粗
 的纯度为
的纯度为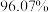 ,其中含
,其中含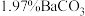 、
、 杂质,煅烧
杂质,煅烧 后,最终产品的产率和纯度(仅含微量
后,最终产品的产率和纯度(仅含微量 杂质)均明显提高。试回答下列问题:
杂质)均明显提高。试回答下列问题:①用化学方程式解释“800℃煅烧”时产率提高的原因:
②最终产品的纯度为
(6)流程Ⅰ
您最近一年使用:0次
名校
6 . 下列实验操作能达到对应目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将 通入漂白粉溶液中 通入漂白粉溶液中 | 证明 的酸性强于 的酸性强于 |
| B | 向混合溶液加入氢氧化钠,反应后静置、分液 | 除去溴苯中混有的 |
| C | 向 溶液中滴加酸性高锰酸钾溶液 溶液中滴加酸性高锰酸钾溶液 | 证明 的氧化性强于 的氧化性强于 |
| D | 将表面打磨过的铝片迅速投入正在沸腾的水中 | 验证 是否和沸水发生反应 是否和沸水发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 海水资源开发利用的部分过程如图所示。
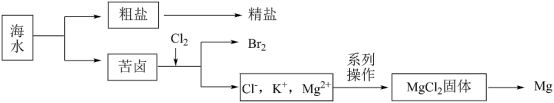
(1)向苦卤中通入Cl2制备溴的离子方程式为:___________ 。
(2)从MgCl2制取金属Mg,工业上常用___________ 方法。
(3)粗盐中含的杂质离子有Ca2+、Mg2+、SO ,提纯过程中加入试剂的顺序不正确的是
,提纯过程中加入试剂的顺序不正确的是___________
A.NaOH、BaCl2、Na2CO3、盐酸 B.BaCl2、NaOH、Na2CO3、盐酸
C.Na2CO3、BaCl2、NaOH、盐酸 D.Ba(OH)2、Na2CO3、盐酸
实验过程中,验证SO 已完全沉淀的简单操作及现象是
已完全沉淀的简单操作及现象是___________ 。
(4)加入Na2CO3溶液时发生的离子方程式为___________ 。
(5)从除杂后的氯化钠溶液中获得NaCl固体需要的仪器有铁架台(带铁圈)、酒精灯和___________ 。
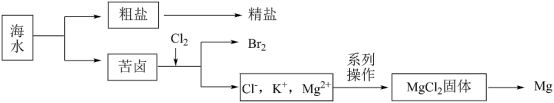
(1)向苦卤中通入Cl2制备溴的离子方程式为:
(2)从MgCl2制取金属Mg,工业上常用
(3)粗盐中含的杂质离子有Ca2+、Mg2+、SO
 ,提纯过程中加入试剂的顺序不正确的是
,提纯过程中加入试剂的顺序不正确的是A.NaOH、BaCl2、Na2CO3、盐酸 B.BaCl2、NaOH、Na2CO3、盐酸
C.Na2CO3、BaCl2、NaOH、盐酸 D.Ba(OH)2、Na2CO3、盐酸
实验过程中,验证SO
 已完全沉淀的简单操作及现象是
已完全沉淀的简单操作及现象是(4)加入Na2CO3溶液时发生的离子方程式为
(5)从除杂后的氯化钠溶液中获得NaCl固体需要的仪器有铁架台(带铁圈)、酒精灯和
您最近一年使用:0次
2022·全国·模拟预测
名校
8 . 一定量的甲苯和 溶液在100℃下发生反应,一段时间后停止反应,按如图所示流程分离出苯甲酸和回收未反应的甲苯(已知:苯甲酸的熔点为122.13℃)。
溶液在100℃下发生反应,一段时间后停止反应,按如图所示流程分离出苯甲酸和回收未反应的甲苯(已知:苯甲酸的熔点为122.13℃)。
 溶液在100℃下发生反应,一段时间后停止反应,按如图所示流程分离出苯甲酸和回收未反应的甲苯(已知:苯甲酸的熔点为122.13℃)。
溶液在100℃下发生反应,一段时间后停止反应,按如图所示流程分离出苯甲酸和回收未反应的甲苯(已知:苯甲酸的熔点为122.13℃)。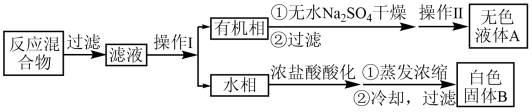
| A.操作I是分液,操作II是蒸馏 |
| B.定性检验无色液体A的试剂可以是酸性高锰酸钾溶液 |
| C.在实验室中,蒸发浓缩操作中所用到的仪器主要有坩埚,泥三角,三脚架,酒精灯 |
| D.可通过测定熔点验证白色固体B是否为纯净物 |
您最近一年使用:0次
2022-03-24更新
|
766次组卷
|
8卷引用:重庆市西南大学附属中学2022-2023学年高二下学期期中考试化学试题
重庆市西南大学附属中学2022-2023学年高二下学期期中考试化学试题(已下线)高考化学预测卷(三)广东省汕头市潮阳林百欣中学2021-2022学年高二下学期期中考试化学试题安徽省怀宁中学2021-2022学年高二下学期期中考试化学试题天津市重点校2022-2023学年高二下学期期末联考化学试题云南省宣威市第六中学2023-2024学年高二上学期10月月考化学试题广东省广州市越秀区广东实验中学2023-2024学年高二下学期5月期中考试化学试题(已下线)题型05 有机实验分析-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)
名校
解题方法
9 . 工业上由粗锰粉(主要杂质为Fe、Ni、Pb等金属单质)制备高纯碳酸锰。其主要工艺流程如下:

下列有关说法不正确 的是

下列有关说法
| A.可以通过搅拌的方式提高“酸浸”时粗锰粉的浸取率 |
B.向酸浸后的滤液中加入 ,反应的离子方程式为: ,反应的离子方程式为: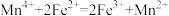 |
C.除铁时加入的物质X可以为 ,使 ,使 转化为 转化为 沉淀而除去 沉淀而除去 |
D.取除铁后的滤液,加入几滴KSCN溶液,无明显现象证明 已除尽 已除尽 |
您最近一年使用:0次
2022-01-23更新
|
217次组卷
|
3卷引用:重庆市缙云教育联盟2021-2022学年高二下学期4月质量检测化学试题
名校
10 . 医用 用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为
用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为 、含少量
、含少量 、
、 、
、 、
、 等杂质)为原料制备
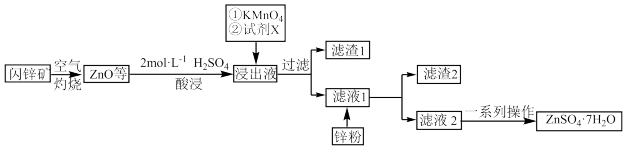
等杂质)为原料制备 的流程如图:
的流程如图:
 金属阳离子沉淀的
金属阳离子沉淀的 如下表
如下表
回答下列问题:
(1)实验室进行“灼烧”操作时在___________ (填仪器名称)中进行,闪锌矿在灼烧时产生的有毒气体的分子式为___________ 。写出一种提高“酸浸”浸出率的方法:___________ 。
(2)向浸出液中加入 溶液的目的是除去浸出液中的
溶液的目的是除去浸出液中的 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。同时加入试剂 调节
调节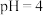 除去
除去 ,试剂X可以为
,试剂X可以为___________ (填化学式)。
(3)加入锌粉可以除去滤液中的 、
、 ,除去
,除去 的离子方程式为
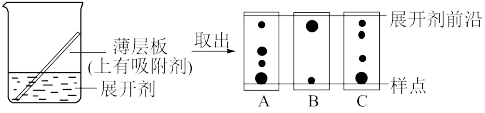
的离子方程式为___________ 。薄层色谱法是一种对混合样品进行快速分离和定性分析的一种实验技术,原理是利用样品中不同组分对同一吸附剂(固定相)的吸附能力不同,在展开剂溶液(移动相)流过吸附剂时,各组分就以不同速率随展开剂扩散,最后达到分析分离的目的。某实验小组利用薄层色谱法监控上述用 除去
除去 、
、 反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是
反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是___________ (填字母)。
(4)滤液2得到 的一系列操作为:加入
的一系列操作为:加入 调节溶液
调节溶液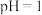 、
、___________ 、减压过滤、洗涤、干燥。
(5)某化工厂用mt闪锌矿(含 )制备
)制备 ,最后制得
,最后制得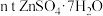 ,忽略工艺中后引入的锌元素,
,忽略工艺中后引入的锌元素, 的产率为
的产率为___________ (用含m、n、w的代数式表示)。
 用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为
用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为 、含少量
、含少量 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的流程如图:
的流程如图:
 金属阳离子沉淀的
金属阳离子沉淀的 如下表
如下表| 金属离子 |  |  |  |  |  |  |
开始沉淀 | 8.1 | 6.7 | 1.9 | 6.1 | 7.2 | 7.7 |
完全沉淀 | 10.1 | 9.0 | 3.2 | 8.2 | 9.2 | 9.7 |
回答下列问题:
(1)实验室进行“灼烧”操作时在
(2)向浸出液中加入
 溶液的目的是除去浸出液中的
溶液的目的是除去浸出液中的 ,该反应的离子方程式为
,该反应的离子方程式为 调节
调节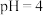 除去
除去 ,试剂X可以为
,试剂X可以为(3)加入锌粉可以除去滤液中的
 、
、 ,除去
,除去 的离子方程式为
的离子方程式为 除去
除去 、
、 反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是
反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是
(4)滤液2得到
 的一系列操作为:加入
的一系列操作为:加入 调节溶液
调节溶液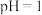 、
、(5)某化工厂用mt闪锌矿(含
 )制备
)制备 ,最后制得
,最后制得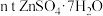 ,忽略工艺中后引入的锌元素,
,忽略工艺中后引入的锌元素, 的产率为
的产率为
您最近一年使用:0次



