解题方法
1 . 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:_______ 。
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
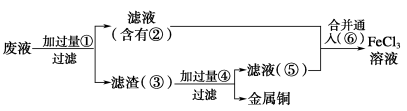
A.请写出上述实验中加入或生成的有关物质的化学式。
①_______ ,②_______ ,③_______ ,④_______ 。
B.请写出相关反应的化学方程式。
i.加过量①_______ ,_______ ;
ii.加过量④_______ 。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式:
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

A.请写出上述实验中加入或生成的有关物质的化学式。
①
B.请写出相关反应的化学方程式。
i.加过量①
ii.加过量④
您最近一年使用:0次
解题方法
2 . 镁铝合金在交通、航空,电子等行业有着广泛的应用。某化学兴趣小组对镁铝合金废料进行回收利用,实验中可将铝转化为硫酸铝晶体,并对硫酸铝晶体进行热重分析。镁铝合金废料转化为硫酸铝晶体的实验流程如图:

回答下列问题:
(1)向镁铝合金中加入NaOH溶液,写出发生反应的化学方程式:______ 。固体A、B的主要成分分别为_____ 、_____ (填化学式)。
(2)操作II包含的实验步骤:蒸发浓缩、_____ 、______ 、洗涤、干燥。
(3)操作II中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是:______ 。
(4)若初始时称取的镁铝合金废料的质量为9.00g,得到固体A的质量为4.95g,硫酸铝晶体的质量为49.95g(假设每一步的转化率均为100%,合金废料中不含溶于碱的杂质)。
①硫酸铝的摩尔质量为______ 。
②硫酸铝晶体的化学式为______ 。

回答下列问题:
(1)向镁铝合金中加入NaOH溶液,写出发生反应的化学方程式:
(2)操作II包含的实验步骤:蒸发浓缩、
(3)操作II中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是:
(4)若初始时称取的镁铝合金废料的质量为9.00g,得到固体A的质量为4.95g,硫酸铝晶体的质量为49.95g(假设每一步的转化率均为100%,合金废料中不含溶于碱的杂质)。
①硫酸铝的摩尔质量为
②硫酸铝晶体的化学式为
您最近一年使用:0次
名校
解题方法
3 . 海水是一个资源宝库,能从海水中提取大量有用的物质。图是从海水中获得的粗盐(含泥沙、少量MgCl2、CaCl2和Na2SO4等杂质)提纯的流程,回答下列问题:
(注意:abc试剂加入的量都是过量的)

(1)操作1是_______ ,操作2是_______
(2)a、b、c是试剂①氯化钡溶液 ②氢氧化钠溶液 ③碳酸钠溶液中的一种,则加入试剂的正确顺序有_______
A.①②③ B.①③② C.②①③ D.②③① E.③①② F.③②①
(3)写出加入碳酸钠溶液发生的离子方程式: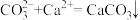 和
和_______
(4)试剂d是一种酸,它是_______ ,写出加入试剂d发生的离子方程式H+ + OH-= H2O和_______
(注意:abc试剂加入的量都是过量的)

(1)操作1是
(2)a、b、c是试剂①氯化钡溶液 ②氢氧化钠溶液 ③碳酸钠溶液中的一种,则加入试剂的正确顺序有
A.①②③ B.①③② C.②①③ D.②③① E.③①② F.③②①
(3)写出加入碳酸钠溶液发生的离子方程式:
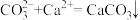 和
和(4)试剂d是一种酸,它是
您最近一年使用:0次
2022-12-09更新
|
146次组卷
|
2卷引用:广东省深圳市龙华高级中学教育集团2021-2022学年高一上学期第一次段考化学试题
4 . 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋植物中提取碘的流程如图:

某化学兴趣小组将上述流程②③设计成如图所示。
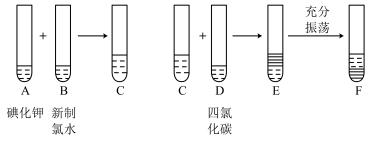
已知氯水中含有 ,②中发生反应的化学方程式为
,②中发生反应的化学方程式为 。回答下列问题:
。回答下列问题:
(1)写出提取过程①③中实验操作的名称:①_______ ,③_______ 。
(2)F中的现象是_______ 。
(3)从碘的四氯化碳溶液中得到单质碘还需进行的操作是_______ 。实验装置如图所示,该实验采用的加热方式为_______ 。
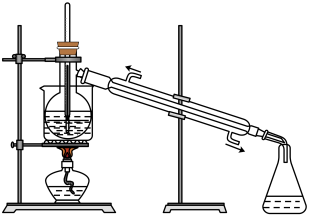
(4)现用 从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL 加入分液漏斗中,并盖好玻璃塞;
加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
完成下列填空:
①正确操作步骤的顺序是:(用上述各操作的编号字母填写)
_______ →_______ →_______ →A→_______ →G→E→F
②上述G步骤操作的目的是_______ 。

某化学兴趣小组将上述流程②③设计成如图所示。

已知氯水中含有
 ,②中发生反应的化学方程式为
,②中发生反应的化学方程式为 。回答下列问题:
。回答下列问题:(1)写出提取过程①③中实验操作的名称:①
(2)F中的现象是
(3)从碘的四氯化碳溶液中得到单质碘还需进行的操作是

(4)现用
 从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL
 加入分液漏斗中,并盖好玻璃塞;
加入分液漏斗中,并盖好玻璃塞;C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
完成下列填空:
①正确操作步骤的顺序是:(用上述各操作的编号字母填写)
②上述G步骤操作的目的是
您最近一年使用:0次
解题方法
5 . 某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色沉淀,I为红褐色沉淀。
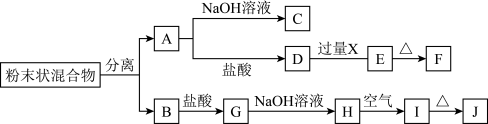
(此转化关系中所用的试剂都是足量的)
(1)写出下列物质的化学式:F_______ G_______
(2)将混合物中两种金属分离开的最简单的方法是_______ 。
(3)写出下列转化的离子方程式:A→C:_______

(此转化关系中所用的试剂都是足量的)
(1)写出下列物质的化学式:F
(2)将混合物中两种金属分离开的最简单的方法是
(3)写出下列转化的离子方程式:A→C:
您最近一年使用:0次
解题方法
6 . 粗盐中含有泥沙以及 、
、 、SO
、SO 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程:

某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(1)操作②、④的名称是_______ 。
(2)操作③按a、b、c顺序依次加入过量的试剂,若a为NaOH溶液,则c为_______ ,加入a发生反应的离子方程式为_______ 。
(3)加盐酸调溶液pH的目的是_______ 。
(4)步骤⑥操作名称是_______ 。
 、
、 、SO
、SO 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程:
某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(1)操作②、④的名称是
(2)操作③按a、b、c顺序依次加入过量的试剂,若a为NaOH溶液,则c为
(3)加盐酸调溶液pH的目的是
(4)步骤⑥操作名称是
您最近一年使用:0次
解题方法
7 . 为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)检验粗盐中含有 方法是
方法是_______ 。
(2)在 中填写所使用除杂试剂的化学式
中填写所使用除杂试剂的化学式_______ ,在( )中的操作名称是_______ 。
(3)步骤②和④所加试剂顺序能否颠倒?_______ (填“能”或“否”),如不能请说明原因_______ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)检验粗盐中含有
 方法是
方法是(2)在
 中填写所使用除杂试剂的化学式
中填写所使用除杂试剂的化学式(3)步骤②和④所加试剂顺序能否颠倒?
您最近一年使用:0次
名校
8 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池板的是_________ (填化学式)。
(2)工艺师常用氢氟酸雕刻玻璃,该反应的化学方程式为_________ 。
(3)兵马俑中所用颜料成分之一为蓝紫色的硅酸铜钡(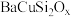 铜为
铜为 价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
(4)工业上提纯硅有多种路线,其中一种工艺流程如图:

①电弧炉中发生反应的化学方程式为_________ 。
②在流化床反应的产物中, 大约占85%,还有
大约占85%,还有 等,有关物质的沸点数据如表,则提纯
等,有关物质的沸点数据如表,则提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和_________ 。
③整个制作过程必须严格控制无水、无氧, 遇水剧烈反应生成
遇水剧烈反应生成 、
、 气体和另一种物质,该反应的化学方程式为
气体和另一种物质,该反应的化学方程式为_________ 。
(1)可用于制作计算机芯片和太阳能电池板的是
(2)工艺师常用氢氟酸雕刻玻璃,该反应的化学方程式为
(3)兵马俑中所用颜料成分之一为蓝紫色的硅酸铜钡(
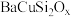 铜为
铜为 价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。A.可用氧化物形式表示为 | B.性质稳定,不易脱色 |
| C.x等于6 | D.易溶解于强酸和强碱 |

①电弧炉中发生反应的化学方程式为
②在流化床反应的产物中,
 大约占85%,还有
大约占85%,还有 等,有关物质的沸点数据如表,则提纯
等,有关物质的沸点数据如表,则提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和| 物质 |  |  |  | 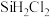 | 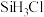 |  |  |
沸点/ | 2355 | 57.6 | 31.8 | 8.2 |  |  |  |
③整个制作过程必须严格控制无水、无氧,
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 气体和另一种物质,该反应的化学方程式为
气体和另一种物质,该反应的化学方程式为
您最近一年使用:0次
解题方法
9 . 印刷电路板(PCB)是用腐蚀液(FeCl3溶液)将覆铜板上的部分铜腐蚀掉而制得。一种制作PCB并将腐蚀后废液(其中金属阳离子主要含Fe3+、Cu2+、Fe2+)回收再生的流程如图。

请回答:
(1)腐蚀池中发生反应的化学方程式是_____ 。
(2)上述各池中,没有发生化学变化的是_____ 池。
(3)由置换池中得到固体的操作名称是_____ 。
(4)置换池中发生反应的离子方程式有_____ 。
(5)向再生池中通入Cl2也可以使废液再生,相比Cl2,用双氧水的优点是_____ 。

请回答:
(1)腐蚀池中发生反应的化学方程式是
(2)上述各池中,没有发生化学变化的是
(3)由置换池中得到固体的操作名称是
(4)置换池中发生反应的离子方程式有
(5)向再生池中通入Cl2也可以使废液再生,相比Cl2,用双氧水的优点是
您最近一年使用:0次
10 . 除去下列物质中杂质,选用试剂和操作方法不正确 的是。
| 选项 | 物质 | 所含 | 除去杂质的试剂或方法 |
| A | CaO固体 | CaCO3固体 | 加热 |
| B | Cu | Fe | 加过量的稀盐酸后过滤,洗涤,干燥 |
| C | NaCl | KNO3 | 硝银溶液 |
| D | CO2 | CO | 通过灼热的氧化铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



