解题方法
1 . 某固体可能含有 、Cu2+、Na+、Cl-、
、Cu2+、Na+、Cl-、 、
、 中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.27g,在沉淀中加入过量稀盐酸,仍有2.33g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)。
下列说法正确的是
 、Cu2+、Na+、Cl-、
、Cu2+、Na+、Cl-、 、
、 中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.27g,在沉淀中加入过量稀盐酸,仍有2.33g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)。
下列说法正确的是
A.该固体中一定含有 、 、 、 、 、Na+ 、Na+ |
| B.该固体中一定没有Cu2+、Cl-、Na+ |
C.该固体中只含有 、 、 、 、 、Cl- 、Cl- |
| D.根据以上实验,无法确定该固体中有Na+ |
您最近一年使用:0次
2017-04-11更新
|
263次组卷
|
2卷引用:2016-2017学年上海市青浦区高三上学期期终学业质量调研测试化学试卷
2 . 某溶液中可能含有H+、Na+、NH 、Mg2+、Fe3+、Al3+、SO
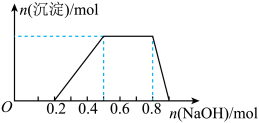
、Mg2+、Fe3+、Al3+、SO 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关对该溶液的判断不正确的是
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关对该溶液的判断不正确的是
 、Mg2+、Fe3+、Al3+、SO
、Mg2+、Fe3+、Al3+、SO 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关对该溶液的判断不正确的是
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关对该溶液的判断不正确的是
A.该溶液中肯定含有的离子是H+、NH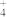 、Al3+、SO 、Al3+、SO |
| B.肯定不含的阳离子是Mg2+、Fe3+ |
| C.要确定该溶液是否含有Na+,必须做焰色反应实验,看焰色是否为黄色 |
D.该溶液中肯定含有的离子的物质的量之比为n(H+):n(NH ):n(Al3+):n(SO ):n(Al3+):n(SO )=2:3:1:4 )=2:3:1:4 |
您最近一年使用:0次
2017-04-09更新
|
289次组卷
|
4卷引用:2016-2017学年黑龙江省虎林市高级中学高一下学期第二次月考化学试卷
3 . 某小组为探究AgNO3溶液和不同类型盐溶液反应的多样性,设计如下实验:
已知:AgSCN为白色难溶物;(SCN)2与卤素单质性质相似,(SCN)2为有色物质。
(1)①中的白色沉淀是___________________ 。
(2)分离并洗涤①的沉淀,滴加0.5mol/L KI溶液,白色沉淀转变为黄色沉淀,用离子方程式解释上述变化____________________________ 。
(3)②中可能发生的离子反应有_________________ 。
(4)实验①的设计目的_______________________ 。
(5)对于③中红色褪去的原因及Ag+与SCN-反应的情况,小组进行以下分析和设计:
Ⅰ.甲同学认为,红色褪去的原因与平衡移动原理有关,解释为_________________ 。
Ⅱ.乙同学为了探究③中是否发生Ag+氧化SCN-的反应,又设计以下对比实验:
现象:生成白色沉淀,长时间观察,溶液和沉淀均未发生颜色改变。
Ⅲ.丙同学认为,理论上Ag+能够氧化SCN-,为证明其猜想,设计如下实验:
现象:电流计指针发生偏转,a电极上产生具有金属光泽的物质,b电极附近的溶液发生颜色变化。
丙同学的设计在证明氧化还原反应的优点是___________________________ 。
(6)通过以上探究,得出AgNO3溶液和不同类型盐溶液反应多样性的结论是______ 。

已知:AgSCN为白色难溶物;(SCN)2与卤素单质性质相似,(SCN)2为有色物质。
(1)①中的白色沉淀是
(2)分离并洗涤①的沉淀,滴加0.5mol/L KI溶液,白色沉淀转变为黄色沉淀,用离子方程式解释上述变化
(3)②中可能发生的离子反应有
(4)实验①的设计目的
(5)对于③中红色褪去的原因及Ag+与SCN-反应的情况,小组进行以下分析和设计:
Ⅰ.甲同学认为,红色褪去的原因与平衡移动原理有关,解释为
Ⅱ.乙同学为了探究③中是否发生Ag+氧化SCN-的反应,又设计以下对比实验:
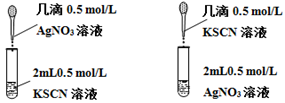
现象:生成白色沉淀,长时间观察,溶液和沉淀均未发生颜色改变。
Ⅲ.丙同学认为,理论上Ag+能够氧化SCN-,为证明其猜想,设计如下实验:

现象:电流计指针发生偏转,a电极上产生具有金属光泽的物质,b电极附近的溶液发生颜色变化。
丙同学的设计在证明氧化还原反应的优点是
(6)通过以上探究,得出AgNO3溶液和不同类型盐溶液反应多样性的结论是
您最近一年使用:0次
4 . 下列有关实验的设计、现象、结论均正确的是
| A.加热固体,用湿润的红色石蕊试纸靠近,看颜色变化,用此法鉴别固体是否为铵盐 |
| B.用短胶头滴管向FeSO4溶液滴加NaOH溶液,产生的白色沉淀可长时间存在 |
| C.将金属钠投入CuSO4溶液,可观察到有红色固体析出 |
| D.向25mL沸腾的蒸馏水中逐滴加入5-6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色, 停止加热,便得到Fe(OH)3胶体 |
您最近一年使用:0次
名校
5 . 某实验小组探究少量Cl2和FeBr2反应的过程。
(1)配制FeBr2溶液:
ⅰ.配制50mL1.0mol/LFeBr2溶液;
ⅱ.上述溶液呈淡黄色。取少量此溶液,向其中滴入KSCN溶液,变为浅红色。
①配制50mL1.0mol/LFeBr2溶液需要的玻璃容器是________________ 。
②由ⅱ可知,此FeBr2溶液呈黄色的原因是其中含有________ ,用离子方程式解释产生其原因:_______ 。
(2)氯气和FeBr2反应实验操作及现象如下:
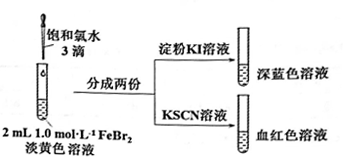
据此甲同学得出结论:少量Cl2既能和Fe2+又能和Br-发生氧化还原反应。
①Cl2和Fe2+发生反应的离子方程式是________________ 。
②乙同学认为上述实验不能证明Cl2和Br-发生反应,理由是_____________ 。
③乙同学改进实验如下:在上述FeBr2溶液中加入过量铁粉,取上清液2 mL,向其中滴加3滴饱和氯水后,再加入CCl4,振荡后静置,观察现象。乙得出结论:少量Cl2只与Fe2+反应,不与Br-反应。乙得出该结论依据的实验现象是____________________ 。
(3)丙同学继续设计实验,探究反应过程:
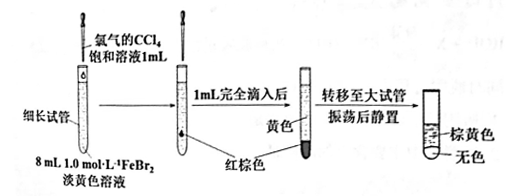
①转移到大试管前CCl4液体中呈红棕色的物质是___________ 。
②丙通过此实验可得出结论:________ 。
(1)配制FeBr2溶液:
ⅰ.配制50mL1.0mol/LFeBr2溶液;
ⅱ.上述溶液呈淡黄色。取少量此溶液,向其中滴入KSCN溶液,变为浅红色。
①配制50mL1.0mol/LFeBr2溶液需要的玻璃容器是
②由ⅱ可知,此FeBr2溶液呈黄色的原因是其中含有
(2)氯气和FeBr2反应实验操作及现象如下:

据此甲同学得出结论:少量Cl2既能和Fe2+又能和Br-发生氧化还原反应。
①Cl2和Fe2+发生反应的离子方程式是
②乙同学认为上述实验不能证明Cl2和Br-发生反应,理由是
③乙同学改进实验如下:在上述FeBr2溶液中加入过量铁粉,取上清液2 mL,向其中滴加3滴饱和氯水后,再加入CCl4,振荡后静置,观察现象。乙得出结论:少量Cl2只与Fe2+反应,不与Br-反应。乙得出该结论依据的实验现象是
(3)丙同学继续设计实验,探究反应过程:

①转移到大试管前CCl4液体中呈红棕色的物质是
②丙通过此实验可得出结论:
您最近一年使用:0次
2017-03-15更新
|
785次组卷
|
4卷引用:2017届北京市海淀区高三3月适应性考试(零模)理综化学试卷
2017届北京市海淀区高三3月适应性考试(零模)理综化学试卷2020届高考化学二轮复习大题精准训练——反应原理(历程)的探究式实验(已下线)专题6.2 实验综合题(必考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升北京市中央民族大学附属中学2022届高三9月月考化学试题
名校
解题方法
6 . 硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]是透明、浅蓝绿色晶体,易溶于水而不溶于酒精等有机溶剂,在空气中一般比较稳定,不易被氧化。制备步骤如下:
步骤1.称取还原铁粉0.4g,炭粉0.3g,放入50mL 锥形瓶中,加入3.5 mL2mol·L-1硫酸置于60℃ 热水浴中加热(如下左图),待反应完全,取出冷却,再加入6 mol·L-1的硫酸2 mL。
步骤2.在上述反应液中加入浓氨水0.8 mL,振荡混匀,抽滤(如上右图)。向滤液中加入10mL无水乙醇,静置,大量晶体析出,倾析,再次抽滤。
步骤3.取出晶体,用干净的滤纸吸干,称量并分析样品。
请回答下列问题:
(1)步骤1中炭粉的作用是_______ ,加入6 mol·L-1硫酸的作用是____________ 。
(2)向滤液中加入无水乙醇目的是_________________ 。
(3)产品中金属阳离子的检验方法及现象________________ 。
(4)称取获得的硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](摩尔质量为392g·mol-1)1.9600 g 配成100mL溶液,取出20.00mL滴加稀H2SO4酸化后用0 . 0100 mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液为18.00mL 。
下列有关滴定的操作正确的是_(填字母编号)。
a.滴定过程中眼睛注视滴定管中液面变化
b.滴定完成后取下滴定管握住中部防止掉落
c.读数过程中保持滴定管自然悬垂
d.读数时视线与刻度线、凹液面最低处切线相平齐
滴定过程中反应离子方程式为____________ ,制得硫酸亚铁铵样品的纯度为__________ 。
步骤1.称取还原铁粉0.4g,炭粉0.3g,放入50mL 锥形瓶中,加入3.5 mL2mol·L-1硫酸置于60℃ 热水浴中加热(如下左图),待反应完全,取出冷却,再加入6 mol·L-1的硫酸2 mL。

步骤2.在上述反应液中加入浓氨水0.8 mL,振荡混匀,抽滤(如上右图)。向滤液中加入10mL无水乙醇,静置,大量晶体析出,倾析,再次抽滤。
步骤3.取出晶体,用干净的滤纸吸干,称量并分析样品。
请回答下列问题:
(1)步骤1中炭粉的作用是
(2)向滤液中加入无水乙醇目的是
(3)产品中金属阳离子的检验方法及现象
(4)称取获得的硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](摩尔质量为392g·mol-1)1.9600 g 配成100mL溶液,取出20.00mL滴加稀H2SO4酸化后用0 . 0100 mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液为18.00mL 。
下列有关滴定的操作正确的是_(填字母编号)。
a.滴定过程中眼睛注视滴定管中液面变化
b.滴定完成后取下滴定管握住中部防止掉落
c.读数过程中保持滴定管自然悬垂
d.读数时视线与刻度线、凹液面最低处切线相平齐
滴定过程中反应离子方程式为
您最近一年使用:0次
2017-03-15更新
|
369次组卷
|
2卷引用:2017届安徽省“江南十校”高三3月联考理综化学试卷
7 . 下列实验方法能达到实验目的的是
| A.用KMnO4溶液鉴别甲烷和乙烯 |
| B.用焰色反应鉴别KNO3和KCl |
| C.用BaCl2溶液鉴别Na2CO3和Na2SO4 |
| D.用NaOH溶液除去Cl2中含有的少量HCl |
您最近一年使用:0次
2017-03-13更新
|
154次组卷
|
3卷引用:2016-2017学年江苏省扬州市高二第二次(3月)学业水平模拟测试化学试卷
8 . 下列离子检验的方法正确的是
| A.向某无色溶液中加入BaCl2溶液,产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有SO42- |
| B.向某无色溶液中加入盐酸,有无色、无味的气体产生,则说明原溶液中一定有CO32- |
| C.灼烧某白色粉末,火焰呈黄色,则说明原粉末中有Na+,无K+ |
| D.向某溶液中滴加硫氰化钾溶液,溶液不变红,再滴加氯水,溶液变红,说明原溶液一定有Fe2+ |
您最近一年使用:0次
2017-03-11更新
|
144次组卷
|
4卷引用:2016-2017学年河北省张家口市高一上学期期末考试化学试卷
9 . 已知还原性:SO32->I-。某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如下实验:
下列说法正确的是

下列说法正确的是
| A.溶液X肯定只存在NH4+、SO42- |
| B.溶液X一定不含有Ba2+、Fe3+,可能含有I- |
| C.为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液 |
| D.为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧 |
您最近一年使用:0次
2017-03-11更新
|
511次组卷
|
2卷引用:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试题
10 . 某工厂的污水中可能含有NH4+、Fe2+、Cl-、Fe3+、SO42-、HCO3-离子中的一种或几种,为检验上述离子,某兴趣小组设计了如下实验方案,请回答下列问题:
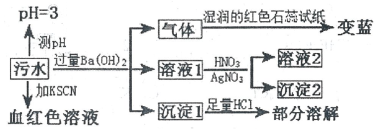
下列说法正确的是

下列说法正确的是
| A.该污水中一定存在Fe3+,不存在Fe2+ | B.沉淀l为BaCO3和BaSO4 |
| C.沉淀2可能为AgCl和Ag2SO4 | D.该污水中一定存在NH4+、Cl-、Fe3+、SO42-离子 |
您最近一年使用:0次



