1 . 某溶液X中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理正确的是
中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理正确的是
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理正确的是
中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理正确的是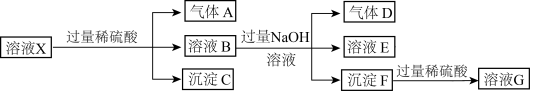
A.生成气体A为 |
B.溶液X中一定不存在 和 和 |
| C.气体D能使湿润的蓝色石蕊试纸变红 |
D.溶液G中一定含有的阳离子为 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
2 . 工业上以黄铁矿为原料利用“接触法”制硫酸,并利用硫酸渣(主要含 、
、 、
、 ,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。
,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。 外还有
外还有_______ 。
(2)以下有关说法不正确的是_______。
(3)“氧化”中,生成FeOOH的离子方程式为_______ 。
(4)“酸溶”过程中ρ(溶液的质量浓度)及F(溶液的酸度)与w( 质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数
质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数_______ (填“增大”“减小”或“不变”)。_______ 。
 、
、 、
、 ,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。
,其它杂质不考虑)生产铁基颜料铁黄(FeOOH)的制备流程如图所示。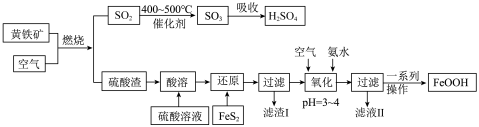
 外还有
外还有(2)以下有关说法不正确的是_______。
A.工业上用98.3%的浓硫酸吸收生成的 |
B. 和 和 都属于酸性氧化物,通到 都属于酸性氧化物,通到 溶液中都会产生白色沉淀 溶液中都会产生白色沉淀 |
C.FeOOH、 中均含有非极性共价键 中均含有非极性共价键 |
D.氟氢化钾(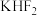 )与发烟硫酸反应可生成氟磺酸( )与发烟硫酸反应可生成氟磺酸(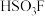 ),说明硫酸的酸性大于氟磺酸 ),说明硫酸的酸性大于氟磺酸 |
(3)“氧化”中,生成FeOOH的离子方程式为
(4)“酸溶”过程中ρ(溶液的质量浓度)及F(溶液的酸度)与w(
 质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数
质量分数)之间的关系如右图所示。当F值恒定时,随溶液质量浓度增大,所需硫酸的质量分数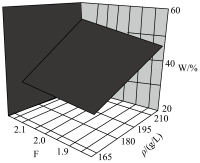
您最近一年使用:0次
名校
3 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。请回答下列问题: 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。
请回答:
(1)写出肼的电子式______ 。
(2)写出反应I的化学方程式______ 。
(3)下列说法正确的是______。
(4)已知: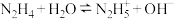 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
①生成的气体M和白色沉淀N的成分分别是______ 、______ (填化学式)。
②请设计实验验证白色沉淀N的组成元素______ 。

已知:①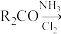
 (异肼)
(异肼)
 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。请回答:
(1)写出肼的电子式
(2)写出反应I的化学方程式
(3)下列说法正确的是______。
A.碱性: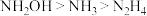 |
| B.肼可以用做还原剂,也可用做配合物的配体 |
| C.肼在水中的溶解度小于在苯中的溶解度 |
| D.反应Ⅱ中的产物之一可以循环利用 |
(4)已知:
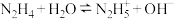 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。①生成的气体M和白色沉淀N的成分分别是
②请设计实验验证白色沉淀N的组成元素
您最近一年使用:0次
4 . 为实现实验目的,选用的玻璃仪器及试剂不合理的是
选项 | 实验目的 | 玻璃仪器 | 试剂 |
A | 探究金属离子对反应速率的影响 | 试管、量筒、胶头滴管 | 双氧水、 |
B | 验证纤维素水解 | 试管、玻璃棒、胶头滴管、酒精灯 | 蒸馏水、浓硫酸、 |
C | 验证乙醇发生消去反应 | 酒精灯、温度计、圆底烧瓶、试管、导管、量筒 | 乙醇、浓硫酸、 |
D | 检验菠菜中含有铁元素 | 试管、烧杯、胶头滴管、玻璃棒 | 蒸馏水、稀硝酸、 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
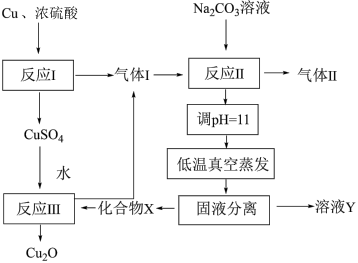
5 . 一种制备 的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。
的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。
已知:常温下, 的电离平衡常数
的电离平衡常数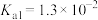 ,
,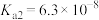 。
。
请回答: 的化学方程式为
的化学方程式为___________ 。
(2)反应 的离子反应方程式为
的离子反应方程式为___________ 。
(3)下列说法正确的是___________。
(4)反应 需及时补加NaOH以保持反应在pH=5条件下进行,原因是
需及时补加NaOH以保持反应在pH=5条件下进行,原因是___________ (结合离子反应方程式和必要的文字说明)。
(5)请用实验验证反应 后的溶液中存在的阳离子
后的溶液中存在的阳离子___________ 。
 的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。
的工艺路线如图所示。反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以保持反应在pH=5条件下进行。已知:常温下,
 的电离平衡常数
的电离平衡常数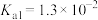 ,
,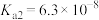 。
。请回答:
 的化学方程式为
的化学方程式为(2)反应
 的离子反应方程式为
的离子反应方程式为(3)下列说法正确的是___________。
A.反应 、 、 、 、 均为氧化还原反应 均为氧化还原反应 |
B.低温真空蒸发主要目的是防止 分解 分解 |
C.溶液Y可循环用于反应 所在操作单元吸收气体 所在操作单元吸收气体 |
D.若 产量不变,参与反应 产量不变,参与反应 的X与 的X与 物质的量之比 物质的量之比 增大时,需补加NaOH的量减少 增大时,需补加NaOH的量减少 |
(4)反应
 需及时补加NaOH以保持反应在pH=5条件下进行,原因是
需及时补加NaOH以保持反应在pH=5条件下进行,原因是(5)请用实验验证反应
 后的溶液中存在的阳离子
后的溶液中存在的阳离子
您最近一年使用:0次
6 . 下列物质的检验中,其结论一定正确的是
A.向某无色溶液中加入NaOH溶液,微热,用湿润的红色石蕊试纸在试管口检验,试纸变蓝色,说明溶液中含有 |
B.向某溶液中加入盐酸产生无色无味的气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 |
C.向某溶液中加入 溶液,产生白色沉淀,加入稀 溶液,产生白色沉淀,加入稀 后,白色沉淀不溶解,也无其它现象,说明原溶液中一定含有 后,白色沉淀不溶解,也无其它现象,说明原溶液中一定含有 |
D.将某气体通入品红溶液中,品红溶液褪色,该气体定是 |
您最近一年使用:0次
7 . 下列“实验结论”与“实验操作及现象”不相符 的一组是
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有 |
| 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和漂白性物质 |
C | 向某溶液中加入浓 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中一定含有 |
D | 向某溶液中加入足量稀盐酸,无明显现象,再加入 溶液,有白色沉淀产生 溶液,有白色沉淀产生 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
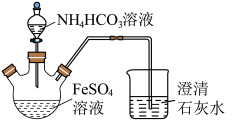
8 . 碳酸亚铁(FeCO3)难溶于水,常用于制取铁盐或补血剂。一种FeCO3的制备装置如图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得FeCO3沉淀。______________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:__________________ 。
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程_________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O
 =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
您最近一年使用:0次
解题方法
9 . 某透明溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子(浓度均为
中的几种离子(浓度均为 )。常温下,对其进行如下实验操作:
)。常温下,对其进行如下实验操作:
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子(浓度均为
中的几种离子(浓度均为 )。常温下,对其进行如下实验操作:
)。常温下,对其进行如下实验操作: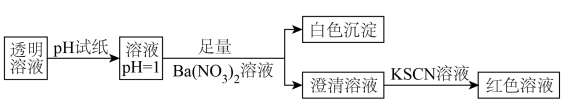
| A.实验过程中有氧化还原反应发生 |
B.无法判断原溶液中是否含有 |
C.原溶液中一定不含 、 、 、 、 、 、 、 、 、 、 |
D.原溶液中一定含有 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.现有某固体混合物,可能由 中的若干种物质组成,设计部分实验方案探究该固体混合物的成分(如图),所加试剂均过量。
中的若干种物质组成,设计部分实验方案探究该固体混合物的成分(如图),所加试剂均过量。
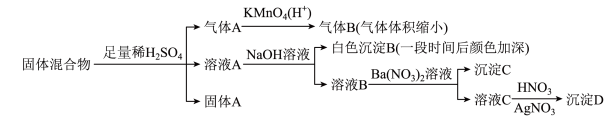
(1)该固体混合物中一定含有___________ 。
(2)写出气体A通入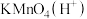 后,气体体积缩小所发生反应的离子方程式
后,气体体积缩小所发生反应的离子方程式___________ 。
(3)写出白色沉淀B放置在空气中发生反应的化学方程式___________ 。
Ⅱ.某溶液中只可能含有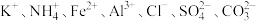 中的若干种离子,离子浓度均为
中的若干种离子,离子浓度均为 。某同学进行了如下实验:
。某同学进行了如下实验:
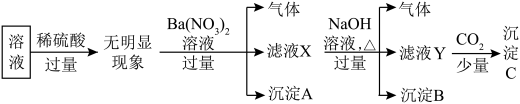
(4)原溶液中一定不存在的离子是___________ 。
(5)沉淀C的成分是___________ (写化学式)。
(6)写出加入过量 时产生气体的离子方程式
时产生气体的离子方程式___________ ,检验产物中的阳离子所用试剂及现象为___________ 。
 中的若干种物质组成,设计部分实验方案探究该固体混合物的成分(如图),所加试剂均过量。
中的若干种物质组成,设计部分实验方案探究该固体混合物的成分(如图),所加试剂均过量。
(1)该固体混合物中一定含有
(2)写出气体A通入
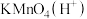 后,气体体积缩小所发生反应的离子方程式
后,气体体积缩小所发生反应的离子方程式(3)写出白色沉淀B放置在空气中发生反应的化学方程式
Ⅱ.某溶液中只可能含有
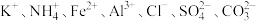 中的若干种离子,离子浓度均为
中的若干种离子,离子浓度均为 。某同学进行了如下实验:
。某同学进行了如下实验:
(4)原溶液中一定不存在的离子是
(5)沉淀C的成分是
(6)写出加入过量
 时产生气体的离子方程式
时产生气体的离子方程式
您最近一年使用:0次

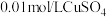 溶液、
溶液、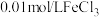 溶液
溶液 溶液、
溶液、 溶液
溶液 溶液
溶液


