1 . 某化学兴趣小组探究SO2与Ca( NO3)2溶液的反应。
I.实验一:用如下装置制备SO2,然后将SO2通入Ca(NO3)2溶液中,有白色沉淀M产生。

(1)固体a是_______ (写名称) 。
(2)装置D的作用是_______ 。
(3)配制1mol·L-1Ca(NO3)2溶液时所用蒸馏水必须除去溶解的氧气,除氧方法是_______ 。
II.根据所学知识推测:白色沉淀M可能为CaSO3或CaSO4也可能是二者混合物。(查阅资料得知:CaSO4微溶于水;CaSO3难溶于水。)
实验二:探究白色沉淀M的成分。反应后将装置C中物质转移到烧杯中静置,利用倾析法倾倒出上层清液,抽滤,洗涤得到沉淀M。取沉淀M少许于试管中,加入过量的稀HCI,充分反应,发现沉淀部分溶解。由此可知白色沉淀M含有CaSO3。
(4)适合利用倾析法将下列物质与水分离的是_______
(5)取加入过量稀HCl静置后的上层溶液于试管中,加入一种试剂,可进一步证实沉淀M中含有CaSO3,则所加试剂及现象是_______ 。
实验三:探究SO 的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。
的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。
(6)有氧CaCl2溶液中通入SO2发生反应的离子方程式为_______ 。
(7)从上述实验现象可得出对SO2氧化起主要作用的是_______ (填O2或NO ),其理由是
),其理由是_______ 。
I.实验一:用如下装置制备SO2,然后将SO2通入Ca(NO3)2溶液中,有白色沉淀M产生。

(1)固体a是
(2)装置D的作用是
(3)配制1mol·L-1Ca(NO3)2溶液时所用蒸馏水必须除去溶解的氧气,除氧方法是
II.根据所学知识推测:白色沉淀M可能为CaSO3或CaSO4也可能是二者混合物。(查阅资料得知:CaSO4微溶于水;CaSO3难溶于水。)
实验二:探究白色沉淀M的成分。反应后将装置C中物质转移到烧杯中静置,利用倾析法倾倒出上层清液,抽滤,洗涤得到沉淀M。取沉淀M少许于试管中,加入过量的稀HCI,充分反应,发现沉淀部分溶解。由此可知白色沉淀M含有CaSO3。
(4)适合利用倾析法将下列物质与水分离的是_______
| A.易沉淀固体 | B.胶状物质 | C.大颗粒沉淀 | D.絮状物质 |
实验三:探究SO
 的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。
的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。(6)有氧CaCl2溶液中通入SO2发生反应的离子方程式为
(7)从上述实验现象可得出对SO2氧化起主要作用的是
 ),其理由是
),其理由是
您最近一年使用:0次
2022-02-17更新
|
614次组卷
|
2卷引用:吉林省长春市博硕学校(原北师大长春附属学校)2021-2022学年高二下学期期末考试化学试题
14-15高一上·安徽淮北·期末
名校
解题方法
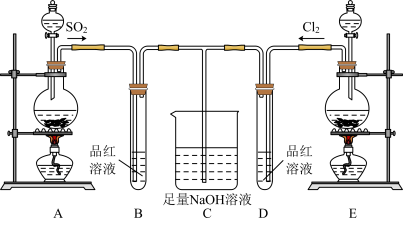
2 . 某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下实验装置:__ 。
(2)实验室可用装置E通过MnO2和浓盐酸反应制备Cl2,若有6molHCl参加反应,则转移电子的总数为___ 。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象分别是:B__ ,D___ 。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别是:B__ ,D__ 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会更强。他们将制得的SO2和Cl2按物质的量之比为1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析产生该现象的原因:__ (用化学方程式表示)。
(2)实验室可用装置E通过MnO2和浓盐酸反应制备Cl2,若有6molHCl参加反应,则转移电子的总数为
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象分别是:B
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会更强。他们将制得的SO2和Cl2按物质的量之比为1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析产生该现象的原因:
您最近一年使用:0次
2020-09-16更新
|
154次组卷
|
8卷引用:吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期期末考试化学试题
吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期期末考试化学试题(已下线)2013-2014学年安徽省濉溪县高一上学期期末考试化学试卷(已下线)2013-2014学年河南省平顶山市高一第一学期期末调研考试化学试卷2014-2015甘肃省白银市会宁县五中高一上学期期末化学试卷【全国百强校】西藏自治区拉萨中学2017-2018学年高一下学期期中考试化学试题鲁科版(2019)高一必修第一册第三章易错疑难集训(二)高一必修第一册(苏教2019版)专题4 第一单元 含硫化合物的性质 易错疑难集训陕西省西安市选课分科摸底考2023-2024学年高一下学期4月月考化学试题
解题方法
3 . 钠和氯是我们熟悉的典型金属元素与非金属元素,研究它们的性质对于生产、生活、科研具有重要意义。
I.某化学兴趣小组为了探究“干燥的CO2不能与Na2O2反应”而“潮湿的CO2能与Na2O2反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。
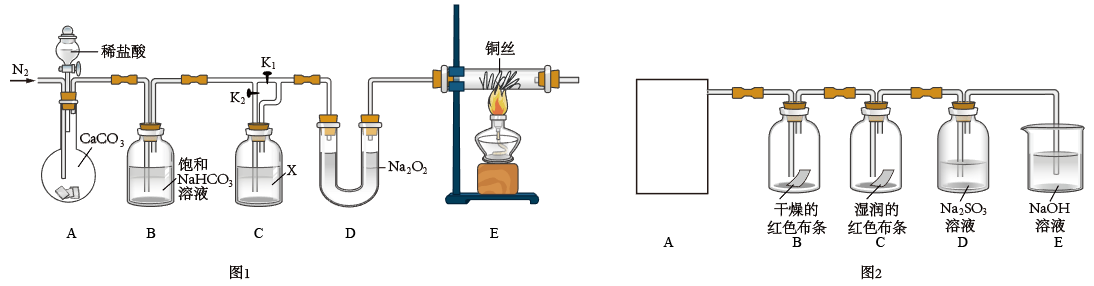
回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是___ 。
(2)饱和NaHCO3溶液的作用是___ ,试剂X是___ 。
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是___ 。
(4)写出D中CO2与Na2O2反应的化学方程式___ 。
II.为探究氯气的性质,某同学利用此原理制氯气并设计了如图2所示的实验装置(A为氯气制取装置,未画出)。
(1)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是___ 。实验过程中该同学发现装置B中的布条也褪色,说明该装置存在明显的缺陷,改进的方法是___ 。
(2)E中NaOH溶液吸收氯气时发生反应的化学方程式是___ 。
(3)D中氯气可将SO 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是___ (提示:SO 遇盐酸生成SO2气体。写出操作试剂和现象)
遇盐酸生成SO2气体。写出操作试剂和现象)
(4)“84消毒液”是生活中常用的消毒剂,可与硫酸反应制取氯气,反应原理为NaClO+NaCl+H2SO4 Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是
Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是___ mol。
I.某化学兴趣小组为了探究“干燥的CO2不能与Na2O2反应”而“潮湿的CO2能与Na2O2反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。

回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是
(2)饱和NaHCO3溶液的作用是
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是
(4)写出D中CO2与Na2O2反应的化学方程式
II.为探究氯气的性质,某同学利用此原理制氯气并设计了如图2所示的实验装置(A为氯气制取装置,未画出)。
(1)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是
(2)E中NaOH溶液吸收氯气时发生反应的化学方程式是
(3)D中氯气可将SO
 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是 遇盐酸生成SO2气体。写出操作试剂和现象)
遇盐酸生成SO2气体。写出操作试剂和现象)(4)“84消毒液”是生活中常用的消毒剂,可与硫酸反应制取氯气,反应原理为NaClO+NaCl+H2SO4
 Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是
Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是
您最近一年使用:0次
解题方法
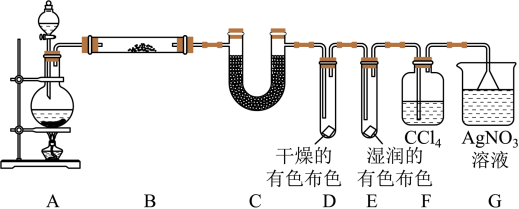
4 . 兴趣小组探究实验室中制备Cl2的过程,为证明过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置,按要求回答问题:
(1)若用浓盐酸与足量的MnO2反应制Cl2。MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O。
①用双线桥表示该反应的电子转移___ 。
②___ 作氧化剂 ,___ 作还原产物。
(2)①装置B中盛放的试剂名称为___ ,作用是___ 。
②装置D和E中出现的不同现象说明的问题是___ 。
③写出装置G中发生反应的离子方程式:___ 。

(1)若用浓盐酸与足量的MnO2反应制Cl2。MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O。
①用双线桥表示该反应的电子转移
②
(2)①装置B中盛放的试剂名称为
②装置D和E中出现的不同现象说明的问题是
③写出装置G中发生反应的离子方程式:
您最近一年使用:0次
2020-01-09更新
|
135次组卷
|
3卷引用:吉林省长春市榆树市2019-2020学年高一上学期期末考试化学试题
5 . 化学是一门以实验为基础的学科,试回答以下问题:
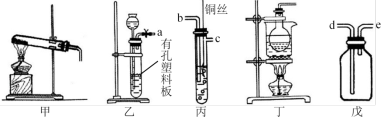
(1)实验室中用装置甲和戊制取并收集少量氨气,甲中发生反应的化学方程式为:____ 。 戊装置收集氨气应从收集装置的_____ (填字母序号)导管进气。
(2)选用装置乙、丙、戊制备、收集一氧化氮气体,乙中塑料板上若放置石灰石,戊中盛 满稀 NaOH 溶液,仪器正确的连接顺序为_____ (用接口字母表示);戊中盛放稀 NaOH 溶液 的原因是_____ 。
(3)用内置有螺旋状铜丝的胶头滴管小心吸取一滴管浓硝酸后迅速插入细口瓶中(如图), 滴管与瓶口接触处垫一小块滤纸使滴管与瓶口留少量空隙,依次观察到如下现象:
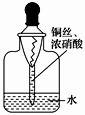
a.滴管内产生红棕色气体,液面下降; b.滴管内的液面上升,气体变成无色; c.滴管内的液面再次下降。
①现象 a 中产生的红棕色气体时发生的反应为:_____ 。
②产生现象 b 的原因是_____ 。
③产生现象 c 的原因是(用方程式表示):_____ 。

(1)实验室中用装置甲和戊制取并收集少量氨气,甲中发生反应的化学方程式为:
(2)选用装置乙、丙、戊制备、收集一氧化氮气体,乙中塑料板上若放置石灰石,戊中盛 满稀 NaOH 溶液,仪器正确的连接顺序为
(3)用内置有螺旋状铜丝的胶头滴管小心吸取一滴管浓硝酸后迅速插入细口瓶中(如图), 滴管与瓶口接触处垫一小块滤纸使滴管与瓶口留少量空隙,依次观察到如下现象:

a.滴管内产生红棕色气体,液面下降; b.滴管内的液面上升,气体变成无色; c.滴管内的液面再次下降。
①现象 a 中产生的红棕色气体时发生的反应为:
②产生现象 b 的原因是
③产生现象 c 的原因是(用方程式表示):
您最近一年使用:0次
2019-01-11更新
|
180次组卷
|
2卷引用:【校级联考】吉林省榆树一中五校联考2018-2019学年高一上学期期末联考化学试题
6 . 某课外活动小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”.
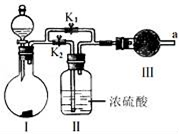
(1)过氧化钠与水反应的化学方程式是__ .
(2)装置I是制备纯净的__ (填化学式).则装置I中最适宜的试剂组合是__ (填字母).
a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹K2,关闭K1,观察到预期现象后,打开K1,再关闭K2.
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃.
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是__ ;
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是__ .

(1)过氧化钠与水反应的化学方程式是
(2)装置I是制备纯净的
a.稀盐酸 b.稀硫酸 c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹K2,关闭K1,观察到预期现象后,打开K1,再关闭K2.
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃.
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是
您最近一年使用:0次
2018-03-19更新
|
291次组卷
|
3卷引用:吉林省东丰县第三中学2017-2018学年高一上学期期末考试化学试题
名校
解题方法
7 . 某学习小组通过下列装置探究 与
与 能否反应产生
能否反应产生 。
。
已知:①溴水为橙色
②三氯化铁常温下为固体,熔点为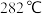 ,沸点为
,沸点为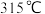 ,在
,在 以上易升华;易溶于水。
以上易升华;易溶于水。
(1)现象ⅰ中的白雾成分是___________ (化学式)。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热 ,产生白雾和黄色气体。
,产生白雾和黄色气体。
b.用 溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
通过该实验说明现象ⅱ中黄色气体含有___________ (化学式)。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是___________ ,实验证实此推测成立。
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过实验进一步验证与空气无关。
(4)为进一步确认黄色气体是否含有 ,小组提出两种方案,并证实了
,小组提出两种方案,并证实了 的存在。
的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中 淀粉溶液替换为
淀粉溶液替换为 溶液,并检验反应后是否存在
溶液,并检验反应后是否存在 。现象如下:
。现象如下:
①方案1的C中盛放的试剂是___________ 。
②方案2中检验 的原因是
的原因是___________ 。
③综合方案1、2的现象,说明选择 溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为
溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为___________ 。
 与
与 能否反应产生
能否反应产生 。
。已知:①溴水为橙色
②三氯化铁常温下为固体,熔点为
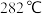 ,沸点为
,沸点为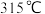 ,在
,在 以上易升华;易溶于水。
以上易升华;易溶于水。| 操作 | 现象 | 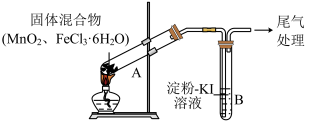 |
| 点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(1)现象ⅰ中的白雾成分是
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热
 ,产生白雾和黄色气体。
,产生白雾和黄色气体。b.用
 溶液检验现象ⅱ和a中的黄色气体,溶液均变红。
溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过实验进一步验证与空气无关。
(4)为进一步确认黄色气体是否含有
 ,小组提出两种方案,并证实了
,小组提出两种方案,并证实了 的存在。
的存在。方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中
 淀粉溶液替换为
淀粉溶液替换为 溶液,并检验反应后是否存在
溶液,并检验反应后是否存在 。现象如下:
。现象如下:| 方案1 | B中溶液变为蓝色 |
| 方案2 | B中溶液呈橙色;未检出 |
②方案2中检验
 的原因是
的原因是③综合方案1、2的现象,说明选择
 溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为
溶液是由氧化剂氧化性的强弱决定,其氧化剂的氧化性由强到弱的顺序为
您最近一年使用:0次
2024-02-27更新
|
131次组卷
|
3卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
解题方法
8 . 某同学为了验证硫铁矿(主要成分为FeS2。含有少量的碳)焙烧产物(产生的气体是SO2,CO2),设计如下装置进行实验:
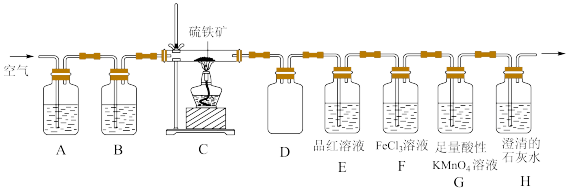
回答下列问题:
(1)装置A、B中的试剂分别是_______ 、_______ 。
(2)装置D的作用是_______ 。
(3)验证焙烧后气体产物的实验现象分别为_______ 、_______ ;若F中颜色发生改变,写出产生颜色变化反应的离子方程式:_______ 。取F中反应后的溶液于洁净的试管中。滴加少量KSCN溶液,溶液不变红,说明溶液中_______ (填“含有”或“不含有”)Fe3+;再继续滴加少量氯水,溶液也不变红。产生这种现象的原因可能是_______ 。
(4)G中盛放足量酸性KMnO4溶液的目的是_______ (用离子方程式表示)。
(5)反应完成后经检验,C中剩余固体物质只有Fe2O3,写出FeS2焙烧反应的化学方程式:_______ 。

回答下列问题:
(1)装置A、B中的试剂分别是
(2)装置D的作用是
(3)验证焙烧后气体产物的实验现象分别为
(4)G中盛放足量酸性KMnO4溶液的目的是
(5)反应完成后经检验,C中剩余固体物质只有Fe2O3,写出FeS2焙烧反应的化学方程式:
您最近一年使用:0次
解题方法
9 . 某同学用如图装置(夹持装置略)探究铜丝与过量浓硫酸的反应。
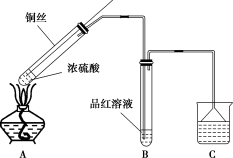
回答下列问题:
(1)铜与浓硫酸反应的化学方程式为___ 。
(2)B中观察到的现象为___ 。
(3)C中应加入的试剂为___ ,倒置漏斗的作用是___ 。
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,优点是___ 。

回答下列问题:
(1)铜与浓硫酸反应的化学方程式为
(2)B中观察到的现象为
(3)C中应加入的试剂为
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,优点是
您最近一年使用:0次
2021-05-26更新
|
268次组卷
|
4卷引用:吉林省延边州汪清县第六中学2021-2022学年高一下学期期末考试化学试题
10 . 某兴趣小组的同学设计实验制备并探究SO2的性质。回答下列问题:
(1)实验室用废铜屑制备SO2的化学方程式为______ 。
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有______ 性。
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为______ 。
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为______ 。(Cr2O72-被还原为Cr3+)
(5)常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=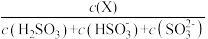 ]随pH的变化如图所示:
]随pH的变化如图所示:
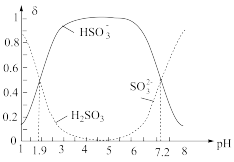
H2SO3的lgKa1=______ ;反应HSO3-+OH- SO32-+H2O的lgK=
SO32-+H2O的lgK=______ ;用0.100mol•L-1NaOH溶液滴入0.100mol•L-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为______ 。
(1)实验室用废铜屑制备SO2的化学方程式为
(2)将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有
(3)将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为
(4)将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为
(5)常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=
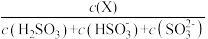 ]随pH的变化如图所示:
]随pH的变化如图所示:
H2SO3的lgKa1=
 SO32-+H2O的lgK=
SO32-+H2O的lgK=
您最近一年使用:0次



