名校
解题方法
1 . I.某小组在实验室模拟工业提溴的流程(见下图),设计下图的装置进行实验。

回答下列问题:
(1)实验中先向A中通入Cl2,反应的离子方程式是_______ 。再向A中鼓入热空气,观察到的现象是_______ 。
(2)A中产生的气体被B中的 水溶液吸收,反应的化学方程式为
水溶液吸收,反应的化学方程式为_______ 。从氧化还原角度分析, 在该反应中体现了
在该反应中体现了_______ 性,下列试剂中能代替 水溶液的是
水溶液的是_______ (选填编号)。
a. 溶液 b. NaCl溶液 c.
溶液 b. NaCl溶液 c. 溶液
溶液
(3)为将B中的溴元素转化为液溴,向反应后B装置的溶液中通入氯气,充分反应,再加入苯,后续的实验操作步骤包含_______ (选填编号)。
a.过滤 b.萃取、分液 c.结晶 d. 蒸馏
(4)将1m3海水浓缩后最终得到21gBr2,若提取率为70%,则海水中溴元素的浓度为_______ g/L。
II.为了从海带中提取碘,该小组设计如下实验:
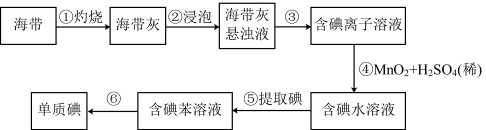
(5)步骤④的作用是_______ (选填编号)。
a. 浓缩 b. 氧化 c. 提取
(6)步骤⑤中选用苯提取碘的原因是_______ 。

回答下列问题:
(1)实验中先向A中通入Cl2,反应的离子方程式是
(2)A中产生的气体被B中的
 水溶液吸收,反应的化学方程式为
水溶液吸收,反应的化学方程式为 在该反应中体现了
在该反应中体现了 水溶液的是
水溶液的是a.
 溶液 b. NaCl溶液 c.
溶液 b. NaCl溶液 c. 溶液
溶液(3)为将B中的溴元素转化为液溴,向反应后B装置的溶液中通入氯气,充分反应,再加入苯,后续的实验操作步骤包含
a.过滤 b.萃取、分液 c.结晶 d. 蒸馏
(4)将1m3海水浓缩后最终得到21gBr2,若提取率为70%,则海水中溴元素的浓度为
II.为了从海带中提取碘,该小组设计如下实验:

(5)步骤④的作用是
a. 浓缩 b. 氧化 c. 提取
(6)步骤⑤中选用苯提取碘的原因是
您最近一年使用:0次
2023-01-13更新
|
332次组卷
|
2卷引用:上海市华东师范大学第三附属中学 2022-2023 学年高一上学期期末考试化学试题
名校
解题方法
2 . 海水的综合利用
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是___________ 。
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是___________ 。
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是___________ 。
A.贝壳在海水提取镁的生产流程中,主要经历了 的过程
的过程
B.工业生产中利用电解熔融 制备镁
制备镁
C.在从海水中提取镁的工业流程中, 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁
(4)下图是海水提溴的工艺流程,下列说法错误的是___________ 。
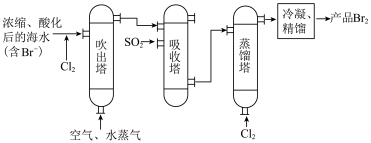
A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为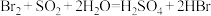
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式___________ 。
②检验阳极产物时可选用___________ ,向阴极附近溶液滴加紫色石蕊试液呈___________ 色。
③实验测得产生的 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为___________  。
。
(6)实验室模拟工业从海藻中提碘的流程如图:
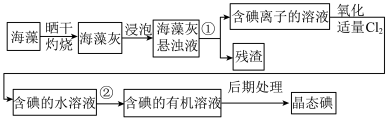
①选择合适实验操作名称填入流程图中:①___________ ,②___________ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
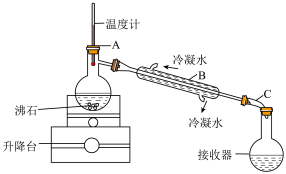
②装置中间部分是“冷凝管”,该装置中有一处明显的错误是___________ 。
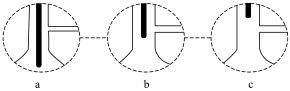
③装置A中,温度计所处的正确位置是___________ 。(选填编号)
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是
A.贝壳在海水提取镁的生产流程中,主要经历了
 的过程
的过程B.工业生产中利用电解熔融
 制备镁
制备镁C.在从海水中提取镁的工业流程中,
 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用
 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁(4)下图是海水提溴的工艺流程,下列说法错误的是

A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为
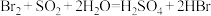
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式
②检验阳极产物时可选用
③实验测得产生的
 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为 。
。(6)实验室模拟工业从海藻中提碘的流程如图:

①选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

②装置中间部分是“冷凝管”,该装置中有一处明显的错误是
③装置A中,温度计所处的正确位置是

您最近一年使用:0次
3 . 海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
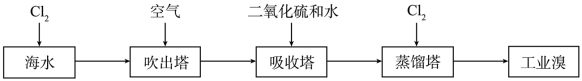
(1)溴元素在元素周期表中的位置为_______ 。
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_______ 。
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______ 。
Ⅱ.海水提镁
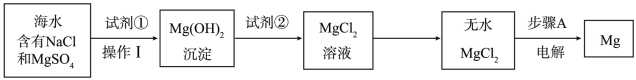
(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(5)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______ 。
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(5)步骤A的化学方程式为
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是
您最近一年使用:0次
2022-07-10更新
|
351次组卷
|
2卷引用:湖北省新高考联考协作体2021-2022学年高一下学期期末考试化学试题
4 . 溴、碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→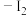 的
的 溶液
溶液
(1)上述实验流程中灼烧用到的仪器是_______ (从下列图中选择,写出名称,下同),萃取分液在_______ 中进行。

(2)“氧化”时加入 和
和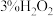 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ 。
(3)检验氧化后的溶液中存在碘单质,可选用的试剂是_______ (填名称)溶液。
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。
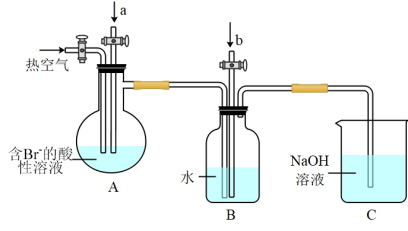
(4)A装置中通入a气体通常为_______ ,发生反应的离子方程式为_______ 。
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是_______ 。
(6)B装置的作用是收集并还原溴,则气体b为_______ 。
(7)C装置的作用是_______ 。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→
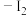 的
的 溶液
溶液(1)上述实验流程中灼烧用到的仪器是

(2)“氧化”时加入
 和
和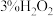 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)检验氧化后的溶液中存在碘单质,可选用的试剂是
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。

(4)A装置中通入a气体通常为
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是
(6)B装置的作用是收集并还原溴,则气体b为
(7)C装置的作用是
您最近一年使用:0次
5 . 围绕海水的综合利用,化学课外兴趣小组进行下列实验:
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
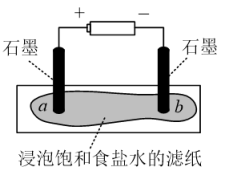
①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈___________ 色。
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
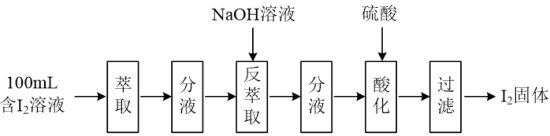
①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和___________ 。
②“反萃取”操作时溶液中有I-、IO 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为___________ 。
(3)模拟浓海水提取镁实验流程如下图:
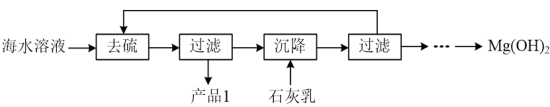
说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
①产品1的化学式为___________ 。
②沉降阶段主要的化学反应方程式为___________ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是
(2)模拟反萃取法提取碘实验流程如下图:

①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和
②“反萃取”操作时溶液中有I-、IO
 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为(3)模拟浓海水提取镁实验流程如下图:

说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②沉降阶段主要的化学反应方程式为
您最近一年使用:0次
6 . 碘是人体的必需微量元素之一,海带提取碘的部分实验流程如下
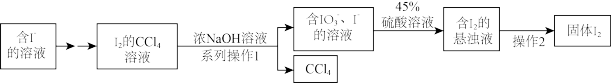
(1)系列操作1中需用到的玻璃仪器有烧杯、玻璃棒和___________ ,操作2的实验方法是___________ 。
(2)氧化 通常用
通常用 作为氧化剂,写出反应的离子方程式
作为氧化剂,写出反应的离子方程式___________ 。
(3)某实验小组研究 的氧化,将
的氧化,将 通入KI溶液中,出现黄色,查阅资料,发生了以下反应:
通入KI溶液中,出现黄色,查阅资料,发生了以下反应: 。为了探究该反应的影响因素,设计以下实验:
。为了探究该反应的影响因素,设计以下实验:
①用水吸收 制取
制取 水溶液,吸收装置最佳的是
水溶液,吸收装置最佳的是___________ 。

②实验1和2探究___________ 对实验的影响,实验2和3探究___________ 对实验的影响,实验2加蒸馏水的体积为___________ (用表中字母或字母的表达式作答)。
③添加药品的合理顺序为: 水溶液、
水溶液、___________ 、稀盐酸、___________ (填“KI溶液”或“蒸馏水”)。
④往三组实验中滴加淀粉溶液,均没有出现蓝色,你认为原因是___________ (用化学方程式解释)。检验该反应发生的实验试剂是___________ 。
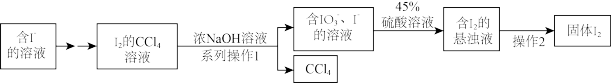
(1)系列操作1中需用到的玻璃仪器有烧杯、玻璃棒和
(2)氧化
 通常用
通常用 作为氧化剂,写出反应的离子方程式
作为氧化剂,写出反应的离子方程式(3)某实验小组研究
 的氧化,将
的氧化,将 通入KI溶液中,出现黄色,查阅资料,发生了以下反应:
通入KI溶液中,出现黄色,查阅资料,发生了以下反应: 。为了探究该反应的影响因素,设计以下实验:
。为了探究该反应的影响因素,设计以下实验:| 实验序号 |  水溶液(mL) 水溶液(mL) |  溶液(mL) 溶液(mL) | 稀盐酸(mL) | 蒸馏水(mL) | 实验现象 |
| 1 | a(过量) | b | 0 | d | 溶液逐渐变浅黄色 |
| 2 | a(过量) | b | c | ___________ | 溶液变黄,有浑浊 |
| 3 | a(过量) | 2b | c | 0 | 溶液变黄,比实验2出现浑浊更快 |
 制取
制取 水溶液,吸收装置最佳的是
水溶液,吸收装置最佳的是
②实验1和2探究
③添加药品的合理顺序为:
 水溶液、
水溶液、④往三组实验中滴加淀粉溶液,均没有出现蓝色,你认为原因是
您最近一年使用:0次
2021-08-04更新
|
586次组卷
|
3卷引用:广东省2022届高三8月阶段性质量检测化学试题
名校
解题方法
7 . 海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
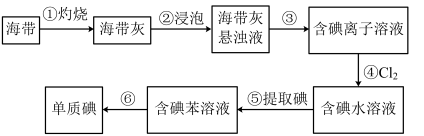
请填写下列空白:
(1)步骤③⑥的实验操作名称分别是_______ 和_______ 。步骤④反应的离子方程式是_______ 。除了氯水,从绿色化学角度考虑,最合适的试剂为_______ 。
A.浓硫酸 B.浓硝酸 C.KMnO4溶液 D.H2O2
(2)步骤⑤中,某学生选择用苯来提取碘的理由有:碘与苯不反应;苯与水不互溶:还有_______ 。从含碘水溶液中获得含碘苯溶液,该操作名称为_______ ,用到最主要仪器为_______ ,不能用酒精代替苯的理由是:_______
(3)向一容积为15 mL的试管中先加入3 mL碘水,再加入1 mL苯,充分振荡、静置后,下列图示现象正确的是_______

关于卤素氯、溴、碘的叙述,错误的是_______
a.单质易溶于有机溶剂中 b. X-的颜色逐渐加深
c.单质氧化性性逐渐减弱 d.X-的还原性逐渐增强

请填写下列空白:
(1)步骤③⑥的实验操作名称分别是
A.浓硫酸 B.浓硝酸 C.KMnO4溶液 D.H2O2
(2)步骤⑤中,某学生选择用苯来提取碘的理由有:碘与苯不反应;苯与水不互溶:还有
(3)向一容积为15 mL的试管中先加入3 mL碘水,再加入1 mL苯,充分振荡、静置后,下列图示现象正确的是

关于卤素氯、溴、碘的叙述,错误的是
a.单质易溶于有机溶剂中 b. X-的颜色逐渐加深
c.单质氧化性性逐渐减弱 d.X-的还原性逐渐增强
您最近一年使用:0次
名校
8 . 碘元素是我们人体不可或缺的微量元素,某化学兴趣小组在实验室模拟工业提碘,流程图如下,请回答下列问题:
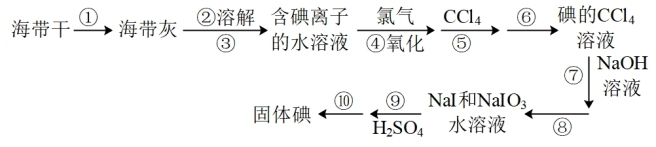
(1)请填写流程图中的操作步骤名称:③___________ ; ⑤___________ ;⑧___________ ;⑩___________ 。
(2)请填写该操作所需要的重要仪器名称:①___________ ;⑥___________ 。
(3)步骤①的目的是:___________ 。步骤④⑤⑥⑦⑧的目的是:___________ 。
(4)检验步骤③后的水溶液中是否含有碘离子的方法是___________ 。
(5)请写出步骤⑦发生的离子方程式:___________ 。
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)

(1)请填写流程图中的操作步骤名称:③
(2)请填写该操作所需要的重要仪器名称:①
(3)步骤①的目的是:
(4)检验步骤③后的水溶液中是否含有碘离子的方法是
(5)请写出步骤⑦发生的离子方程式:
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)
| A.加入干燥剂,加热升华 | B.蒸馏 |
| C.重结晶 | D.萃取、分液 |
您最近一年使用:0次
9 . 实验室模拟工业从海藻中提取碘的流程如图:
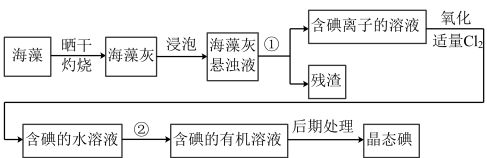
(1)选择合适实验操作名称填入流程图中:①_____ ,②_____ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
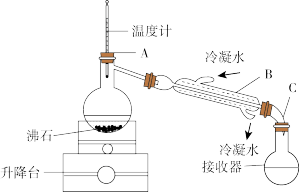
(2)装置中间部分是“冷凝管”,该装置中有一处明显的错误是_____ 。
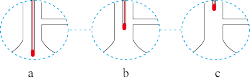
(3)装置A中,温度计所处的正确位置是_____ 。(选填编号)

(1)选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

(2)装置中间部分是“冷凝管”,该装置中有一处明显的错误是
(3)装置A中,温度计所处的正确位置是

您最近一年使用:0次
解题方法
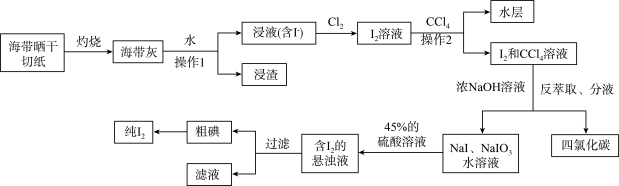
10 . 某化学实验小组从市场购买海带并设计提碘的流程如图所示:
请回答下列问题:
(1)操作2包括以下步骤:a.振荡萃取b.分液c.静置分层d.加碘溶液和CCl4e.检漏。
①上述步骤的正确先后顺序是______ (填编号)。
②完成步骤a时要及时放气,放气时分液漏斗下端应_____ (填“向上倾斜”或“向下倾斜”),放气的目的是______ 。
③步骤b的具体操作是______ ,再将分液漏斗下面的活塞拧开,使下层液体沿烧杯内壁流下,当下层液体刚好放完时关闭活塞,______ 。
(2)浓NaOH溶液与I2反应的化学方程式是_____ 。
(3)加入45%硫酸溶液的作用是______ (用离子方程式表示)。
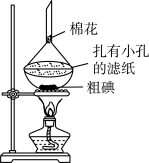
(4)利用如图所示装置进行粗碘提纯。简述纯化I2的原理:_____ 。棉花的作用是______ 。

请回答下列问题:
(1)操作2包括以下步骤:a.振荡萃取b.分液c.静置分层d.加碘溶液和CCl4e.检漏。
①上述步骤的正确先后顺序是
②完成步骤a时要及时放气,放气时分液漏斗下端应
③步骤b的具体操作是
(2)浓NaOH溶液与I2反应的化学方程式是
(3)加入45%硫酸溶液的作用是
(4)利用如图所示装置进行粗碘提纯。简述纯化I2的原理:

您最近一年使用:0次



