21. 锰及其化合物在现代工业和国防建设中具有十分重要的地位。金属锰的提炼方式主要有热还原法和电解法两种,热还原法得到的锰纯度在95-98%之间,电解法得到的锰(简称电解锰),其纯度可达99.7~99.9%以上。
(1)锰锌铁氧体是当前广泛使用的一种隐形涂料,其化学组成为Mn
xZn
1-xFe
2O
4(铁为+3价),其中当锰锌铁氧体中
n(Zn):
n(Fe)=2:5时,它对雷达波的吸收能力最强。
① 锰锌铁氧体中锰元素的化合价为
_______。
② 当雷达波吸收能力最强时,该物质的化学式为
________(改写成氧化物的形式)。
(2)写出以MnO
2和Al粉为原料,利用热还原法制备Mn的化学方程式:
________。
(3)工业上以菱锰矿(主要成分是MnCO
3,含有Fe
2+、Co
2+、Ni
2+等杂质金属离子)为原料制备电解锰的流程图如下所示。
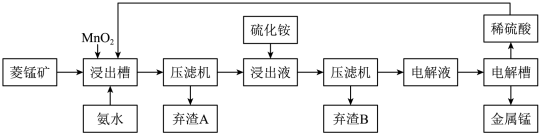
生成氢氧化物的pH如下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀时pH | 7.5 | 2.l | 7.7 | 7.6 | 8.3 |
| 完全沉淀时pH | 9.7 | 3.7 | 8.5 | 8.2 | 9.8 |
① 浸出槽中发生多个反应:如主要成分与硫酸的反应、MnO
2与Fe
2+间的氧化还原反应等,写出这两个反应的离子方程式:
___________________、
____________________。
② 加入氨水的目的是为除去杂质,根据流程图及表中数据,pH 应调控在
_____范围内。常温下,
Ksp[Fe(OH)
3]=4.0×10
-38,当pH=4时溶液中
c(Fe
3+)=
__________。
③ 加入硫化铵是为除去剩余的Ni
2+,反应的离子方程式为
____________________。
④ 写出电解硫酸锰溶液制取金属锰的化学方程式:
________________________。