20. 氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式
_____。
(2)氨是制备氮肥、硝酸等的重要原料
①已知:N
2(g)+3H
2(g)

2NH
3(g)
△H=-92.4kJ/mol
N
2(g)+O
2(g)

2NO(g)
△H=+180 kJ/mol
2H
2(g)+O
2(g)

2H
2O(1)
△H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式
_____。
②某电解法制氨的装置如图所示,电解质只允许质子通过,试写出阴极的电极反应式
_____。
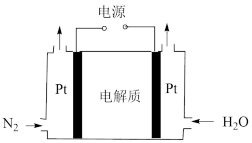
(3)反应:2NO(g)+O
2(g)

2NO
2(g)
△H<0 是制备硝酸过程中的一个反应。
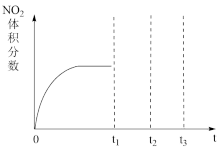
①将NO和O
2按物质的量之比为 2:1 置于恒温恒容密闭容器中进行上述反 应,得到NO
2 体积分数与时间的关系如图所示。保持其它条件不变,t
1 时再向 容器中充入适量物质的量之比为2:1的NO和O
2的混合气体,t
2 时再次达到平 衡,请画出 t
l-t
3 时间范围内 NO
2 体积分数随时间的变化曲线:
_________。
②在研究此反应速率与温度的关系时发现,NO 转化成 NO
2 的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I.2NO(g)

N
2O
2(g)
△H<0
II.N
2O
2(g)+O
2(g)

2NO
2(g)
△H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO 转化成 NO
2 的速率减慢的可能原因
________。
(4)已知常温下,K
a(CH
3COOH)=K
b(NH
3·H
2O)=l.8×l0
-5。则常温下 0.lmol/L 的 CH
3COONH
4 溶液中,c(CH
3COO
-):c(NH
3·H
2O)=
_____。