9. 高铁酸钾在饮用水源和废水处理过程中,不仅能去除污染物和致癌化学污染物,而且不产生任何诱变致癌的产物,具有高度的安全性;其可溶于水,微溶于浓 KOH 溶液,且在强碱性溶液中比 较稳定。实验室用次氯酸盐氧化法制备高铁酸钾(K
2FeO
4)的流程如图所示:

流程图中的饱和次氯酸钾溶液的制备装置如图所示:
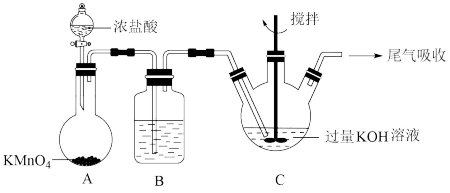
(1)A 为氯气发生装置。A 中反应的离子方程式是
___________;装置 B 内的试剂及作用是
____________;
(2)装置 C 反应温度控制在 0~5℃进行,在不改变 KOH 溶液浓度前提下,实验中可采取措施是
________。
(3)流程图中在加入 KOH 固体的时候会产生大量的白色沉淀
_____(填化学式)。
(4)在搅拌下,将 Fe(NO
3)
3饱和溶液缓慢滴加到 KClO 饱和溶液中即可制取 K
2FeO
4,写出该反应的离子方程式
__________;反应过程中温度控制在 10~15℃,温度过低或过高对反应的影响是
_____________。
(5)过滤除杂时不用普通漏斗和滤纸而采用砂芯漏斗(如图)的原因是
_____________。
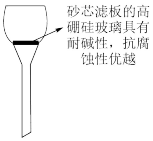
(6)在提纯高铁酸钾时采用重结晶、洗涤、干燥的方法,洗涤剂可以选用
_____。
A.H
2O B.浓 KOH 溶液 C.Fe(NO
3)
3溶液
D.异丙醇
(7)若提纯得到 a gK
2FeO
4(M=198g/mol),上述流程中有 5%的 Fe 损失,则需要提供 Fe(NO
3)
3(M=242g/mol)的质量为
_____g(用含 a 的计算式表示)。