16. (I)某探究小组用HNO
3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO
3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO
3的用量为25.00 mL,大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
| 实验编号 | 温度(℃) | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响;
(Ⅱ)实验①和③探究温度对反应速率的影响;
(Ⅲ)实验①和④探究e_______对反应速率的影响 |
| ② | 25 | 粗颗粒 | a______ |
| ③ | b_______ | 粗颗粒 | 2.00 |
| ④ | c________ | 细颗粒 | d______ |
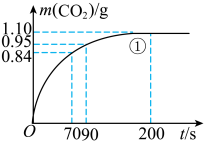
(2)实验①中CO
2质量随时间变化的关系见下图。计算实验①中70 s~90 s范围内用HNO
3表示的平均反应速率
________(忽略溶液体积变化,不需要写出计算过程)。在0~70、70~90、90~200各相同的时间段里,反应速率最大的时间段是
________。
(II)某小组利用H
2C
2O
4溶液和硫酸酸化的KMnO
4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO
4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:2KMnO
4+5H
2C
2O
4+3H
2SO
4=K
2SO
4+2MnSO
4+10CO
2↑+8H
2O
| 实验编号 | 0.1 mol·L-1酸性KMnO4溶液的体积/mL | 0.6mol·L-1H2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
| ① | 10 | V1 | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 | V2 | 50 | |
(3)表中V
1=
_______mL,V
2=
_______mL。
(4)探究温度对化学反应速率影响的实验编号是
________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是
________。
(5)实验①测得KMnO
4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H
2C
2O
4)=
________mol·L
-1·min
-1。