20. 近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
I. Deacon发明的直接氧化法为:4HCl(g)+O
2(g)=2Cl
2(g)+2H
2O(g)。如图为刚性容器中,进料浓度比c(HCl)∶c(O
2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:

(1)可知反应平衡常数K(300 ℃)
_____K(400 ℃)(填“大于”或“小于”)。设HCl初始浓度为c
0,根据进料浓度比c(HCl)∶c(O
2)=1∶1的数据计算K(400 ℃)=
_____(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O
2)过低、过高的不利影响分别是
_____________、
____________。
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
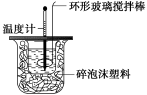
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
温度
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ |
H2SO4 | NaOH | 平均值 |
1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
2 | 27.0 | 27.4 | 27.2 | 31.2 |
3 | 25.9 | 25.9 | 25.9 | 29.8 |
4 | 26.4 | 26.2 | 26.3 | 30.4 |
②近似认为0.50 mol·L
-1 NaOH溶液和0.50 mol·L
-1硫酸溶液的密度都是1 g·cm
-3,中和后生成溶液的比热容c=4.18 J·g
-1·℃
-1。则中和热ΔH=
_______________________(取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol
-1有偏差,产生偏差的原因可能是(填字母)
____________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H
2SO
4溶液的温度