河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
河南
高三
阶段练习
2021-10-14
425次
整体难度:
适中
考查范围:
化学与STSE、初中衔接知识点、常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、化学反应原理
河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
河南
高三
阶段练习
2021-10-14
425次
整体难度:
适中
考查范围:
化学与STSE、初中衔接知识点、常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、化学反应原理
一、单选题 添加题型下试题
1. 《天工开物》中记载:“石胆-名胆矾者,亦出晋、隰等州,乃山石穴中自结成者,故绿色带宝光。烧铁器淬于胆矾水中,即成铜色也。”《本草纲目》记载:“灵砂亦名二气砂,乃水银、硫磺合炼而成”古文中“石胆”和“灵砂”的主要成分分别是
| A.CuSO4·5H2O、HgS | B.CuSO4、S |
| C.KAl(SO4)2·12H2O、FeO | D.CuSO4·2H2O、FeS |
【知识点】 化学科学对人类文明发展的意义解读 化学与社会发展
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
2. 邮票记载了我国发展历程,形象地呈现了人类与化学相互依存的关系,下列邮票相关的叙述中没有发生化学变化的是
| A.上海炼钢厂将生铁炼成钢 | B.春牛耕种田地 | C.中国第一颗人造卫星发射 | D.用侯氏制碱法生产纯碱 |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 在实验室采用如图所示装置进行气体的制备、收集、尾气处理,合理的是


| A.用氢氧化钙与氯化铵制备氨气 | B.用浓硝酸与铝制备二氧化氮 |
| C.用二氧化锰与浓盐酸制备氯气 | D.用70%浓硫酸与亚硫酸钠制备二氧化硫 |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 化学与生活、生产及科技密切相关,下列有关说法错误的是
| A.用水玻璃浸泡过的纺织品可防火 |
| B.纳米铁粉主要通过物理吸附作用除去污水中的Cu2+、Ag+、Hg2+ |
| C.中国“奋斗者”号万米载人潜水器的钛合金材料是金属材料 |
| D.75%(体积分数)的酒精、含氯消毒剂均可以有效灭活新型冠状病毒 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 甲、乙、丙、丁对应的物质与图示类别相符的是


| A.甲——氧化钠 | B.乙——氯化钾 |
| C.丙——次氯酸钠 | D.丁——氢氧化钠 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 下列物质鉴别或除杂的方法错误的是
| A.可用NaOH溶液除去氧化镁中的硅单质 |
| B.可用AgNO3溶液鉴别二氧化氮和溴蒸气 |
| C.可用饱和NaHCO3溶液除去氯气中的氯化氢 |
| D.可用稀盐酸鉴别K2CO3和NaHCO3两种溶液 |
您最近一年使用:0次
2021-10-13更新
|
137次组卷
|
2卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
单选题
|
适中(0.65)
名校
7. 甲、乙、丙三种物质中均含有某种相同的元素,它们之间具有如图所示的转化关系(反应条件及部分产物已略去),不能按箭头指示一步实现的是
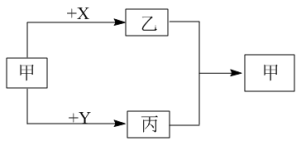

| 选项 | 甲 | X | Y |
| A | N2 | O2 | H2 |
| B | SO2 | NaOH溶液 | H2O2溶液 |
| C | Na2CO3溶液 | Ba(OH)2溶液 | CO2 |
| D | Al2O3 | 稀盐酸 | NaOH溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-13更新
|
285次组卷
|
2卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
单选题
|
适中(0.65)
解题方法
8. 下列离子方程式书写错误的是
A.将SO2通入碘水中:I2+SO2+2H2O=4H++ +2I- +2I- |
B.过量铁粉与稀硝酸反应:Fe+4H++ =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| C.工业上制备漂白液:2OH-+Cl2=Cl-+ClO-+H2O |
| D.Na2O2与足量盐酸反应:2Na2O2+4H+=4Na++O2↑+2H2O |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
9. 下列由实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将红热的碳放入浓硫酸中,并将产生的气体通入澄清的石灰水中 | 澄清石灰水变浑浊 | 碳被浓硫酸氧化成CO2 |
| B | 室温下,将绿豆大小的钠块放入冷水中 | 钠块浮在水面上并熔化成小球 | 钠的密度比水小,熔点低 |
| C | 向黄色的Fe(NO3)3溶液中滴加氢碘酸 | 溶液变为紫红色 | 氧化性:Fe3+>I2 |
| D | 将过量的SO2通入BaCl2溶液中,再通入Cl2 | 先无沉淀生成,后出现白色沉淀 | 生成BaSO4沉淀,体现SO2的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
10. 设阿伏加德罗常数的值为NA,NaOCN与NaClO发生反应:2NaOCN+3NaClO=Na2CO3+3NaCl+CO2↑+N2↑。下列有关说法正确的是
| A.常温下,pH=12的Na2CO3溶液中含OH-数目为0.01NA |
| B.每消耗1 mol NaOCN,上述反应中转移的电子数目为6NA |
| C.1 mol NaClO和NaOCN的混合物中含Na+离子和O原子数目均为NA |
| D.若有11.2LN2生成,则上述反应中生成的CO2中含质子数目为11NA |
【知识点】 物质的量有关计算 氧化还原反应有关计算 水的电离
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 雾霾微颗粒中硫酸盐的生成可能存在三个阶段的转化,其主要过程的示意图如下。下列说法正确的是
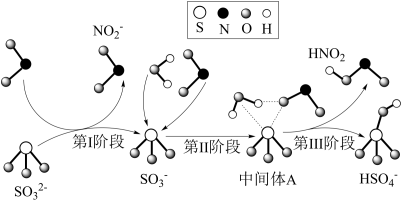

A.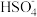 的摩尔质量为97 的摩尔质量为97 |
| B.第I阶段的反应中NO2被氧化 |
| C.HNO2、NO2、H2O均为电解质 |
D.第II、III阶段总反应的化学方程式为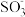 +H2O+NO2=HNO2+ +H2O+NO2=HNO2+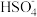 |
【知识点】 摩尔质量 氧化还原反应的几组概念解读 氧化还原反应方程式的配平解读
您最近一年使用:0次
2021-10-13更新
|
455次组卷
|
7卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
单选题
|
适中(0.65)
12. 某混合物粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品于试管中,加入足量稀盐酸,有气泡产生,振荡后固体全部溶解,再加入足量碳酸氢钠溶液,既有沉淀产生,又有气泡产生;
②取少量样品于试管中,加入足量氢氧化钠溶液,振荡后固体部分溶解。
该混合物粉末可能为
①取少量样品于试管中,加入足量稀盐酸,有气泡产生,振荡后固体全部溶解,再加入足量碳酸氢钠溶液,既有沉淀产生,又有气泡产生;
②取少量样品于试管中,加入足量氢氧化钠溶液,振荡后固体部分溶解。
该混合物粉末可能为
| A.Al2O3、BaCO3 | B.NaHSO3、Al(OH)3 |
| C.SiO2、Fe2O3 | D.CaCO3、CuO |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
13. 高铁酸钠(Na2FeO4)具有优异的氧化漂白、杀菌作用。工业上可以用下列四种方法制备高铁酸钠:
①Fe2O3+Na2O2→Na2FeO4+Na2O
②FeSO4+Na2O2→Na2FeO4+Na2O+Na2SO4+O2↑
③Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
④Fe(OH)3+NaClO+NaOH→Na2FeO4+NaCl+H2O
下列说法正确的是
①Fe2O3+Na2O2→Na2FeO4+Na2O
②FeSO4+Na2O2→Na2FeO4+Na2O+Na2SO4+O2↑
③Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
④Fe(OH)3+NaClO+NaOH→Na2FeO4+NaCl+H2O
下列说法正确的是
| A.反应①和②中Na2O2均只作氧化剂 |
| B.Na2FeO4的氧化性强于NaClO、Na2O2 |
| C.反应③中氧化产物和还原产物的物质的量比为2:3 |
| D.反应④中转移3mol电子时,消耗2mol NaOH |
您最近一年使用:0次
2021-10-13更新
|
208次组卷
|
3卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
单选题
|
适中(0.65)
解题方法
14. 化学中常用图象直观地描述化学反应的进程或结果。向100 mL浓度均为1.0 mol·L-1的Na2CO3、NaAlO2混合溶液中滴加2.0 mol·L-1盐酸,下列图象描述正确的是
A. | B. |
C. | D. |
【知识点】 碳酸钠与盐酸的反应解读 偏铝酸钠与盐酸的反应解读
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
15. 锗在航空航天测控、核物理探测、光纤通讯、红外光学、化学催化剂、生物医学等领域有广泛而重要的应用。一种从二氧化锗粗品(主要含GeO2、As2O3)中制备锗的工艺流程如下:
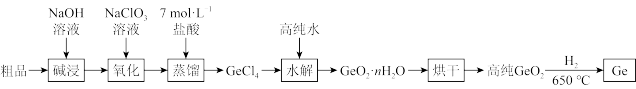
已知:
i.GeO2与Al2O3的性质相似;
ii.GeCl4极易水解,GeCl4的沸点为86.6℃;
iii.As2O3+2NaOH=2NaAsO2+H2O,NaAsO2与盐酸反应生成有毒的AsCl3。
下列说法正确的是

已知:
i.GeO2与Al2O3的性质相似;
ii.GeCl4极易水解,GeCl4的沸点为86.6℃;
iii.As2O3+2NaOH=2NaAsO2+H2O,NaAsO2与盐酸反应生成有毒的AsCl3。
下列说法正确的是
| A.“蒸馏”步骤中用1 mol·L-1盐酸比7 mol·L-1盐酸的效果好 |
| B.在实验室中蒸馏需要用到的玻璃仪器有冷凝管、牛角管、蒸发皿、锥形瓶 |
| C.“水解”反应的化学方程式为GeCl4+(n+2)H2O=GeO2·nH2O↓+4HCl |
| D.“氧化”的目的是将NaAsO2氧化为Na3AsO4,该反应中氧化剂与还原剂的物质的量比为3:1 |
您最近一年使用:0次
16. 向体积均为V mL的0.5 mol·L-1 FeI2和c mol·L-1 FeBr2两种溶液中分别滴加100 mL等浓度的NaNO3溶液,并加入足量稀硫酸,NO3-全部转化为NO,两种溶液反应转移的电子均为0.3 mol,FeI2恰好反应完全(I-只被氧化为I2),FeBr2溶液中Fe2+恰好被完全氧化。下列说法正确的是
| A.V为100 |
| B.两种溶液反应生成NO的质量均为6.0g |
| C.c为1.5 |
D. 全部转化为NO时,两种溶液反应消耗H+的物质的量不相等 全部转化为NO时,两种溶液反应消耗H+的物质的量不相等 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
17. 二氯乙酰氯( )是无色有刺激性气味的液体,沸点为108℃,能与乙醚混溶,遇水和醇会分解,在空气中会发烟,主要用于有机合成及农药、医药中间体,还用于杀菌、消毒等;氯仿(CHCl3沸点为61.2℃)与一氧化碳在无水三氯化铝催化下制备二氯乙酰氯的装置如图所示(部分夹持装置省略,制备一氧化碳的反应原理是HCOOH
)是无色有刺激性气味的液体,沸点为108℃,能与乙醚混溶,遇水和醇会分解,在空气中会发烟,主要用于有机合成及农药、医药中间体,还用于杀菌、消毒等;氯仿(CHCl3沸点为61.2℃)与一氧化碳在无水三氯化铝催化下制备二氯乙酰氯的装置如图所示(部分夹持装置省略,制备一氧化碳的反应原理是HCOOH CO↑+H2O。
CO↑+H2O。

(1)仪器a的名称是___________ ,装置B中浓硫酸的作用是___________ 。
(2)装置A采用的加热方式是___________ (填“酒精灯加热”或“水浴加热”)。
(3)装置C中发生反应的化学方程式为___________ 。
(4)试剂M是___________ ,其作用是___________ 。
(5)装置E是尾气处理装置,还可以用其他方法代替装置E,则其他方法有______ (填一种)。
(6)将二氯乙酰氯与氯仿分离的方法名称是___________ 。
 )是无色有刺激性气味的液体,沸点为108℃,能与乙醚混溶,遇水和醇会分解,在空气中会发烟,主要用于有机合成及农药、医药中间体,还用于杀菌、消毒等;氯仿(CHCl3沸点为61.2℃)与一氧化碳在无水三氯化铝催化下制备二氯乙酰氯的装置如图所示(部分夹持装置省略,制备一氧化碳的反应原理是HCOOH
)是无色有刺激性气味的液体,沸点为108℃,能与乙醚混溶,遇水和醇会分解,在空气中会发烟,主要用于有机合成及农药、医药中间体,还用于杀菌、消毒等;氯仿(CHCl3沸点为61.2℃)与一氧化碳在无水三氯化铝催化下制备二氯乙酰氯的装置如图所示(部分夹持装置省略,制备一氧化碳的反应原理是HCOOH CO↑+H2O。
CO↑+H2O。
(1)仪器a的名称是
(2)装置A采用的加热方式是
(3)装置C中发生反应的化学方程式为
(4)试剂M是
(5)装置E是尾气处理装置,还可以用其他方法代替装置E,则其他方法有
(6)将二氯乙酰氯与氯仿分离的方法名称是
您最近一年使用:0次
2021-10-13更新
|
147次组卷
|
2卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
18. 铜、铬、锰均为过渡元素,其单质及化合物在工业、科技和生产中有着广泛的应用。
(1)Cu2S可用作制防污涂料、污水处理剂、催化剂等。
①灼烧Cu2S时,铜的焰色为___________ (填序号)。
A.黄色 B.洋红色 C.紫色 D.绿色
②用CuS、Cu2S处理酸性废水中的 时发生的反应如下:
时发生的反应如下:
I.CuS+ +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2O
II.Cu2S+ +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2O
当消耗的CuS、Cu2S的物质的量相同时,两者去除 的物质的量比为
的物质的量比为___________ 。
(2)Cr2O3可用于冶金,也可用作陶瓷、耐火材料、颜料业原料及有机合成催化剂等。
①Cr2O3与Al2O3性质类似,具有两性,写出Cr2O3与NaOH溶液反应的离子方程式:___________ 。
②用碳还原重铬酸钾可制备Cr2O3,同时生成一种可燃性有毒气体,当该反应中碳与重铬酸钾的化学计量数比为2:1时,氧化产物的化学式为___________ 。
(3)锰酸钾可用作皮革、纤维漂白剂以及杀菌剂、羊毛的媒染剂等。
①金属锰与熔融碱在氧化剂作用下生成锰酸钾,反应为2Mn+4KOH(熔融)+3O2=2K2MnO4+2H2O,若生成98.5 g K2MnO4,则消耗标准状况下O2的体积为___________ 。
②在KOH溶液的环境中高锰酸钾溶液与亚硫酸钠反应可以制得锰酸钾,写出该反应的离子方程式___________ 。
(1)Cu2S可用作制防污涂料、污水处理剂、催化剂等。
①灼烧Cu2S时,铜的焰色为
A.黄色 B.洋红色 C.紫色 D.绿色
②用CuS、Cu2S处理酸性废水中的
 时发生的反应如下:
时发生的反应如下:I.CuS+
 +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2OII.Cu2S+
 +H+→Cu2++
+H+→Cu2++ +Cr3++H2O
+Cr3++H2O当消耗的CuS、Cu2S的物质的量相同时,两者去除
 的物质的量比为
的物质的量比为(2)Cr2O3可用于冶金,也可用作陶瓷、耐火材料、颜料业原料及有机合成催化剂等。
①Cr2O3与Al2O3性质类似,具有两性,写出Cr2O3与NaOH溶液反应的离子方程式:
②用碳还原重铬酸钾可制备Cr2O3,同时生成一种可燃性有毒气体,当该反应中碳与重铬酸钾的化学计量数比为2:1时,氧化产物的化学式为
(3)锰酸钾可用作皮革、纤维漂白剂以及杀菌剂、羊毛的媒染剂等。
①金属锰与熔融碱在氧化剂作用下生成锰酸钾,反应为2Mn+4KOH(熔融)+3O2=2K2MnO4+2H2O,若生成98.5 g K2MnO4,则消耗标准状况下O2的体积为
②在KOH溶液的环境中高锰酸钾溶液与亚硫酸钠反应可以制得锰酸钾,写出该反应的离子方程式
您最近一年使用:0次
2021-10-13更新
|
267次组卷
|
3卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题(已下线)第10练 金属材料-2022年【寒假分层作业】高一化学(人教版2019)吉林省长春市第六中学2022-2023学年高一上学期期末考试化学试题
四、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
19. 硒化镉(CdSe)用于电子发射器和光谱分析、光导体、半导体、光敏元件等。以镉铁矿(成分为CdO、Fe2O3、FeO及少量的Al2O3和SiO2)为原料制备硒化镉和铁红的工艺流程如图所示:

已知CdSO4易溶于水。
回答下列问题:
(1)“酸浸”时,CdO与稀硫酸反应的离子方程式为___________ 。
(2)常温下,下列物质能与滤渣1发生反应的是___________ (填序号)。
a.浓硝酸 b.碳酸钠 c.氢氟酸
(3)试剂X为___________ 。
(4)“氧化”时加入过量双氧水的目的是将溶液中的Fe2+氧化为Fe3+,检验该溶液中Fe3+的试剂是___________ 。
(5)在实验室中“灼烧”时用到的含硅酸盐的仪器有___________ (任填两种),生成的铁红的用途有___________ (任填一种)。
(6)已知镉铁矿中CdO的质量分数为64%,整个流程中镉元素的损耗率为8%,则1 t该镉铁矿可制得CdSe的质量为___________ kg。

已知CdSO4易溶于水。
回答下列问题:
(1)“酸浸”时,CdO与稀硫酸反应的离子方程式为
(2)常温下,下列物质能与滤渣1发生反应的是
a.浓硝酸 b.碳酸钠 c.氢氟酸
(3)试剂X为
(4)“氧化”时加入过量双氧水的目的是将溶液中的Fe2+氧化为Fe3+,检验该溶液中Fe3+的试剂是
(5)在实验室中“灼烧”时用到的含硅酸盐的仪器有
(6)已知镉铁矿中CdO的质量分数为64%,整个流程中镉元素的损耗率为8%,则1 t该镉铁矿可制得CdSe的质量为
您最近一年使用:0次
2021-10-13更新
|
134次组卷
|
2卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
解答题-无机推断题
|
较难(0.4)
20. 常温下,200 mL某透明溶液中可能含有Na+、Al3+、 、Fe2+、
、Fe2+、 、
、 、OH-和Cl-中的某几种,对该溶液进行如下实验(实验中气体体积均已折算成标准状况下的体积)。
、OH-和Cl-中的某几种,对该溶液进行如下实验(实验中气体体积均已折算成标准状况下的体积)。
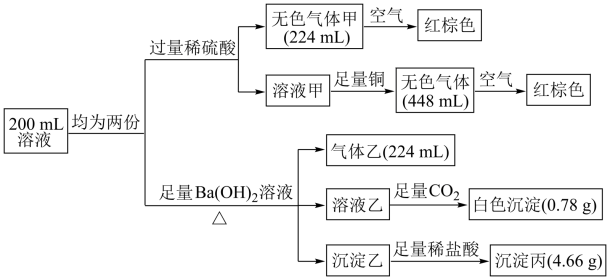
请回答下列问题:
(1)一定不存在的离子是___________ ,沉淀丙的化学式为___________ 。
(2)向溶液甲中加入足量铜产生无色气体的离子方程式为___________ 。
(3)200 mL溶液中 的物质的量是
的物质的量是___________ 。
(4)该溶液中一定存在的阳离子的物质的量比为___________ (要指明相应的离子)。
(5)该溶液中是否存在Cl-?___________ (填“是”或“否”)。
 、Fe2+、
、Fe2+、 、
、 、OH-和Cl-中的某几种,对该溶液进行如下实验(实验中气体体积均已折算成标准状况下的体积)。
、OH-和Cl-中的某几种,对该溶液进行如下实验(实验中气体体积均已折算成标准状况下的体积)。
请回答下列问题:
(1)一定不存在的离子是
(2)向溶液甲中加入足量铜产生无色气体的离子方程式为
(3)200 mL溶液中
 的物质的量是
的物质的量是(4)该溶液中一定存在的阳离子的物质的量比为
(5)该溶液中是否存在Cl-?
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
较难(0.4)
名校
21. 硫及其化合物应用广泛,同时也会对环境造成污染。
(1)硫被用来制造黑色火药、火柴等,也是生产橡胶制品的重要原料。有一种硫单质Sx,该单质蒸气对氢气的相对密度为128,则x=___________ 。
(2)H2S有剧毒,可用作有机合成还原剂、农药、医药、催化剂的再生等。一种脱硫技术如下:第一步,用Na2CO3溶液吸收H2S:H2S+Na2CO3=NaHS+NaHCO3;第二步,用NaVO3溶液与NaHS反应生成硫单质,同时还产生Na2V4O9.Na2V4O9中V的平均化合价为___________ ,第二步反应的离子方程式为___________ 。
(3)SO2尾气先用氨水吸收生成(NH4)2SO3, 再被氧化成
再被氧化成 ,最终得到副产物氮肥,变废为宝。两种氧化方案如下:
,最终得到副产物氮肥,变废为宝。两种氧化方案如下:
方案l:2 +O2=2
+O2=2 。
。
方案2:2[Co(NH3)6]2++O2=[(NH3)5Co-O-O-Co(NH3)5]4++2NH3, +H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌
+H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌ +2[Co(NH3)6]3++2OH-。
+2[Co(NH3)6]3++2OH-。
①氨水中存在的分子有___________ (填化学式)。
②通过实验可知,[(NH3)5Co-O-O-Co(NH3)5]4+将 氧化为
氧化为 的能力大于O2,可能的原因是
的能力大于O2,可能的原因是___________ 。
(4)连二亚硫酸钠(Na2S2O4)适合作木浆造纸的漂白剂。实验室制法:将甲酸和溶于甲醇和水混合溶剂的NaOH混合反应后,再通入SO2气体即可制得连二亚硫酸钠,同时生成能使澄清石灰水变浑浊的气体,则该制备反应的化学方程式为___________ 。
(1)硫被用来制造黑色火药、火柴等,也是生产橡胶制品的重要原料。有一种硫单质Sx,该单质蒸气对氢气的相对密度为128,则x=
(2)H2S有剧毒,可用作有机合成还原剂、农药、医药、催化剂的再生等。一种脱硫技术如下:第一步,用Na2CO3溶液吸收H2S:H2S+Na2CO3=NaHS+NaHCO3;第二步,用NaVO3溶液与NaHS反应生成硫单质,同时还产生Na2V4O9.Na2V4O9中V的平均化合价为
(3)SO2尾气先用氨水吸收生成(NH4)2SO3,
 再被氧化成
再被氧化成 ,最终得到副产物氮肥,变废为宝。两种氧化方案如下:
,最终得到副产物氮肥,变废为宝。两种氧化方案如下:方案l:2
 +O2=2
+O2=2 。
。方案2:2[Co(NH3)6]2++O2=[(NH3)5Co-O-O-Co(NH3)5]4++2NH3,
 +H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌
+H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌ +2[Co(NH3)6]3++2OH-。
+2[Co(NH3)6]3++2OH-。①氨水中存在的分子有
②通过实验可知,[(NH3)5Co-O-O-Co(NH3)5]4+将
 氧化为
氧化为 的能力大于O2,可能的原因是
的能力大于O2,可能的原因是(4)连二亚硫酸钠(Na2S2O4)适合作木浆造纸的漂白剂。实验室制法:将甲酸和溶于甲醇和水混合溶剂的NaOH混合反应后,再通入SO2气体即可制得连二亚硫酸钠,同时生成能使澄清石灰水变浑浊的气体,则该制备反应的化学方程式为
【知识点】 离子反应的发生及书写 氨气 二氧化硫
您最近一年使用:0次
2021-10-13更新
|
698次组卷
|
3卷引用:河南省的商丘市、周口市,安徽省...“皖豫名校联盟体” 2021-2022学年高三上学期第一次考试化学试题
试卷分析
整体难度:适中
考查范围:化学与STSE、初中衔接知识点、常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、化学反应原理
试卷题型(共 21题)
题型
数量
单选题
16
解答题
3
填空题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学对人类文明发展的意义 化学与社会发展 | |
| 2 | 0.85 | 碳酸氢钠 碳酸氢钠的不稳定性 铁矿石与高炉炼铁 化学科学对人类文明发展的意义 | |
| 3 | 0.65 | 氯气的实验室制法 氨气的实验室制法 常见无机物的制备 | |
| 4 | 0.65 | 硅酸钠的俗名和用途 蛋白质的变性 金属材料的应用 | |
| 5 | 0.65 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 漂白粉和漂粉精的制备原理 溴、碘单质与碱的反应 | |
| 6 | 0.65 | 硅的化学性质 碳酸氢钠与酸反应 物质的分离、提纯 物质分离、提纯的常见化学方法 | |
| 7 | 0.65 | 氨的还原性 含硫化合物之间的转化 碳酸钠与碳酸氢钠的相互转化 铝三角转化 | |
| 8 | 0.65 | 离子方程式的正误判断 氯气与碱溶液反应 硝酸的强氧化性 二氧化硫与其他强氧化剂的反应 | |
| 9 | 0.65 | 硝酸的强氧化性 二氧化硫与其他强氧化剂的反应 浓硫酸的强氧化性 钠与水反应原理 | |
| 10 | 0.65 | 物质的量有关计算 氧化还原反应有关计算 水的电离 | |
| 11 | 0.65 | 摩尔质量 氧化还原反应的几组概念 氧化还原反应方程式的配平 | |
| 12 | 0.65 | 二氧化硅的化学性质 氧化铝与酸反应 氧化铝与碱溶液反应 | |
| 13 | 0.65 | 氧化还原反应的几组概念 氧化还原反应有关计算 氧化还原反应方程式的配平 | |
| 14 | 0.65 | 碳酸钠与盐酸的反应 偏铝酸钠与盐酸的反应 | |
| 15 | 0.4 | 氧化还原反应的几组概念 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 16 | 0.65 | 氧化还原反应方程式的配平 基于氧化还原反应守恒规律的计算 硝酸的强氧化性 电子转移计算 | |
| 二、解答题 | |||
| 17 | 0.65 | 常用仪器及使用 常见有机物的制备 综合实验设计与评价 | 实验探究题 |
| 19 | 0.65 | 二氧化硅的化学性质 Fe2+的还原性 铁盐的检验 物质分离、提纯综合应用 | 工业流程题 |
| 20 | 0.4 | 离子共存 硝酸 一氧化氮 其他含铝化合物 | 无机推断题 |
| 三、填空题 | |||
| 18 | 0.65 | 化学方程式计算中物质的量的运用 氧化还原反应方程式的配平 焰色试验 氧化铝与碱溶液反应 | |
| 21 | 0.4 | 离子反应的发生及书写 氨气 二氧化硫 | |



