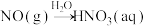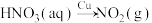江苏省淮安市2022-2023学年高一下学期期末调研测试化学试题
江苏
高一
期末
2023-08-15
473次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学与STSE、有机化学基础、化学实验基础、化学反应原理、物质结构与性质
江苏省淮安市2022-2023学年高一下学期期末调研测试化学试题
江苏
高一
期末
2023-08-15
473次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学与STSE、有机化学基础、化学实验基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. “材料是人类文明的基础,现代生活处处离不开材料。”下列生活材料的主要成分是有机化合物的是
| A.镁铝合金 | B.汽车轮胎 | C.光导纤维 | D.陶瓷餐具 |
您最近一年使用:0次
2. 下列有关化学用语正确的是
A.氯原子的结构示意图: | B.乙醇的结构式: |
C. 的电子式: 的电子式: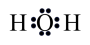 | D.甲烷的球棍模型: |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 下列有关物质性质与用途具有对应关系的是
| A.苯易挥发,可用作萃取剂 | B.SiO2硬度高,可用作半导体材料 |
| C.Fe2O3能与酸反应,可用作红色颜料 | D.SO2有还原性,可用作葡萄酒的抗氧化剂 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
您最近一年使用:0次
2023-07-11更新
|
143次组卷
|
4卷引用:江苏省阜宁中学2022-2023学年高一下学期第一次综合测试化学试题
单选题
|
适中(0.65)
名校
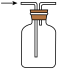
5. 下列装置能达到实验目的的是( )
| A.制取NH3 | B.干燥NH3 | C.收集NH3 | D.处理尾气 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-11更新
|
192次组卷
|
2卷引用:江苏省淮安市2022-2023学年高一下学期期末调研测试化学试题
6. 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业。合成氨反应为
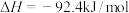 。下列有关合成氨反应的说法正确的是
。下列有关合成氨反应的说法正确的是

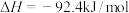 。下列有关合成氨反应的说法正确的是
。下列有关合成氨反应的说法正确的是A.反应的 (E表示键能) (E表示键能) |
B.反应中每消耗 转移电子的数目约等于 转移电子的数目约等于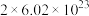 |
C. 和 和 在一定条件下发生反应放出的热量为92.4kJ 在一定条件下发生反应放出的热量为92.4kJ |
D.当容器内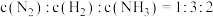 时反应达到平衡状态 时反应达到平衡状态 |
您最近一年使用:0次
单选题
|
容易(0.94)
名校
解题方法
7. W、X、Y、Z为四种短周期主族元素,其中W在周期表中原子半径最小;X、Y同主族,Y、Z同周期,X原子最外层电子数是核外电子层数的3倍;Z的最高正价与最低负价的代数和为6,下列说法正确的是
A.W与X可以形成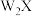 , , 两种物质 两种物质 |
B.原子半径由小到大的顺序是 |
C.Z元素最高价氧化物对应水化物的化学式为 |
| D.Y、Z两元素的气态氢化物中,Y的气态氢化物更稳定 |
您最近一年使用:0次
2023-07-11更新
|
231次组卷
|
3卷引用:江苏省淮安市2022-2023学年高一下学期期末调研测试化学试题
单选题
|
适中(0.65)
解题方法
8. 氢气和氧气发生反应的过程用如下模型表示(“—”表示化学键),下列说法正确的是

| A.过程I是放热过程 |
| B.过程Ⅲ一定是吸热过程 |
| C.该反应的能量转化形式只能以热能的形式进行 |
| D.该反应过程中参加反应物质的旧化学键都断裂,且形成了新化学键 |
您最近一年使用:0次
9. 香叶醇是合成玫瑰香油的主要原料,其结构简式如图,下列有关香叶醇的叙述正确的
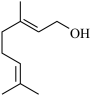

| A.属于乙醇的同系物 | B.香叶醇的分子式为C10H18O |
| C.不能使酸性高锰酸钾溶液褪色 | D.能与氢气按1:2发生加成反应,不能发生取代反应 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 我国科学家以LiI为催化剂,通过改变盐的浓度调节锂—氧气电池放电效率,模拟装置如图所示。下列说法正确的是
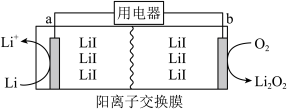

| A.放电时,a电极为正极 |
| B.放电时,电流由b极经用电器流向a极 |
C.充电时,阳极上的电极反应式为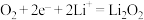 |
| D.充电时,a极净增14g时电路中转移1mol电子 |
您最近一年使用:0次
12. 下列实验操作、现象、解释与结论均正确的是
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向红色布条上滴加几滴新制氯水 | 红色布条褪色 | 新制氯水有漂白性 |
| B | 向鸡蛋清溶液中加入饱和的硫酸铵溶液 | 产生白色沉淀 | 硫酸铵能使蛋白质发生变性 |
| C | 向淀粉溶液中滴加少量稀硫酸,加热,待冷却后,再加入少量新制的Cu(OH)2悬浊液,加热至沸腾 | 无砖红色沉淀 | 淀粉未发生水解 |
| D | 向FeCl3溶液中滴加维生素C溶液 | 溶液变为浅绿色 | 维生素C有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
13. 工业上用铝土矿(主要成分Al2O3,含SiO2、Fe2O3等杂质)冶炼铝的主要流程如下:

(注:SiO2碱溶时转变为铝硅酸钠沉淀)
下列叙述错误的是

(注:SiO2碱溶时转变为铝硅酸钠沉淀)
下列叙述错误的是
| A.操作I适当增大NaOH溶液浓度可提高Al2O3的浸取速率 |
B.通入过量CO2的离子方程式为: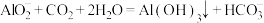 |
| C.实验室进行操作IV的仪器有蒸发皿、酒精灯、铁架台等 |
| D.加入的冰晶石目的是降低Al2O3的熔融温度 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
解题方法
14. 氮及其化合物是重要的化工原料,研究其性质、用途和转化具有重要意义。
回答下列问题:

(1)X属于___________ (填“离子”或“共价”)化合物;常温下,NO2为___________ (填颜色)气体。
(2)物质N2H4(肼)可作为火箭发动机的燃料,已知在298K、101kPa时1g液态肼燃烧生成氮气和液态水,释放19.44kJ的热量,写出表示其燃烧热的热化学方程式___________ 。
(3)农业上常用物质R作氮肥,实验室检验物质R中阳离子的方法为___________ (写出操作过程和现象)。
(4)硫可与Q的浓溶液反应,硫转化为___________ (化学式)。
(5)氮的氧化物(NOx)是常见的大气污染物之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质Y与NO2的物质的量之比为1:1时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,该反应的化学方程式为___________ 。
回答下列问题:

(1)X属于
(2)物质N2H4(肼)可作为火箭发动机的燃料,已知在298K、101kPa时1g液态肼燃烧生成氮气和液态水,释放19.44kJ的热量,写出表示其燃烧热的热化学方程式
(3)农业上常用物质R作氮肥,实验室检验物质R中阳离子的方法为
(4)硫可与Q的浓溶液反应,硫转化为
(5)氮的氧化物(NOx)是常见的大气污染物之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。当物质Y与NO2的物质的量之比为1:1时,与足量氨气能在催化剂作用下发生反应,生成两种无污染的物质,该反应的化学方程式为
您最近一年使用:0次
15. 已知A是一种气态烃,其密度在标准状况下是H2的14倍,A的产量是衡量一个国家石油化工发展水平的标志。下列关系图中部分产物可能略去,试回答下列问题:
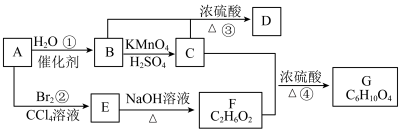
已知: 。
。
(1)A的名称为___________ ,丙烯与A互为同系物,聚丙烯的结构简式为___________ 。
(2)C中官能团的名称是___________ ,F的结构简式为___________ 。
(3)反应④的反应类型是___________ 。
(4)B物质在铜的催化作用下被氧气氧化为具有刺激性气味的物质,写出该反应的化学方程式___________ 。
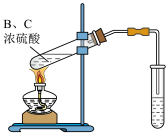
(5)实验室用B和C反应制取D,装置如图所示。右侧试管中的试剂是___________ ,分离该试管中油状液体用到的主要仪器是___________ 。

已知:
 。
。(1)A的名称为
(2)C中官能团的名称是
(3)反应④的反应类型是
(4)B物质在铜的催化作用下被氧气氧化为具有刺激性气味的物质,写出该反应的化学方程式
(5)实验室用B和C反应制取D,装置如图所示。右侧试管中的试剂是

您最近一年使用:0次
2023-07-11更新
|
238次组卷
|
2卷引用:江苏省淮安市2022-2023学年高一下学期期末调研测试化学试题
16. CO2循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减少CO2的排放,可用下列方法把CO2转化成燃料,试回答下列问题:
反应I:

反应II:
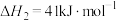
反应III:

(1)计算可知
___________  。
。
(2)某温度下,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,按反应I进行反应,测得CO2和CH3OH的物质的量随时间变化如图1:

①0~2min内,用CH3OH表示的反应速率为___________ ,该反应达到最大限度时H2的转化率为___________ ,此时CH3OH在平衡混合物中的体积分数为___________ 。
②下列措施可以提高该化学反应速率的是___________ (填选项序号)。
A.升高温度 B.容器体积不变,充入He
C.增大容器的体积 D.容器体积不变,充入更多的H2(g)
③下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.
C.混合气体的压强不随时间的变化而变化
D.混合气体的密度不再改变
(3)H2还原CO电化学法制备甲醇(见反应III)的工作原理如图2所示:电池工作过程中H+通过质子膜向___________ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________ 。

反应I:


反应II:

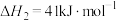
反应III:


(1)计算可知

 。
。(2)某温度下,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,按反应I进行反应,测得CO2和CH3OH的物质的量随时间变化如图1:

①0~2min内,用CH3OH表示的反应速率为
②下列措施可以提高该化学反应速率的是
A.升高温度 B.容器体积不变,充入He
C.增大容器的体积 D.容器体积不变,充入更多的H2(g)
③下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.

C.混合气体的压强不随时间的变化而变化
D.混合气体的密度不再改变
(3)H2还原CO电化学法制备甲醇(见反应III)的工作原理如图2所示:电池工作过程中H+通过质子膜向

您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
17. 纳米铁粉常用于废水处理,以草酸(H2C2O4)与FeSO4为原料可制取纳米铁粉。
I.制取草酸
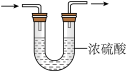
用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液氧化淀粉水解液制备草酸,其装置如下图所示。[已知:硝酸氧化淀粉水解液过程中主要反应: (未配平)]
(未配平)]

(1)仪器甲的名称为___________ 。
(2)装置B的作用___________ 。
(3)控制反应温度不超过60℃可以防止有机物脱水炭化和___________ 。
Ⅱ.制备纳米铁粉,其流程如下:

已知:H2C2O4为二元弱酸。
(4)检验酸溶后的溶液是否含Fe3+的试剂是___________ 。
(5)向酸溶后的溶液中滴加稍过量的H2C2O4,过滤得FeC2O4∙2H2O。
①沉淀反应的离子方程式为___________ 。
②过滤所得沉淀中FeC2O4∙2H2O含量的测定:准确称取5.800g沉淀,加入适量的蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol∙L-1 KMnO4溶液,完全反应时,消耗KMnO4溶液18.00mL。过程中发生的反应为: (未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数
(未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数___________ (写出计算过程)。
I.制取草酸
用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液氧化淀粉水解液制备草酸,其装置如下图所示。[已知:硝酸氧化淀粉水解液过程中主要反应:
 (未配平)]
(未配平)]
(1)仪器甲的名称为
(2)装置B的作用
(3)控制反应温度不超过60℃可以防止有机物脱水炭化和
Ⅱ.制备纳米铁粉,其流程如下:

已知:H2C2O4为二元弱酸。
(4)检验酸溶后的溶液是否含Fe3+的试剂是
(5)向酸溶后的溶液中滴加稍过量的H2C2O4,过滤得FeC2O4∙2H2O。
①沉淀反应的离子方程式为
②过滤所得沉淀中FeC2O4∙2H2O含量的测定:准确称取5.800g沉淀,加入适量的蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol∙L-1 KMnO4溶液,完全反应时,消耗KMnO4溶液18.00mL。过程中发生的反应为:
 (未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数
(未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、化学与STSE、有机化学基础、化学实验基础、化学反应原理、物质结构与性质
试卷题型(共 17题)
题型
数量
单选题
13
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 无机物与有机物 二氧化硅的用途 光导纤维与硅芯片 | |
| 2 | 0.65 | 原子结构示意图、离子结构示意图 共价型分子结构式、电子式 甲烷分子空间构型 乙醇的“三式一型” | |
| 3 | 0.65 | 二氧化硫与其他强氧化剂的反应 硅的物理性质与用途 二氧化硅的用途 几种铁的氧化物的物理性质及用途 | |
| 4 | 0.65 | 氨的还原性 一氧化氮的化学性质 二氧化氮与水反应 硝酸的强氧化性 | |
| 5 | 0.65 | 氨的碱性 氨与水的反应 氨气的实验室制法 常见气体的制备与收集 | |
| 6 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡状态的判断方法 电子转移计算 | |
| 7 | 0.94 | 元素周期律、元素周期表的推断 由元素性质的递变规律进行相关推断 | |
| 8 | 0.65 | 化学键与化学反应中的能量关系 常见能量转化形式 吸热反应和放热反应 | |
| 9 | 0.65 | 同系物的判断 加成反应 醇的取代反应 醇与强氧化剂的氧化反应 | |
| 10 | 0.65 | 电解池电解基本判断 氯碱工业 金属的防护 油脂在碱性条件下水解 | |
| 11 | 0.65 | 原电池正负极判断 原电池电极反应式书写 电解原理的理解及判断 电解池电极反应式及化学方程式的书写与判断 | |
| 12 | 0.65 | 次氯酸及其性质 Fe3+与其他物质氧化性强弱关系 淀粉水解及其产物检验相关实验 蛋白质的盐析 | |
| 13 | 0.65 | 离子方程式的书写 含氧化铝的混合物的提纯 常用仪器及使用 物质制备的探究 | |
| 二、解答题 | |||
| 14 | 0.65 | 无机综合推断 氨的还原性 硝酸的强氧化性 依据热化学方程式的计算 | 无机推断题 |
| 15 | 0.65 | 乙烯的加成反应 乙醇催化氧化 乙酸的酯化反应的机理 有机推断综合考查 | 无机推断题 |
| 16 | 0.65 | 盖斯定律及其有关计算 化学平衡状态的判断方法 转化率的相关计算及判断 原电池电极反应式书写 | 原理综合题 |
| 17 | 0.65 | 离子方程式的书写 铁盐的检验 探究物质组成或测量物质的含量 氧化还原原理滴定 | 实验探究题 |