已知: 。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl,
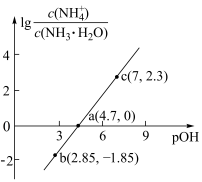
。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl, 随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是
随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是
 。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl,
。室温下,向浓度为0.1mol·L-1的氨水中缓缓通入HCl, 随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是
随pOH的变化曲线如下图所示。假设溶液体积没有变化,下列推断正确的是
| A.NH3·H2O的电离常数的数量级为10-4 |
B.b点溶液中: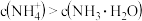 |
C.c点溶液中: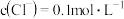 |
D.pOH=8的溶液中: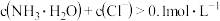 |
2020·福建莆田·二模 查看更多[5]
吉林省长春市第二中学2023-2024学年高二上学期11月期中考试化学试题(已下线)学科网2020年高三11月大联考考后强化卷(广东卷)(已下线)练习6 电离平衡与溶液的PH-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 方法帮福建省莆田市2020届高三5月第二次检测理科综合化学试卷
更新时间:2020-06-11 22:04:41
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】pH是溶液中 的负对数,若定义pC是溶液中微粒物质的量浓度的负对数,则常温下, 某浓度的草酸
的负对数,若定义pC是溶液中微粒物质的量浓度的负对数,则常温下, 某浓度的草酸 水溶液中
水溶液中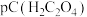 ,
, 、
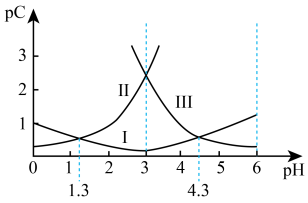
、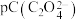 随着溶液pH的变化曲线如图所示。下列说法 不 正 确的是
随着溶液pH的变化曲线如图所示。下列说法 不 正 确的是
 的负对数,若定义pC是溶液中微粒物质的量浓度的负对数,则常温下, 某浓度的草酸
的负对数,若定义pC是溶液中微粒物质的量浓度的负对数,则常温下, 某浓度的草酸 水溶液中
水溶液中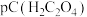 ,
, 、
、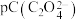 随着溶液pH的变化曲线如图所示。下列说法 不 正 确的是
随着溶液pH的变化曲线如图所示。下列说法 不 正 确的是 
A.曲线Ⅰ代表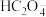 的浓度随着pH增大先变小后变大 的浓度随着pH增大先变小后变大 |
B.草酸的电离常数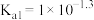 ; ;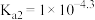 |
C. 时, 时,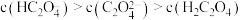 |
D. |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知25℃时有关弱酸的电离平衡常数如下:
则下列有关说法正确的是
| 弱酸化学式 |  | HCN |  |
| 电离平衡常数 |  |  |  |
A.浓度均为 的上述三种溶液,加水稀释10倍后,三者物质的量浓度的关系为 的上述三种溶液,加水稀释10倍后,三者物质的量浓度的关系为 |
B.等体积等浓度的上述三种酸溶液中, 的物质的量分别为a mol、b mol、c mol,其关系为a>c>b 的物质的量分别为a mol、b mol、c mol,其关系为a>c>b |
C.NaCN溶液中通入少量 发生的化学反应为 发生的化学反应为 |
D.稀释HCN溶液过程中, 减小 减小 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】向 溶液中滴加NaOH溶液,溶液中
溶液中滴加NaOH溶液,溶液中 ,
, ,
, ,
, 的分布系数(
的分布系数( )如下图所示 [
)如下图所示 [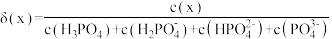 ],下列表述正确的是
],下列表述正确的是
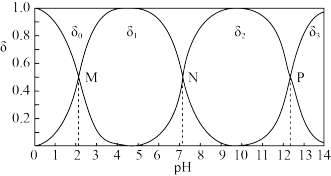
 溶液中滴加NaOH溶液,溶液中
溶液中滴加NaOH溶液,溶液中 ,
, ,
, ,
, 的分布系数(
的分布系数( )如下图所示 [
)如下图所示 [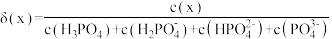 ],下列表述正确的是
],下列表述正确的是
A.由图可知,磷酸的电离平衡常数间存在如下关系: |
B.N点对应的溶液中: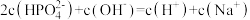 |
C.P点的溶液中, |
D.已知 的 的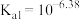 , , ,则制备 ,则制备 和 和 均可用 均可用 和 和 为原料 为原料 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】25C时,用1.0mol·L-1NaOH溶液滴定20mL1.0mol·L-1甲酸溶液,得到混合液中 HCOOH、HCOO-的物质的量与溶液pH的变化关系如下图所示。下列说法正确的是
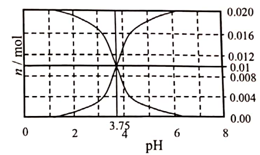

| A.pH=5时,溶液中:c(Na+)<c(HCOO-) |
| B.pH=4.75 时, c(HCOO-)︰c(HCOOH)=1︰10 |
| C.pH=4时,溶液中:c(HCOOH)+c(Na+)+c(H+)-c(OH-)=0.02mol·L-1 |
| D.pH=3.75时,NaOH溶液恰好与 HCOOH完全反应 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,向20mL浓度均为0.1mol·L-1的HX和CH3COOH的混合溶液中滴加0.1mol·L-1的氨水,测得溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积(V)的关系如图。(CH3COOH的Ka=1.8×10-5,NH3·H2O的Kb=1.8×10-5),下列说法正确的是


| A.常温时,同浓度的HX溶液比CH3COOH溶液的pH大 |
| B.a→c过程,水的电离程度先减小后增大 |
C.溶液pH=7时对应的点在c点和d点之间,此时溶液中存在: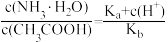 |
D.混合时若忽略体积变化,d点时:4c(NH )+4c(NH3·H2O)=0.3mol·L-1 )+4c(NH3·H2O)=0.3mol·L-1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】 时,下列溶液中微粒的物质的量浓度关系正确的是
时,下列溶液中微粒的物质的量浓度关系正确的是
 时,下列溶液中微粒的物质的量浓度关系正确的是
时,下列溶液中微粒的物质的量浓度关系正确的是A. 的盐酸与 的盐酸与 的 的 溶液混合后: 溶液混合后: |
B.0.1mol/L的NaHS溶液中: |
C.100mL1.0mol/L的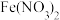 溶液和100mL2.0mol/L的HNO3溶液混合后(忽略混合后溶液体积变化): 溶液和100mL2.0mol/L的HNO3溶液混合后(忽略混合后溶液体积变化): |
D.0.1mol/L的HCN溶液和0.1mol/L的NaCN溶液等体积混合后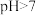 : : |
您最近半年使用:0次

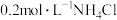 溶液与
溶液与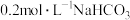 溶液等体积混合后(忽略体积变化),所得混合溶液的pH为7.8。溶液中的含碳粒子和含氮粒子的分布系数(
溶液等体积混合后(忽略体积变化),所得混合溶液的pH为7.8。溶液中的含碳粒子和含氮粒子的分布系数( )随溶液pH的变化如图所示:
)随溶液pH的变化如图所示:
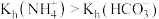
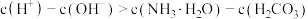
 、
、 均逐渐减小
均逐渐减小


