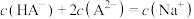已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
| A.水的电离度始终增大 | B.c(NH4+)/c(NH3·H2O) 先增大再减小 |
| C.c(CH3COOH) +c(CH3COO-)不变 | D.加入氨水的体积为10 mL,c(H+)=Kw1/2mol/L |
更新时间:2018-01-31 22:11:12
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】纯的叠氮酸(HN3)是一种弱酸,常温下用 0.2 mol·L-1HN3 溶液滴入 25mL0.1 mol·L-1NaOH 溶液中,滴加过程中的pH 值的变化曲线(溶液混合时的体积变化忽略不计) 如图。下列说法正确的是
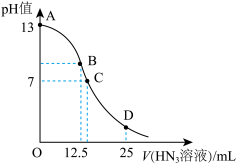

| A.该滴定过程用甲基橙作指示剂 |
B.点 B 对应溶液中: |
C.点 D 对应溶液中: |
| D.沿曲线 A→B→C 的过程中,由水电离产生的 c(OH-)逐渐减少 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】含 杂质的
杂质的 矿物,用
矿物,用 处理后,过滤,滤液里添加
处理后,过滤,滤液里添加 溶液,产生
溶液,产生 沉淀、溶液
沉淀、溶液 随
随 溶液体积关系如图所示,下列说法
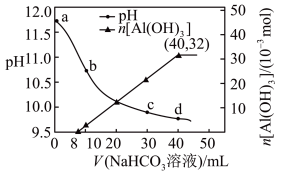
溶液体积关系如图所示,下列说法不正确 的是
 杂质的
杂质的 矿物,用
矿物,用 处理后,过滤,滤液里添加
处理后,过滤,滤液里添加 溶液,产生
溶液,产生 沉淀、溶液
沉淀、溶液 随
随 溶液体积关系如图所示,下列说法
溶液体积关系如图所示,下列说法
A.一开始添加 溶液没有沉淀的原因是: 溶液没有沉淀的原因是: |
| B.b点水的电离程度大于d点水的电离程度 |
C.c点溶液中存在: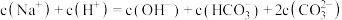 |
D.滤液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】向1000 mL 3mol/LNaOH中通入适量CO2气体,溶液中有关阴离子的物质的量变化曲线如图所示:
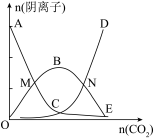
下列说法正确的是

下列说法正确的是
A.CD段反应的离子方程式为OH-+CO2=HCO |
| B.水的电离程度先增大后减小 |
| C.溶液的pH先减小后增大 |
| D.M、N两点对应的溶液中离子种类不同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知NaClO2在水溶液中能发生水解。常温时,有1 mol/L的HClO2溶液和1mol/L的HBF4(氟硼酸)溶液起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积为V,所得曲线如图所示。下列说法错误的是


| A.HClO2为弱酸,HBF4为强酸 |
| B.常温下HClO2的电高平衡常数的数量级为10—4 |
| C.在0≤pH≤5时,HBF4溶液满足pH=lg(V/V0) |
| D.25℃时1L pH=2的HBF4溶液与100℃时1L pH=2的HBF4溶液消耗的NaOH相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】“84”消毒液和“洁厕灵”混用时,可发生反应使人中毒,若发生的反应为 。下列说法正确的是[设
。下列说法正确的是[设 为阿伏加德罗常数的值,已知:
为阿伏加德罗常数的值,已知: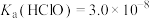 ,
, ,
, ]
]
 。下列说法正确的是[设
。下列说法正确的是[设 为阿伏加德罗常数的值,已知:
为阿伏加德罗常数的值,已知: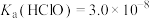 ,
, ,
, ]
]A.理论上,上述反应生成的1  中含有的中子数为40 中含有的中子数为40 |
B.“84”消毒液在空气中会发生反应: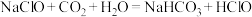 |
C.理论上,每转移1 电子,参与反应的氧化剂比还原剂少2g 电子,参与反应的氧化剂比还原剂少2g |
D.为提高氯水中 的浓度,可加过量 的浓度,可加过量 固体 固体 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】工业上常用 作沉淀剂除去废水中的
作沉淀剂除去废水中的 和
和 。通过调节溶液的pH可使
。通过调节溶液的pH可使 和
和 逐一沉降,处理过程中始终保持
逐一沉降,处理过程中始终保持 溶液为饱和状态即
溶液为饱和状态即 mol/L,体系中
mol/L,体系中 、
、 、
、 ,
, 浓度(mol/L)的负对数pM与pH的关系如图所示。已知:
浓度(mol/L)的负对数pM与pH的关系如图所示。已知: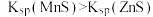 。下列说法不正确的是
。下列说法不正确的是
 作沉淀剂除去废水中的
作沉淀剂除去废水中的 和
和 。通过调节溶液的pH可使
。通过调节溶液的pH可使 和
和 逐一沉降,处理过程中始终保持
逐一沉降,处理过程中始终保持 溶液为饱和状态即
溶液为饱和状态即 mol/L,体系中
mol/L,体系中 、
、 、
、 ,
, 浓度(mol/L)的负对数pM与pH的关系如图所示。已知:
浓度(mol/L)的负对数pM与pH的关系如图所示。已知: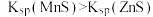 。下列说法不正确的是
。下列说法不正确的是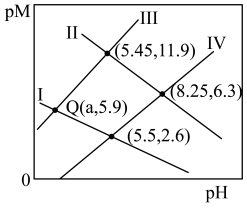
A.Ⅱ表示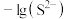 与pH的关系曲线 与pH的关系曲线 |
B.Q点对应 的数量级为 的数量级为 |
C.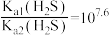 |
D.溶液中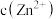 和 和 均为0.1mol/L, 均为0.1mol/L, 完全沉淀时溶液的最小pH为2 完全沉淀时溶液的最小pH为2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列实验操作、现象与结论相匹配的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向 溶液中通入 溶液中通入 | 产生白色沉淀 | 白色沉淀是 |
| B | 常温下,分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 |  均等于7 均等于7 | 常温下, 的 的 溶液和 溶液和 溶液中水的电离程度相等 溶液中水的电离程度相等 |
| C | 向沸水中滴入几滴 饱和溶液,继续煮沸,并用激光笔照射 饱和溶液,继续煮沸,并用激光笔照射 | 溶液变红褐色,出现丁达尔效应 | 产生了 胶体 胶体 |
| D | 向 溶液中滴加 溶液中滴加 等浓度的 等浓度的 溶液,再加入 溶液,再加入 等浓度的 等浓度的 溶液 溶液 | 先产生白色沉淀后产生黑色沉淀 | 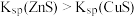 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】室温下,下列实验探究方案能达到探究目的的是
| 选项 | 实验探究方案 | 探究目的 |
| A | 用pH计测量相同浓度CH3COONa和Na2CO3溶液的pH | 比较CH3COOH和H2CO3的酸性 |
| B | 将铁锈溶于浓盐酸,再向溶液中滴入几滴KMnO4溶液,观察溶液颜色变化 | 铁锈中含有二价铁 |
| C | 常温下,向10mL0.1mol·L-1NaCl溶液中滴加5滴0.1mol·L-1AgNO3溶液,充分反应后,再滴加5滴0.1mol·L-1KI溶液,观察沉淀颜色变化 | Ksp(AgCl)>Ksp(AgI) |
| D | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液,观察溶液颜色 | 氧化性:H2O2>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】室温下,甘氨酸在水溶液中主要以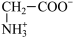 、
、 和
和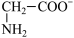 三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )

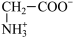 、
、 和
和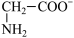 三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
| A.a点溶液中,水的电离程度大于b点 |
B.c点溶液中,c(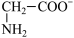 )>c( )>c(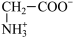 ) ) |
C.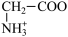 +H2O +H2O 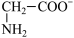 +H3O+的平衡常数为x +H3O+的平衡常数为x |
D.a点溶液中,存在关系式:c( )+c(H+)=c( )+c(H+)=c(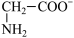 )+c(OH-) )+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列说法正确的是( )
| A.100℃时,KW=10﹣12,此温度下pH=6的溶液一定显酸性 |
| B.25℃时,0.1mol/L的NaHSO3溶液pH=4,说明HSO3﹣在水溶液中只存在电离 |
| C.NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 |
| D.25℃时,10mL 0.1mol/L CH3COOH溶液与5mL 0.1mol/L NaOH溶液混合,所得溶液中有2c(Na+)═c(CH3COO﹣)+c(CH3COOH) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,在体积均为20mL、浓度均为0.lmol•L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)的负对数[-lgc(H+)水]与滴加氢氧化钠溶液体积的关系如图所示:下列说法不正确 的是


| A.a、b、c三点溶液均显中性 |
| B.a点溶液,c(Na+)=c(X-)>c(H+)=c(OH-) |
| C.b点溶液中的离子总浓度大于d点溶液 |
| D.常温下,Ka(HX)≈10-5 |
您最近一年使用:0次

 在溶液中各组分百分含量
在溶液中各组分百分含量 随溶液pH的变化如图所示。下列说法错误的是
随溶液pH的变化如图所示。下列说法错误的是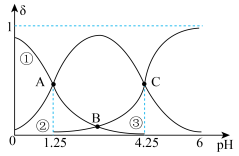
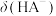 随溶液pH的变化
随溶液pH的变化 的一级电离常数
的一级电离常数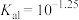
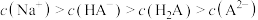
 溶液中滴加
溶液中滴加