Ⅰ.常温下,如果取0.2 mol/LCH3COOH溶液与0.2 mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,试回答以下问题:
(1)写出该混合过程中所发生反应的离子方程式:__________________ ,混合溶液的pH=9的原因是:(用必要的文字和离子方程式表示)________________ 。
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比值为_________ 。
(3)求该混合溶液中下列算式的计算结果:
c(Na+)-c(CH3COO-)=_________ mol/L(代入数据,列出算式即可)
c(OH-)-c(CH3COOH)=_________ moL/L。
Ⅱ.(4)由表格中的电离平衡常数判断可以发生的反应是_________ (填字母序号)。
A.NaClO+NaHCO3=HClO+Na2CO3
B.2HClO+Na2CO3=2NaClO+CO2↑+H2O
C.2NaClO+CO2+H2O=2HClO+Na2CO3
D.NaClO+CO2+H2O=HClO+NaHCO3
(5)将同温度下等浓度的下列四种盐溶液:(已知常温下一水合氨的电离常数Kb=1.8×10-5;碳酸的电离常数:Ka1=4.4×10-7,Ka2=4.7×10-11)
A.NH4HCO3 B.NH4Cl C.(NH4)2SO4 D.CH3COONH4
按pH由大到小的顺序排列:_________ (填字母序号)。
(6)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是_________ (填字母序号)。
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3 ⑤NaHCO3 ⑥高锰酸钾
A.③④ B.①③④ C.①②③④⑤ D.全部
(1)写出该混合过程中所发生反应的离子方程式:
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比值为
(3)求该混合溶液中下列算式的计算结果:
c(Na+)-c(CH3COO-)=
c(OH-)-c(CH3COOH)=
Ⅱ.(4)由表格中的电离平衡常数判断可以发生的反应是
| 化学式 | 常温下的电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
A.NaClO+NaHCO3=HClO+Na2CO3
B.2HClO+Na2CO3=2NaClO+CO2↑+H2O
C.2NaClO+CO2+H2O=2HClO+Na2CO3
D.NaClO+CO2+H2O=HClO+NaHCO3
(5)将同温度下等浓度的下列四种盐溶液:(已知常温下一水合氨的电离常数Kb=1.8×10-5;碳酸的电离常数:Ka1=4.4×10-7,Ka2=4.7×10-11)
A.NH4HCO3 B.NH4Cl C.(NH4)2SO4 D.CH3COONH4
按pH由大到小的顺序排列:
(6)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3 ⑤NaHCO3 ⑥高锰酸钾
A.③④ B.①③④ C.①②③④⑤ D.全部
更新时间:2020-11-30 22:51:55
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】25 ℃时,三种酸的电离平衡常数如下:
(1)下列四种离子结合H+的能力由大到小的顺序是_______ (填编号)
a.CO b.ClO- c.CH3COO- d.HCO
b.ClO- c.CH3COO- d.HCO
(2)下列反应不能发生的是:_______ (填编号)
a.CO + CH3COOH=CH3COO-+ CO2↑+ H2 O
+ CH3COOH=CH3COO-+ CO2↑+ H2 O
b.ClO-+ CH3COOH=CH3COO-+ HClO
c.CO + HClO=HCO
+ HClO=HCO + ClO-
+ ClO-
d.2ClO- + CO2 + H2O=CO + 2HClO
+ 2HClO
(3)用蒸馏水稀释0.10 mol·L-1 的醋酸,则下列各式表示的数值随水量的增加而增大 的是 _______(填编号)
(4)向20 mL硫酸和盐酸的混合溶液中,逐滴加入0.05 mol·L-1 Ba(OH)2 溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图所示。计算:

①原混合溶液中c(H+)=_______ ;c(Cl-)=_______
②A点的pH=_______
(5)25 ℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化的曲线是_______

(6)25 ℃时,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va_______ Vb(填“>”、“<”或“=”)
| 化学式 | CH3 COOH | H2 CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)下列四种离子结合H+的能力由大到小的顺序是
a.CO
 b.ClO- c.CH3COO- d.HCO
b.ClO- c.CH3COO- d.HCO
(2)下列反应不能发生的是:
a.CO
 + CH3COOH=CH3COO-+ CO2↑+ H2 O
+ CH3COOH=CH3COO-+ CO2↑+ H2 O b.ClO-+ CH3COOH=CH3COO-+ HClO
c.CO
 + HClO=HCO
+ HClO=HCO + ClO-
+ ClO-d.2ClO- + CO2 + H2O=CO
 + 2HClO
+ 2HClO(3)用蒸馏水稀释0.10 mol·L-1 的醋酸,则下列各式表示的数值随水量的增加而增大 的是 _______(填编号)
A. | B. | C. | D. |

①原混合溶液中c(H+)=
②A点的pH=
(5)25 ℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化的曲线是

(6)25 ℃时,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】 常用作食品添加剂;亚磷酸
常用作食品添加剂;亚磷酸 是二元弱酸,在工业上是制造塑料稳定剂的原料。回答下列问题:
是二元弱酸,在工业上是制造塑料稳定剂的原料。回答下列问题:
(1) 可作净水剂,其原理是
可作净水剂,其原理是_______ (用离子方程式说明)。
(2)浓度均为 的四种电解质溶液的
的四种电解质溶液的 随温度变化的曲线如图1所示:
随温度变化的曲线如图1所示:
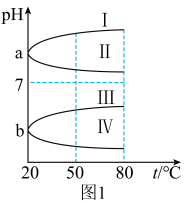
①其中符合 溶液的
溶液的 随温度变化的曲线是
随温度变化的曲线是_______ (填标号),导致 溶液的
溶液的 随温度变化的原因是
随温度变化的原因是_______ 。
② 时,
时,
 溶液中
溶液中
_______  (用含a或b的代数式表示)。
(用含a或b的代数式表示)。
(3)常温下,将 溶液滴加到亚磷酸溶液中,混合溶液的
溶液滴加到亚磷酸溶液中,混合溶液的 与离子浓度变化的关系如图2所示。
与离子浓度变化的关系如图2所示。
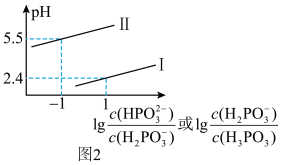
①则曲线_______ (填“I”或“II”)表示 与
与 的对应关系。
的对应关系。
②
_______ ,常温下, 溶液
溶液
_______ 7(填“|>”、“<”或“=”)。
 常用作食品添加剂;亚磷酸
常用作食品添加剂;亚磷酸 是二元弱酸,在工业上是制造塑料稳定剂的原料。回答下列问题:
是二元弱酸,在工业上是制造塑料稳定剂的原料。回答下列问题:(1)
 可作净水剂,其原理是
可作净水剂,其原理是(2)浓度均为
 的四种电解质溶液的
的四种电解质溶液的 随温度变化的曲线如图1所示:
随温度变化的曲线如图1所示:
①其中符合
 溶液的
溶液的 随温度变化的曲线是
随温度变化的曲线是 溶液的
溶液的 随温度变化的原因是
随温度变化的原因是②
 时,
时,
 溶液中
溶液中
 (用含a或b的代数式表示)。
(用含a或b的代数式表示)。(3)常温下,将
 溶液滴加到亚磷酸溶液中,混合溶液的
溶液滴加到亚磷酸溶液中,混合溶液的 与离子浓度变化的关系如图2所示。
与离子浓度变化的关系如图2所示。
①则曲线
 与
与 的对应关系。
的对应关系。②

 溶液
溶液
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】某小组对醋酸展开研究。已知:实验表明,在一定浓度的弱酸和对应的强碱盐组成的混合溶液中,外加少量强酸、强碱或稀释时,溶液的 基本不变。这种溶液叫缓冲溶液。1922年,Vanslyke提出,缓冲容量是衡量缓冲溶液缓冲能力大小的尺度。缓冲容量由缓冲溶液的总浓度(弱酸和弱酸钠之和)、缓冲比(弱酸与弱酸盐之比)决定。当缓冲比为
基本不变。这种溶液叫缓冲溶液。1922年,Vanslyke提出,缓冲容量是衡量缓冲溶液缓冲能力大小的尺度。缓冲容量由缓冲溶液的总浓度(弱酸和弱酸钠之和)、缓冲比(弱酸与弱酸盐之比)决定。当缓冲比为 时,缓冲容量最大。
时,缓冲容量最大。
(1)常温下,向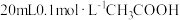 溶液滴加
溶液滴加 的
的 溶液至缓冲溶液的缓冲容量最大,此时
溶液至缓冲溶液的缓冲容量最大,此时 。
。
①在 和
和 组成的缓冲溶液中,加少量盐酸或少量
组成的缓冲溶液中,加少量盐酸或少量 ,具有缓冲能力(
,具有缓冲能力( 基本不变),其原因是加入少量酸被
基本不变),其原因是加入少量酸被 消耗,加少量碱被
消耗,加少量碱被_______ 消耗。
②常温下, 的电离常数
的电离常数
_______ (已知: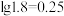 )。
)。
(2)用 计测定
计测定 时不同浓度的醋酸
时不同浓度的醋酸 ,数据如表所示。
,数据如表所示。
①根据表格中数据可知, 是弱酸,依据是
是弱酸,依据是_______ 。
②根据表格中数据可知,醋酸浓度越大,醋酸的电离度_______ (填“越大”“越小”或“不变”),举例说明:_______ 。
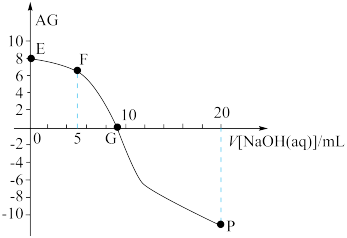
(3)常温下,在 醋酸溶液中滴加
醋酸溶液中滴加 溶液,溶液中
溶液,溶液中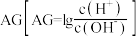 与已滴加
与已滴加 溶液体积的关系如图所示。
溶液体积的关系如图所示。
①常温下 的
的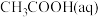 的电离度为
的电离度为_______ (提示:电离度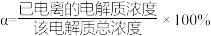 )。
)。
②G点溶液显_______ (填“酸”“碱”或“中”)性。
 基本不变。这种溶液叫缓冲溶液。1922年,Vanslyke提出,缓冲容量是衡量缓冲溶液缓冲能力大小的尺度。缓冲容量由缓冲溶液的总浓度(弱酸和弱酸钠之和)、缓冲比(弱酸与弱酸盐之比)决定。当缓冲比为
基本不变。这种溶液叫缓冲溶液。1922年,Vanslyke提出,缓冲容量是衡量缓冲溶液缓冲能力大小的尺度。缓冲容量由缓冲溶液的总浓度(弱酸和弱酸钠之和)、缓冲比(弱酸与弱酸盐之比)决定。当缓冲比为 时,缓冲容量最大。
时,缓冲容量最大。(1)常温下,向
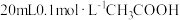 溶液滴加
溶液滴加 的
的 溶液至缓冲溶液的缓冲容量最大,此时
溶液至缓冲溶液的缓冲容量最大,此时 。
。①在
 和
和 组成的缓冲溶液中,加少量盐酸或少量
组成的缓冲溶液中,加少量盐酸或少量 ,具有缓冲能力(
,具有缓冲能力( 基本不变),其原因是加入少量酸被
基本不变),其原因是加入少量酸被 消耗,加少量碱被
消耗,加少量碱被②常温下,
 的电离常数
的电离常数
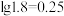 )。
)。(2)用
 计测定
计测定 时不同浓度的醋酸
时不同浓度的醋酸 ,数据如表所示。
,数据如表所示。 | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
 | 3.88 | 3.38 | 3.23 | 2.88 | 2.83 |
 是弱酸,依据是
是弱酸,依据是②根据表格中数据可知,醋酸浓度越大,醋酸的电离度
(3)常温下,在
 醋酸溶液中滴加
醋酸溶液中滴加 溶液,溶液中
溶液,溶液中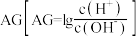 与已滴加
与已滴加 溶液体积的关系如图所示。
溶液体积的关系如图所示。
①常温下
 的
的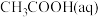 的电离度为
的电离度为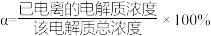 )。
)。②G点溶液显
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】运用溶液中离子平衡的相关知识,解决下列问题。
(1)含酚酞的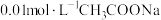 溶液显浅红色的原因为
溶液显浅红色的原因为_______ (用离子方程式)。
(2)室温下,用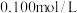 盐酸溶液滴定
盐酸溶液滴定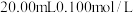 的某氨水溶液,滴定曲线如图所示。
的某氨水溶液,滴定曲线如图所示。
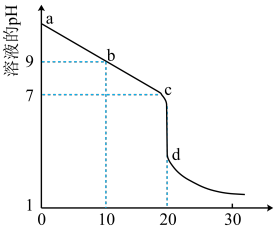
①d点所示的溶液中离子浓度由大到小的顺序依次为_______ 。
②b点所示的溶液中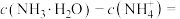
_______ (用溶液中的其它离子浓度表示)。
③ 的氨水与
的氨水与 的
的 溶液中,由水电离出的
溶液中,由水电离出的 之比为
之比为_______ 。
(3)已知 ,
, 。向含有
。向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中
沉淀生成时,溶液中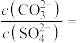
_______ (保留三位有效数字)。
我国国标推荐的食品药品中Ca元素含量的测定方法之一:利用 将处理后的样品中的
将处理后的样品中的 沉淀,过滤洗涤,然后将所得
沉淀,过滤洗涤,然后将所得 固体溶于过量的强酸,最后使用已知浓度的
固体溶于过量的强酸,最后使用已知浓度的 溶液通过滴定来测定溶液中
溶液通过滴定来测定溶液中 的含量。针对该实验中的滴定过程,回答以下问题:
的含量。针对该实验中的滴定过程,回答以下问题:
(4) 溶液应该用
溶液应该用_______ (填“酸式”或“碱式”)滴定管盛装。
(5)写出滴定过程中反应的离子方程式_______ 。
(6)滴定终点的现象:_______ 。
(7)以下哪些操作会导致测定的结果偏高_______ (填字母编号)。
a.装入 溶液前未润洗滴定管
溶液前未润洗滴定管
b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液
d.滴定过程中,振荡时将待测液洒出
(1)含酚酞的
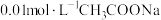 溶液显浅红色的原因为
溶液显浅红色的原因为(2)室温下,用
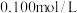 盐酸溶液滴定
盐酸溶液滴定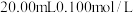 的某氨水溶液,滴定曲线如图所示。
的某氨水溶液,滴定曲线如图所示。
①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中
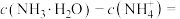
③
 的氨水与
的氨水与 的
的 溶液中,由水电离出的
溶液中,由水电离出的 之比为
之比为(3)已知
 ,
, 。向含有
。向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中
沉淀生成时,溶液中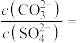
我国国标推荐的食品药品中Ca元素含量的测定方法之一:利用
 将处理后的样品中的
将处理后的样品中的 沉淀,过滤洗涤,然后将所得
沉淀,过滤洗涤,然后将所得 固体溶于过量的强酸,最后使用已知浓度的
固体溶于过量的强酸,最后使用已知浓度的 溶液通过滴定来测定溶液中
溶液通过滴定来测定溶液中 的含量。针对该实验中的滴定过程,回答以下问题:
的含量。针对该实验中的滴定过程,回答以下问题:(4)
 溶液应该用
溶液应该用(5)写出滴定过程中反应的离子方程式
(6)滴定终点的现象:
(7)以下哪些操作会导致测定的结果偏高
a.装入
 溶液前未润洗滴定管
溶液前未润洗滴定管b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液
d.滴定过程中,振荡时将待测液洒出
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】能源、材料和污染已成为当今科学研究的热点。请回答下列问题:
(1)Fe3O4又称磁性氧化铁,可作还原剂。配平下列化学方程式,并标出电子转移的方向与数目___ 。
________K2Cr2O7+________Fe3O4+________H2SO4→________Cr2(SO4)3+________Fe2(SO4)3+________K2SO4+________H2O
(2)新型铝—氧电池用于潜水艇动力源,其原理可以看作铝在强碱溶液中发生吸氧腐蚀。铝氧电池在使用过程中,铝电极发生___ 反应(填“氧化”“还原”),写出反应后铝元素的存在形式___ (写微粒符号)。
(3)二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要,完成下列填空:
①方法一:活性炭法2C(s)+2SO2(g) S2(g)+2CO2(g)
S2(g)+2CO2(g)
上述反应的化学平衡常数表达式为___ ;若在2L的密闭容器中进行上述反应,5min时容器中气体质量增加24g,则SO2的反应速率为___ ;为了加快吸收SO2,可采取的措施有___ 。
②方法二:氨水脱硫法该法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触吸收,一定温度下,往0.1mol/L氨水中加入少量NH4Cl固体,下列数值变小的是___
A. B.c(NH3·H2O) C.
B.c(NH3·H2O) C.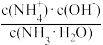 D.c(NH
D.c(NH )
)
③方法三:钠碱循环法
第一步是用Na2SO3水溶液吸收SO2,得到酸性的NaHSO3溶液;
第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
则在NaHSO3溶液中离子浓度关系正确的是___ 。
A.c(Na+)>c(HSO )>c(H+)>c(SO
)>c(H+)>c(SO )>c(OH-)
)>c(OH-)
B.c(Na+)=2c(SO )+c(HSO
)+c(HSO )
)
C.c(H2SO3)+c(H+)=c(SO )+c(OH-)
)+c(OH-)
D.c(Na+)+c(H+)=c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
(1)Fe3O4又称磁性氧化铁,可作还原剂。配平下列化学方程式,并标出电子转移的方向与数目
________K2Cr2O7+________Fe3O4+________H2SO4→________Cr2(SO4)3+________Fe2(SO4)3+________K2SO4+________H2O
(2)新型铝—氧电池用于潜水艇动力源,其原理可以看作铝在强碱溶液中发生吸氧腐蚀。铝氧电池在使用过程中,铝电极发生
(3)二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要,完成下列填空:
①方法一:活性炭法2C(s)+2SO2(g)
 S2(g)+2CO2(g)
S2(g)+2CO2(g)上述反应的化学平衡常数表达式为
②方法二:氨水脱硫法该法采用喷雾吸收法,雾化的氨水与烟气中的SO2直接接触吸收,一定温度下,往0.1mol/L氨水中加入少量NH4Cl固体,下列数值变小的是
A.
 B.c(NH3·H2O) C.
B.c(NH3·H2O) C.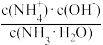 D.c(NH
D.c(NH )
)③方法三:钠碱循环法
第一步是用Na2SO3水溶液吸收SO2,得到酸性的NaHSO3溶液;
第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
则在NaHSO3溶液中离子浓度关系正确的是
A.c(Na+)>c(HSO
 )>c(H+)>c(SO
)>c(H+)>c(SO )>c(OH-)
)>c(OH-)B.c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )
)C.c(H2SO3)+c(H+)=c(SO
 )+c(OH-)
)+c(OH-)D.c(Na+)+c(H+)=c(SO
 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】直接排放含 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。
。
(1)在钠碱循环法中, 溶液作为吸收液,可由
溶液作为吸收液,可由 溶液吸收
溶液吸收 制得,该反应的离子反应方程式是
制得,该反应的离子反应方程式是________ 。
(2)吸收液 溶液)吸收
溶液)吸收 的过程中,
的过程中, 随
随 的变化如下表:
的变化如下表:
①由上表判断 溶液显
溶液显________ 性,用化学平衡原理解释:________ 。
②当吸收液呈中性时,溶液中离子浓度关系正确的是________ (填字母)。
A.
B.
C.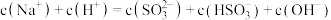
(3)电化学原理在工业生产中有重要的应用,用 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如下图所示。(电极材料为石墨)
,其原理如下图所示。(电极材料为石墨)

①图中a极要连接电源的(填“正”或“负”)___________ 极,C口流出的物质是___________ 。
② 放电的电极反应式为
放电的电极反应式为___________ 。
 的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的
的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的 。
。(1)在钠碱循环法中,
 溶液作为吸收液,可由
溶液作为吸收液,可由 溶液吸收
溶液吸收 制得,该反应的离子反应方程式是
制得,该反应的离子反应方程式是(2)吸收液
 溶液)吸收
溶液)吸收 的过程中,
的过程中, 随
随 的变化如下表:
的变化如下表: | 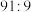 |  | 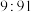 |
 | 8.2 | 7.2 | 6.2 |
 溶液显
溶液显②当吸收液呈中性时,溶液中离子浓度关系正确的是
A.

B.

C.
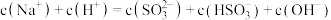
(3)电化学原理在工业生产中有重要的应用,用
 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如下图所示。(电极材料为石墨)
,其原理如下图所示。(电极材料为石墨)
①图中a极要连接电源的(填“正”或“负”)
②
 放电的电极反应式为
放电的电极反应式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.常温下,浓度均为0.1 mol/L的7种溶液pH如下:
请由上表数据回答:
(1)上述表中pH=12的Na2CO3溶液中水电离出的氢氧根离子浓度为:____________ mol/L
(2)pH=6.0的NaHSO3溶液中微粒浓度大小比较:_________________________
(3)NaHSO4溶液的电离方程式为:__________________________
(4)根据表中的数据分析,物质的量浓度均为0.1mol/L的Na2CO3、Na2SiO3、NaHCO3溶液中水的电离程度最大的是:_____________________________ (填化学式)
(5)用离子方程式说明Na2SO3溶液pH>7的原因______________________ 。
II.用含有CuO、SiO2和少量FeO·xFe2O3的废料制备无水CuCl2固体,工艺流程如下(部分操作和条件略):
a.向废料中加入过量稀盐酸,过滤:
b.向滤液中通入过量的氯气,再加入适当的物质调节溶液的pH约为3.2—4.7;过滤。
c.将滤液加热、浓缩、冷却、结晶、过滤,得到产品。
已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol·L-1
回答下列问题:
(6)步骤a过滤时用到的玻璃仪器是:________________________________
(7)步骤b中,通入过量氯气时的离子方程式:______________________
(8)步骤b中加入适当的物质可以是
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaHSO4 | NaClO |
| pH | 12 | 9.7 | 12.3 | 10.0 | 6.0 | 1.0 | 10.3 |
(1)上述表中pH=12的Na2CO3溶液中水电离出的氢氧根离子浓度为:
(2)pH=6.0的NaHSO3溶液中微粒浓度大小比较:
(3)NaHSO4溶液的电离方程式为:
(4)根据表中的数据分析,物质的量浓度均为0.1mol/L的Na2CO3、Na2SiO3、NaHCO3溶液中水的电离程度最大的是:
(5)用离子方程式说明Na2SO3溶液pH>7的原因
II.用含有CuO、SiO2和少量FeO·xFe2O3的废料制备无水CuCl2固体,工艺流程如下(部分操作和条件略):
a.向废料中加入过量稀盐酸,过滤:
b.向滤液中通入过量的氯气,再加入适当的物质调节溶液的pH约为3.2—4.7;过滤。
c.将滤液加热、浓缩、冷却、结晶、过滤,得到产品。
已知:生成氢氧化物沉淀的pH
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
回答下列问题:
(6)步骤a过滤时用到的玻璃仪器是:
(7)步骤b中,通入过量氯气时的离子方程式:
(8)步骤b中加入适当的物质可以是
| A.NaOH | B.Cu | C.CuO | D.Cu(OH)2 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的四种溶液:pH由小到大排列的顺序是______ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是____________________ (填字母)。
A.c(H+) B. C.c(H+)•c(OH﹣) D.
C.c(H+)•c(OH﹣) D.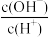 E.
E.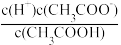
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:______________________ 。
(4)25℃时,将a mol/L的醋酸与等浓度的氢氧化钠等体积混合,反应后溶液中的离子浓度由大到小关系是______________________________ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol/L的四种溶液:pH由小到大排列的顺序是
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.c(H+) B.
 C.c(H+)•c(OH﹣) D.
C.c(H+)•c(OH﹣) D.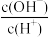 E.
E.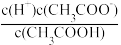
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将a mol/L的醋酸与等浓度的氢氧化钠等体积混合,反应后溶液中的离子浓度由大到小关系是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】根据要求,回答下列问题:
I.已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O H++Cl-+HClO、HClO
H++Cl-+HClO、HClO H++ClO-。
H++ClO-。
(1)要使氯水中的HClO浓度增大,可加入_______(填标号)。
(2)由此说明在实验室里可用排饱和食盐水法收集Cl2的理由是_______ 。
II.如表所示是几种弱酸常温下的电离平衡常数:
(3)CH3COOH、H2CO3、H2S、H3PO4四种酸的酸性由强到弱的顺序为_______ 。
(4)多元弱酸的第二步电离程度远小于第一步电离程度,其原因是_______ 。
(5)CH3COO-、 、
、 、S2-结合H+的能力由强到弱的顺序为
、S2-结合H+的能力由强到弱的顺序为_______ 。
I.已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O
 H++Cl-+HClO、HClO
H++Cl-+HClO、HClO H++ClO-。
H++ClO-。(1)要使氯水中的HClO浓度增大,可加入_______(填标号)。
| A.SO2 | B.NaHCO3 | C.HCl | D.NaOH |
II.如表所示是几种弱酸常温下的电离平衡常数:
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka1=7.5×10-3 Ka2=6.2×10-8 Ka3=2.2×10-13 |
(4)多元弱酸的第二步电离程度远小于第一步电离程度,其原因是
(5)CH3COO-、
 、
、 、S2-结合H+的能力由强到弱的顺序为
、S2-结合H+的能力由强到弱的顺序为
您最近半年使用:0次



