常温下,0.01 mol/L 的三种盐溶液 NaX、NaY、NaZ 的 pH 分别为 7、8、9,则下列比较中正确的是
| A.HX 是弱酸 | B.离子浓度:c(Z )>c(Y )>c(X ) |
| C.电离常数:KHZ)>KHY | D. c(X ) c(Y ) c(HY ) c(Z ) c(HZ) |
更新时间:2020-12-02 21:35:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.电离常数受溶液中电解质浓度的影响 |
| B.电离常数可以表示弱电解质的相对强弱 |
| C.电离常数大的酸溶液中c(H+)一定比电离常数小的酸溶液中的c(H+)大 |
D.H2CO3的电离常数表达式:K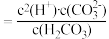 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关系正确的是
| A.将等物质的量的H2CO3和KHCO3溶于水配成的溶液中:2c(K+)= c(H2CO3)+c(HCO3-) |
B.向CH3COONa溶液里加入适量的NaOH固体后得到的混合溶液中: |
C.向0.10 mol·L-1NH4HSO4溶液中滴加适量的NaOH溶液至溶液呈中性,该中性溶液中: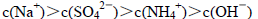 |
D.向NaCN溶液中滴加适量的稀盐酸使溶液呈中性,该中性溶液中: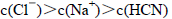 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,下列关系正确的是
| A.新制氯水中加入固体NaOH:c(Na+) = c(Cl−) + c(ClO−) + c(OH−) |
| B.pH = 8.3的NaHCO3溶液:c(Na+)>c(HCO3−)>c(CO32−)>c(H2CO3) |
| C.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:2c(H+) – 2c(OH−) = c(CH3COO−) – c(CH3COOH) |
| D.向硝酸银溶液中逐滴滴加物质的量浓度相等的氯化钾和铬酸钾的混合溶液,若先产生白色的氯化银沉淀,则有:Ksp(AgCl)<Ksp(Ag2CrO4) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,将CO2通入2L pH=12的KOH溶液中,溶液中水电离出的OHˉ离子浓度(c)与通入的CO2的体积(V)的关系如图所示.下列叙述不正确 的是 ( )
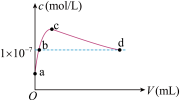

| A.a点溶液中:水电离出的c(H+)=1×10-12mol/L |
| B.b点溶液中:c(K+)>c(CO32 -)>c(HCO3- ) |
| C.c点溶液中: c(K+)=c(HCO3- )+c(CO32 -)+c(H2CO3) |
| D.d点溶液中: c(H+)=1×10-7mol/L |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
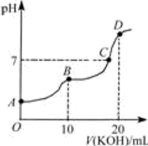
【推荐1】若用 表示溶液的酸度,其表达式为
表示溶液的酸度,其表达式为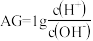 。
。 ,用
,用 的盐酸滴定
的盐酸滴定 溶液,滴定曲线如图所示。下列说法正确的是
溶液,滴定曲线如图所示。下列说法正确的是
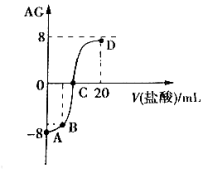
 表示溶液的酸度,其表达式为
表示溶液的酸度,其表达式为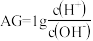 。
。 ,用
,用 的盐酸滴定
的盐酸滴定 溶液,滴定曲线如图所示。下列说法正确的是
溶液,滴定曲线如图所示。下列说法正确的是
A. 为强碱 为强碱 |
B.若B点加入的盐酸体积为 ,所得溶液中: ,所得溶液中: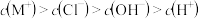 |
C.C点时加入盐酸的体积等于 |
D.滴定过程中从A点到D点溶液中水的电离程度: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,向10mL 0.1mol/L的H2C2O4溶液中逐滴加入0.1mol/LKOH溶液,所得滴定曲线如图所示.下列说法正确的是( )

| A.KHC2O4溶液呈弱碱性 |
B.B点时:c( )>c(K+)>c(H+)>c(OH﹣) )>c(K+)>c(H+)>c(OH﹣) |
C.C点时:c( )+c( )+c( )+c(H2C2O4)<c(K+)<c( )+c(H2C2O4)<c(K+)<c( )+2c( )+2c( )+c(H2C2O4) )+c(H2C2O4) |
D.D点时:c(H+)+c( )+c(H2C2O4)=c(OH﹣) )+c(H2C2O4)=c(OH﹣) |
您最近半年使用:0次

 和
和 的物种分布分数
的物种分布分数 (X)=
(X)=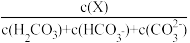 与pH的关系如图所示:
与pH的关系如图所示:
 )>c(NH
)>c(NH )
)

