一定温度下,在三个1L的恒容密闭容器中分别进行反应:2X(g)+Y(g)⇌Z(g),达到化学平衡状态时,相关数据如表。下列说法不正确 的是
| 实验 | 温度/K | 起始时各物质的浓度/(mol/L) | 平衡时物质的浓度/(mol/L) | ||
| c(X) | c(Y) | c(Z) | c(Z) | ||
| Ⅰ | 400 | 0.2 | 0.1 | 0 | 0.08 |
| Ⅱ | 400 | 0.4 | 0.2 | 0.2 | a |
| Ⅲ | 500 | 0.2 | 0.1 | 0 | 0.025 |
| A.达到化学平衡时,Ⅰ中X的转化率为80% |
| B.化学平衡常数:K(Ⅱ)=K(Ⅰ) |
| C.达到化学平衡所需要的时间:Ⅲ<Ⅰ |
| D.按Ⅱ中的起始浓度进行实验,反应逆向进行 |
20-21高二上·北京西城·期末 查看更多[9]
更新时间:2021-01-24 21:03:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业合成氨的反应为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.使用高效催化剂可减小ΔH |
| B.适当降温或加压,反应的平衡常数都增大 |
| C.及时将体系中的NH3液化分离有利于平衡正向移动 |
D.用E表示键能,则: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定条件下热解制取 :
: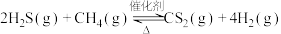 。已知其他条件不变时,温度对
。已知其他条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
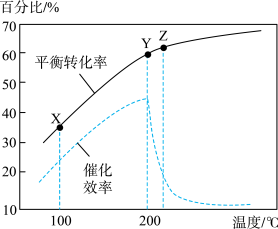
 :
: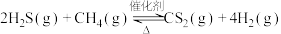 。已知其他条件不变时,温度对
。已知其他条件不变时,温度对 的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是
A.平衡常数: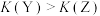 |
B.达到平衡所需时间: |
C.总能量: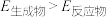 |
D.单位时间的转化率。: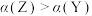 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在恒容密闭容器中,将温度控制在一定范围内发生如下反应,且达到化学平衡状态。
反应I:2NO(g)+2ICl(g) 2NOCl(g)+I2(g)K1
2NOCl(g)+I2(g)K1
反应II:2NOCl(g) 2NO(g)+Cl2(g)K2
2NO(g)+Cl2(g)K2
反应III:2ICl(g) Cl2g)+I2(g)K3
Cl2g)+I2(g)K3
反应I、II的平衡常数的对数(lgK)与温度的倒数( )之间关系如图所示。
)之间关系如图所示。
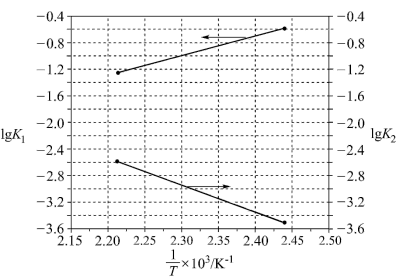
下列说法正确的是
反应I:2NO(g)+2ICl(g)
 2NOCl(g)+I2(g)K1
2NOCl(g)+I2(g)K1反应II:2NOCl(g)
 2NO(g)+Cl2(g)K2
2NO(g)+Cl2(g)K2反应III:2ICl(g)
 Cl2g)+I2(g)K3
Cl2g)+I2(g)K3反应I、II的平衡常数的对数(lgK)与温度的倒数(
 )之间关系如图所示。
)之间关系如图所示。
下列说法正确的是
| A.反应I的ΔH>0 |
B.反应Ⅲ的K3=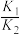 |
| C.升高温度,c(NOCl)增大 |
| D.升高温度,反应Ⅲ的平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】黄铁矿(主要成分FeS2)在空气中会被缓慢氧化,过程如图所示。下列说法正确的是

| A.发生反应a时,每0.2molFeS2被还原,转移2.8mole- |
B.25℃时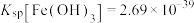 ,则该温度下d的逆反应平衡常数 ,则该温度下d的逆反应平衡常数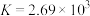 |
C.c发生反应的离子方程式为: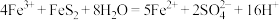 |
| D.黄铁矿是工业制备硫酸的必选原料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用活性炭还原氮氧化物,可防止空气污染。往一恒容密闭容器中加入一定量的活性炭和NO,某温度下发生反应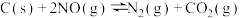 ,测得不同时间内各物质的物质的量数据如表所示:
,测得不同时间内各物质的物质的量数据如表所示:
下列说法错误的是
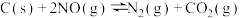 ,测得不同时间内各物质的物质的量数据如表所示:
,测得不同时间内各物质的物质的量数据如表所示:物质 物质的量/mol 时间/min | NO |  |  |
| 0 | 0.400 | 0 | 0 |
| 10 | 0.232 | 0.084 | 0.084 |
| 20 | 0.160 | 0.120 | 0.120 |
| 30 | 0.160 | 0.120 | 0.120 |
A.该反应的平衡常数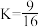 |
B.仅及时移除部分 ,可增大该反应的平衡常数 ,可增大该反应的平衡常数 |
| C.NO的转化率为60% |
| D.反应达平衡后,混合气体的平均相对分子质量为33.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在373K时,把0.5molN2O4气通入体积为5L的恒容真空密闭容器中立即出现红棕色,反应进行到2s时,NO2的浓度为0.02mol/L,在60s时体系达到平衡,此时容器内压强为开始压强的1.6倍。下列说法正确的是
| A.前2svN2O4=0.01mol/L·s |
| B.2s时体系内压强为开始时的1.1倍 |
| C.平衡时体系内含N2O40.25mol |
| D.平衡时若压缩容器体积可提高N2O4的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】甲醇脱氢可制取甲醛,反应原理为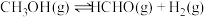 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是

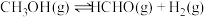 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
A.脱氢反应的 |
B.600K时,Y点: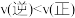 |
| C.要实现从Y点到Z点的变化可通过增大压强的方法 |
D.在 时,该反应的平衡常数为8.1 时,该反应的平衡常数为8.1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用CH4可消除NO2的污染,反应原理为:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
 N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是| 组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.组别①中0~20min内,NO2降解速率为0.25mol·L-1·min-l |
| B.由实验数据可知温度T1>T2 |
| C.40min时,表格中M对应的数据为0.15 |
| D.组别②中,20min时,CO2的浓度为0.32mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】利用CH4消除NO2污染,反应原理为CH4(g)+2NO2(g)⇌N2(g)+CO(g)+2H2O(g)。在10L密闭容器中,分别加入0.50molCH4和1.20molNO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是
| 组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.该反应在高温下才能自发进行 |
| B.T2温度下,若容器内的密度不变则该反应处于平衡状态 |
| C.可以利用40min时的数据,计算T2温度下的平衡常数K |
| D.高温下CH4消除NO2速率较快,所以温度越高越有利于消除NO2 |
您最近一年使用:0次

 4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是(
4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是(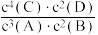
 、1molCO,发生反应
、1molCO,发生反应 ,反应10min达到平衡。该反应平衡常数随温度的变化如图所示,下列说法正确的是
,反应10min达到平衡。该反应平衡常数随温度的变化如图所示,下列说法正确的是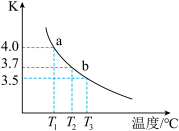

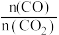 不变
不变


