某实验小组模拟研究汽车尾气的净化过程,一定温度下,在 的恒容密闭容器中加入等物质的量的
的恒容密闭容器中加入等物质的量的 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应:
 ,测得一定时间内
,测得一定时间内 和
和 物质的量变化如下表(
物质的量变化如下表( 后,只改变温度):
后,只改变温度):
下列说法正确的是
 的恒容密闭容器中加入等物质的量的
的恒容密闭容器中加入等物质的量的 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应:
 ,测得一定时间内
,测得一定时间内 和
和 物质的量变化如下表(
物质的量变化如下表( 后,只改变温度):
后,只改变温度):| 温度 | T1℃ | T2℃ | |||||
时间/ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
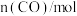 | 2.00 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
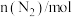 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
A.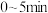 内,用 内,用 表示的平均反应速率为 表示的平均反应速率为 |
B. |
C.以CO表示的正反应速率,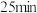 时大于 时大于 时 时 |
D.其他条件不变,改为1L容器, 时测得的 时测得的 一定小于 一定小于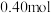 |
21-22高三上·浙江嘉兴·阶段练习 查看更多[6]
(已下线)2020年海南卷化学高考真题变式题1-8(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)山东省济宁市邹城第一中学2021-2022学年高二上学期10月月考化学试卷江西省南昌市南昌大学附属中学 2021-2022学年高二上学期第一次月考化学试卷浙江省嘉兴市2022届高三上学期9月基础测试化学试题
更新时间:2021-09-20 17:11:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入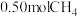 和
和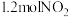 发生反应
发生反应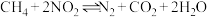 (反应物和产物均为气态)。测得
(反应物和产物均为气态)。测得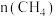 随时间变化的有关实验数据如下表。下列说法不正确的是
随时间变化的有关实验数据如下表。下列说法不正确的是
 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入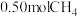 和
和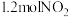 发生反应
发生反应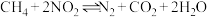 (反应物和产物均为气态)。测得
(反应物和产物均为气态)。测得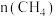 随时间变化的有关实验数据如下表。下列说法不正确的是
随时间变化的有关实验数据如下表。下列说法不正确的是| 组别 | 温度 | 时间/ | 0 | 10 | 20 | 40 | 50 |
| ① |  | 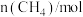 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② |  | 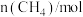 | 0.50 | 0.30 | 0.18 | a | 0.15 |
A.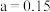 |
B. |
C. 温度下, 温度下,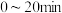 内 内 的反应速率为 的反应速率为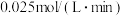 |
D. 温度下,平衡时 温度下,平衡时 的体积分数为 的体积分数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】现有分别为恒温条件和绝热条件的两个容器,体积均为 。都分别充入
。都分别充入 和
和 ,发生反应:
,发生反应: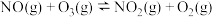 ,在相同起始温度下,经过一段时间后达到平衡。反应过程中
,在相同起始温度下,经过一段时间后达到平衡。反应过程中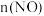 随时间变化的情况如表。
随时间变化的情况如表。
下列说法错误的是
 。都分别充入
。都分别充入 和
和 ,发生反应:
,发生反应: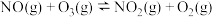 ,在相同起始温度下,经过一段时间后达到平衡。反应过程中
,在相同起始温度下,经过一段时间后达到平衡。反应过程中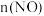 随时间变化的情况如表。
随时间变化的情况如表。时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | |
| 甲 |  | 4.0 | 3.0 | 2.2 | 1.6 | 1.2 | 0.8 | 0.6 | 0.6 | 0.6 |
| 乙 | 4.0 | 2.9 | 1.7 | 1.0 | 0.9 | 0.8 | 0.8 | 0.8 | 0.8 | |
A.该反应的 |
| B.乙容器为绝热容器 |
C.甲容器中用 表示 表示 内的平均反应速率为 内的平均反应速率为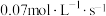 |
D.若在甲容器中充入的是 和 和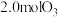 ,则平衡后得到 ,则平衡后得到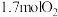 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在1L密闭容器中充入0.2molCl2和0.3molNO,不同温度下发生反应Cl2(g)+2NO(g) 2ClNO(g) ΔH<0,ClNO的体积分数随时间的变化如图所示。下列说法不正确的是
2ClNO(g) ΔH<0,ClNO的体积分数随时间的变化如图所示。下列说法不正确的是
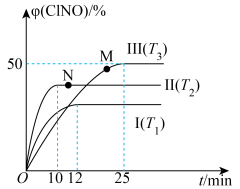
 2ClNO(g) ΔH<0,ClNO的体积分数随时间的变化如图所示。下列说法不正确的是
2ClNO(g) ΔH<0,ClNO的体积分数随时间的变化如图所示。下列说法不正确的是
| A.实验Ⅰ、Ⅱ、Ⅲ反应温度大小关系:T1>T2>T3 |
| B.实验Ⅱ相比实验Ⅰ、Ⅲ,除温度不同外还可能使用了催化剂 |
| C.NO和Cl2的物质的量之比保持不变时,反应达到平衡状态 |
| D.实验Ⅲ25min内用NO表示的反应速率为0.004mol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】往2 L密闭容器中充入NO2,在三种不同条件下发生反应:2NO2(g)  2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。
2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。
下列说法正确的是( )
 2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。
2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表(不考虑生成N2O4)。| 时间(min) 浓度 (mol·L-1) 实验序号/温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 |
| 实验1/800 | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
| 实验2/800 | 1.00 | 0.70 | 0.50 | 0.50 | 0.50 | 0.50 |
| 实验3/850 | 1.00 | 0.50 | 0.40 | 0.15 | 0.15 | 0.15 |
| A.实验2比实验1使用了效率更高的催化剂 |
| B.实验2比实验1的反应容器体积小 |
| C.由实验2和实验3可判断该反应是放热反应 |
| D.实验1比实验3的平衡常数大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用下列实验装置进行相应实验,能达到实验目的的是
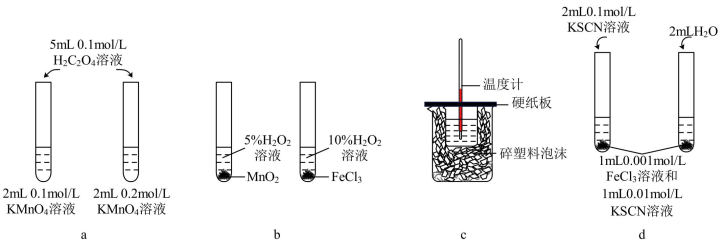

| A.在装置a中可依据褪色快慢比较浓度对反应速率的影响 |
| B.利用装置b探究不同催化剂对反应速率的影响 |
| C.利用装置c测定中和热 |
| D.利用装置d探究浓度对化学平衡的影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】相同温度下,甲、乙两个恒容密闭容器均进行反应:X(g)+Y(s) Z(g) △H<0。实验过程中部分数据如表所示。
Z(g) △H<0。实验过程中部分数据如表所示。
下列说法错误的是
 Z(g) △H<0。实验过程中部分数据如表所示。
Z(g) △H<0。实验过程中部分数据如表所示。| 容器 | 容积 | 物质的起始加入量 | 平衡时Z的物质的量 |
| 甲 | 2 | 1 molX、1 molY、0 molZ | 0.6mol |
| 乙 | 1 | 2 molX、2 molY、2 molZ | a |
| A.a=2.4 mol |
| B.乙中反应向正反应方向进行建立平衡 |
| C.甲中气体密度不再改变说明达到平衡状态 |
| D.平衡后缩小容器容积,甲、乙中X的体积分数均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 | 2molSO2、1molO2 |
| 平衡v正(SO2)/mol·L-1·s-1 | v1 | v2 | v3 |
| 平衡c(SO3)/mol·L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2<2c1 | B.K1>K3,p2>2p3 |
| C.v1<v3,α1(SO2)<α3(SO2) | D.c2>2c3,α2(SO3)+α3(SO2)<1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2-H2催化重整可获得CH3OH。其主要反应为
反应I: CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H1=-53.7kJ·mol-1
反应II:CO2(g) + H2(g)= CO(g) + H2O(g) △H2=+41kJ·mol-1
若仅考虑上述反应,在5.0 MPa、n始(CO2): n始(H2)=1:3时,原料按一定流速通过反应器,CO2的转化率和CH3OH的选择性随温度变化如图所示。CH3OH的选择性=

下列说法正确的是
反应I: CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H1=-53.7kJ·mol-1
反应II:CO2(g) + H2(g)= CO(g) + H2O(g) △H2=+41kJ·mol-1
若仅考虑上述反应,在5.0 MPa、n始(CO2): n始(H2)=1:3时,原料按一定流速通过反应器,CO2的转化率和CH3OH的选择性随温度变化如图所示。CH3OH的选择性=


下列说法正确的是
| A.其他条件不变,升高温度,CO2的平衡转化率增大 |
| B.其他条件不变,T>236℃时,曲线下降的可能原因是反应1正反应程度减弱 |
| C.一定温度下,增大n始(CO2):n始(H2)可提高CO2平衡转化率 |
| D.研发高温高效催化剂可提高平衡时CH3OH的选择性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验事实不能用平衡移动原理解释的是( )
A.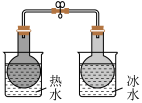 NO2球浸在热水和冰水中 NO2球浸在热水和冰水中 |
B.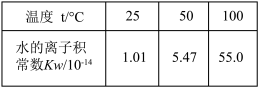 |
C.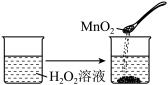 |
D.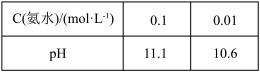 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知某可逆反应: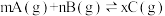 ,在密闭容器中进行,如图表示反应在不同温度T和压强P下,混合气体中B的百分含量(B%)与时间t的关系曲线,则下列正确的是
,在密闭容器中进行,如图表示反应在不同温度T和压强P下,混合气体中B的百分含量(B%)与时间t的关系曲线,则下列正确的是
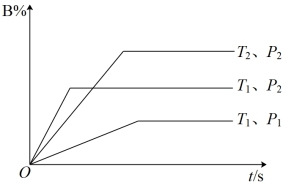
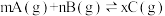 ,在密闭容器中进行,如图表示反应在不同温度T和压强P下,混合气体中B的百分含量(B%)与时间t的关系曲线,则下列正确的是
,在密闭容器中进行,如图表示反应在不同温度T和压强P下,混合气体中B的百分含量(B%)与时间t的关系曲线,则下列正确的是
A. , , , ,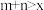 ,正反应放热 ,正反应放热 |
B. , , , ,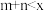 ,正反应吸热 ,正反应吸热 |
C. , , , ,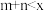 ,正反应吸热 ,正反应吸热 |
D. , , , ,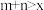 ,正反应吸热 ,正反应吸热 |
您最近一年使用:0次

 芳基羟胺在强酸水溶液作用下重排为氨基部分的反应机理如图:
芳基羟胺在强酸水溶液作用下重排为氨基部分的反应机理如图:
 的方程式为
的方程式为



