常温下,NaHA水溶液中H2A、HA-、A2-粒子的物质的量分数随pH(用NaOH和H2A调pH)的变化如图所示。下列说法错误的是


| A.曲线Ⅱ表示的是HA- |
| B.Ka1的数量级是10-2 |
| C.曲线Ⅱ和Ⅲ的交点处,微粒浓度满足关系式:c(H+)-c(OH-)=3c(A2-)-c(Na+) |
| D.NaHA溶液呈碱性 |
更新时间:2022-03-24 09:22:30
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸 |
| B.强电解质溶液的导电能力不一定比弱电解质溶液强 |
C.将NaOH溶液和氨水各稀释一倍,两者的OH- 浓度 均减小到原来的  |
D.物质的量相同的磷酸钠溶液和磷酸溶液中所含的PO 量相同 量相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】水体中重金属铅的污染问题备受关注。溶液中Pb2+及其与OH-形成的微粒的浓度分数α随溶液pH变化的关系如图所示。已知NH3·H2O的Kb=1.74×10-5。向Pb(NO3)2溶液中滴加氨水,关于该过程的说法正确的是


| A.Pb2+的浓度分数先减小后增大 |
B.c( )与c(Pb2+)的比值减小后增大,pH>10后不变 )与c(Pb2+)的比值减小后增大,pH>10后不变 |
| C.pH=7时,存在的阳离子仅有Pb2+、Pb(OH)+和H+ |
D.溶液中Pb2+与Pb(OH)2浓度相等时,氨主要以 的形式存在 的形式存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的一组是
①等体积等浓度的NaOH溶液中和相同浓度的盐酸和醋酸两溶液,两溶液消耗的体积一样多
②在500℃、20MPa条件下,在5L密闭容器中进行合成氨的反应,使用催化剂后K增大
③S(g)+O2(g)=SO2(g)可用该反应的△H表示燃烧热
④向醋酸钠溶液中加入醋酸使溶液的pH=7,此时混合液中c(Na+)>c(CH3COO-)
⑤CO(g)+2H2(g) CH3OH(g)△H=-90.7kJ/mol,将1molCO(g)和2molH2(g)充分反应,反应放出的能量小于90.7kJ
CH3OH(g)△H=-90.7kJ/mol,将1molCO(g)和2molH2(g)充分反应,反应放出的能量小于90.7kJ
⑥pH=3的盐酸与pH=3的醋酸溶液中,水电离的c(H+)相同
①等体积等浓度的NaOH溶液中和相同浓度的盐酸和醋酸两溶液,两溶液消耗的体积一样多
②在500℃、20MPa条件下,在5L密闭容器中进行合成氨的反应,使用催化剂后K增大
③S(g)+O2(g)=SO2(g)可用该反应的△H表示燃烧热
④向醋酸钠溶液中加入醋酸使溶液的pH=7,此时混合液中c(Na+)>c(CH3COO-)
⑤CO(g)+2H2(g)
 CH3OH(g)△H=-90.7kJ/mol,将1molCO(g)和2molH2(g)充分反应,反应放出的能量小于90.7kJ
CH3OH(g)△H=-90.7kJ/mol,将1molCO(g)和2molH2(g)充分反应,反应放出的能量小于90.7kJ⑥pH=3的盐酸与pH=3的醋酸溶液中,水电离的c(H+)相同
| A.②③⑥ | B.①③④ | C.①④⑥ | D.①⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.pH=6.8的溶液一定显酸性 |
B.相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH )由大到小的顺序是:①>②>③ )由大到小的顺序是:①>②>③ |
| C.电离平衡常数(K)只与弱电解质本身有关,与其它外部因素无关 |
| D.0.1 mol•L-1的硫化钠溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】向1L 0.3mol/L 的氢氧化钠溶液中通入二氧化碳,假设完全反应,下列说法错误的是( )
A.通入二氧化碳为 0.15mol 时,2c(Na+)=c(H2CO3)+c( )+c( )+c( ) ) |
B.通入二氧化碳为 0.15mol 时,c(Na+)>c( )>c(OH-)>c( )>c(OH-)>c( ) ) |
C.通入二氧化碳为 0.2mol 时,c(H+)+c(Na+)=c(OH-)+c( )+2c( )+2c( ) ) |
| D.向 A 选项反应后溶液中通入 0.3molHCl,加热,c(Na+)=c(Cl-)=0.3mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,下列叙述不正确的是 ( )
| A.25℃时pH=5的盐酸与pH=9的氨水中水的电离程度一定相同 |
B.pH=5的硫酸溶液稀释到原来的500倍,稀释后c(SO )与c(H+)之比约为1:10 )与c(H+)之比约为1:10 |
| C.0.1mol/L的Na2S溶液中粒子浓度关系:c(OH-)= c(HS-)+ c(H2S) +c(H+) |
| D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ· mol-1则含20.0g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.7kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】有25mL0.1mol•L-1的三种溶液①Na2CO3溶液;②CH3COONa溶液;③NaOH溶液,下列说法正确的是
| 电离平衡常数 | Ka1 | Ka2 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
| CH3COOH | 1.75×10-5 | —— |
| A.3种溶液pH的大小顺序是③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL0.1mol•L-1盐酸后,pH最大的是① |
| D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】联氨( )溶于水后是一种二元弱碱,在水中的电离方式与氨相似。25℃时,
)溶于水后是一种二元弱碱,在水中的电离方式与氨相似。25℃时,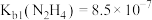 ,
,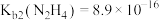 。下列说法错误的是
。下列说法错误的是
 )溶于水后是一种二元弱碱,在水中的电离方式与氨相似。25℃时,
)溶于水后是一种二元弱碱,在水中的电离方式与氨相似。25℃时,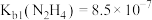 ,
,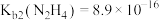 。下列说法错误的是
。下列说法错误的是A. 的 的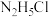 溶液呈酸性 溶液呈酸性 |
B. 的第二步电离方程式为 的第二步电离方程式为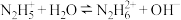 |
C. 与稀 与稀 中和生成的酸式盐的化学式为 中和生成的酸式盐的化学式为 |
D. 的稀溶液中存在 的稀溶液中存在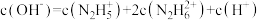 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据pH的计算方法,可定义 。常温下,向20mL0.1mol/L的氨水中滴加一定浓度的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示,下列说法正确的是
。常温下,向20mL0.1mol/L的氨水中滴加一定浓度的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示,下列说法正确的是

 。常温下,向20mL0.1mol/L的氨水中滴加一定浓度的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示,下列说法正确的是
。常温下,向20mL0.1mol/L的氨水中滴加一定浓度的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示,下列说法正确的是
| A.常温下,该稀硫酸的pH=2 |
| B.a点溶液中水电离产生的OH—的物质的量浓度为0.001mol/L |
C.c点对应溶液中存在 |
D.a、b、c三点对应 的水解平衡常数: 的水解平衡常数: |
您最近一年使用:0次

 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是 溶液中含有
溶液中含有
 溶液中
溶液中 的数目为
的数目为
 溶液中
溶液中 数目为
数目为 充分反应,产物的分子数小于
充分反应,产物的分子数小于


