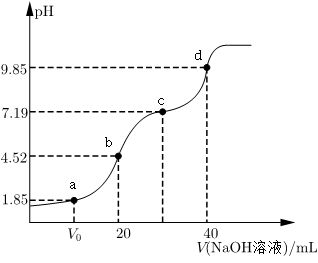
常温下,用0.1mol/L的NaOH溶液滴定20mL 0.1mol/L丙酮酸(CH3COCOOH)溶液,滴定过程中pH及电导率随加入NaOH溶液的体积变化曲线如图。下列说法正确的是
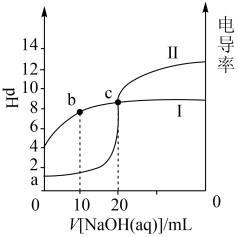

| A.水的电离程度:b>c |
| B.曲线Ⅱ为电导率曲线 |
C.b点溶液中: |
D.若a=1.7,则CH3COCOOH的电离常数Ka的数量级为10-2(已知 ) ) |
2022·湖南湘西·三模 查看更多[7]
河南省南阳市2022-2023学年高二下学期期末考试化学试题陕西省咸阳市2023届高三下学期模拟检测(二)理综化学试题(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)微专题41 水溶液中的三大守恒和浓度大小比较-备战2023年高考化学一轮复习考点微专题宁夏石嘴山市第三中学2022届高三第三次模拟考试理综化学试题(已下线)【直抵名校】04-备战2022年高考化学名校进阶模拟卷(通用版)湖南省湘西自治州2022届高三下学期4月第三次模拟考试化学试题
更新时间:2022-04-15 18:27:26
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各组离子在溶液中一定能大量共存的是( )
A.含有大量的[Al(OH)4]-的溶液:NH 、Na+、HCO 、Na+、HCO 、SO 、SO |
B.澄清透明的溶液中:MnO 、SO 、SO 、K+、H+ 、K+、H+ |
C.pH=11的溶液中:ClO-、Na+、SO 、I- 、I- |
D.水电离产生的c(H+)=1×10−14 mol·L−1的溶液中:HCO 、NH 、NH 、Cl-、Ca2+ 、Cl-、Ca2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在pH均为9的NaOH和CH3COONa两种溶液中,假设由水电离产生的OH- 离子浓度分别为Amol/L与Bmol/L,则A和B关系为:
| A.A>B | B.A=10-4B | C.B=10-4 A | D.A=B |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,下列溶液中的微粒一定能大量共存的是
A.c(Fe3+)=0.1mol•L-1的溶液:Al3+、SO 、SCN-、I- 、SCN-、I- |
B.常温下,由水电离的c(H+)•c(OH-)=1.0×10-26溶液中:K+、Na+、MnO 、Cl- 、Cl- |
C.无色透明的水溶液中:K+、Ba2+、Cl-、NO |
D.使石蕊试液变红的溶液:Al3+、NO 、Fe2+、Br- 、Fe2+、Br- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各溶液中,微粒的物质的量浓度关系表述正确的是
| A.0.1mol/LNa2CO3溶液中:c(Na+)=(HCO3-)+c(H2CO3)+2c(CO32-) |
| B.pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 |
| C.将0.2mol/LNaA溶液和0.1mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D.常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列溶液中有关微粒的物质的量浓度关系正确的是
| A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HRO3-)+2c(RO32-) |
| B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl﹣)>c(CH3COOH) |
| C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):①<③<② |
| D.等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数多少:N前>N后 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
A.常温下,0.5mol/LHB溶液和0.5mol/LNaOH溶液等体积混合后溶液的 ,则混合溶液中离子浓度的大小顺序为: ,则混合溶液中离子浓度的大小顺序为: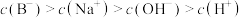 |
B.常温下,0.2mol/L的下列溶液① ,② ,② ,③ ,③ ,④ ,④ 中, 中, 由大到小的顺序是:②>①>④>③ 由大到小的顺序是:②>①>④>③ |
C.常温下0.1mol/LpH为3的NaHA溶液中: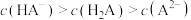 |
D.常温下,pH均为4的HF溶液和 溶液、pH均为10的氨水和 溶液、pH均为10的氨水和 溶液,四种溶液中由水电离的 溶液,四种溶液中由水电离的 相等 相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,下列说法正确的是
| A.0.1 mol/L的NaHA溶液pH=1,则有:c(Na+)=c(H2A)+c(HA-)+2c(A2-) |
| B.向NaAlO2溶液中逐滴加入稀盐酸至沉淀恰好消失时:c(Cl-)=3c(Al3+) |
C.将a mol/L的醋酸溶液与0.01 mol/L的氢氧化钠溶液等体积混合,溶液中:c(Na+)=c(CH3COO-),醋酸的电离常数Ka= (用含a的代数式表示) (用含a的代数式表示) |
D.向NH4Cl溶液中加入量等物质的量浓度的稀盐酸,则 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】乙二胺(H2NCH2CH2NH2)是二元弱碱,在溶液中的电离类似于氨,且分步电离。25℃时,乙二胺溶液中各含氮微粒的分布分数δ(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pOH[pOH=-lgc(OH-)]的变化曲线如图所示。下列说法错误的是


A.H2NCH2CH2NH2在水溶液中第二级电离方程式为:H2NCH2CH2NH +H2O⇌[H3NCH2CH2NH3]2++OH- +H2O⇌[H3NCH2CH2NH3]2++OH- |
| B.乙二胺一级电离平衡常数Kb1与二级电离平衡常数Kb2的比值为103 |
| C.向一定浓度的H2NCH2CH2NH2溶液中滴加稀盐酸,至B点时,溶液中的离子浓度关系:c(Cl-)+c(OH-)=3c([H3NCH2CH2NH3]2+)+c(H+) |
| D.将0.1mol/L 100 ml [H3NCH2CH2NH3]Cl2与0.1mol/L 100 mLH2NCH2CH2NH2混合,所得溶液呈酸性 |
您最近一年使用:0次