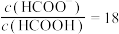常温时,向 溶液中逐滴加入
溶液中逐滴加入 的氨水,导电能力、pH与
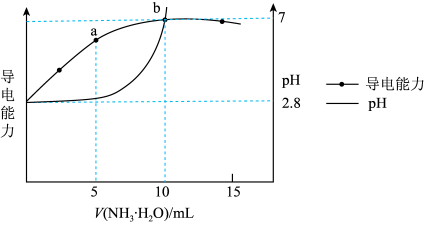
的氨水,导电能力、pH与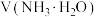 的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
 溶液中逐滴加入
溶液中逐滴加入 的氨水,导电能力、pH与
的氨水,导电能力、pH与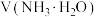 的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是
A.水的电离程度: |
B. ,该温度下的 ,该温度下的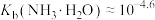 |
C.该温度下反应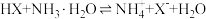 的平衡常数的数量级为 的平衡常数的数量级为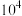 |
D.a点对应的溶液中存在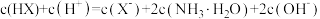 |
2022·云南·二模 查看更多[9]
云南省2022届高三第二次高中毕业生复习统一检测理科综合能力测试化学试题(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-2022年高考真题+模拟题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国乙卷高考变式题(选择题)福建省厦门双十中学2022届高三热身考化学试题湖南省株洲市天元区名校2022-2023学年高二上学期12月月考化学试题(已下线)学科特色3 电解质溶液图像福建省永春第一中学2023届高三下学期适应性考试(五)化学试题
更新时间:2022-04-22 20:42:54
|
相似题推荐
【推荐1】CO2催化加氢是碳中和的重要手段之一,以下是CO2加氢时发生的两个主要反应:
反应I:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH1=-165.0 kJ·mol-1
反应II:CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH2
在体积为VL的两个恒容密闭容器中,分别按表所示充入一定量的CO2和H2.平衡体系中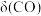 和
和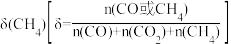 随温度变化关系如图所示。
随温度变化关系如图所示。
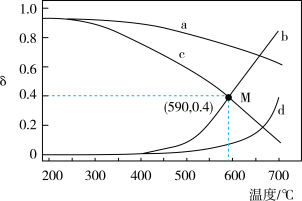
下列有关说法正确的是
反应I:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH1=-165.0 kJ·mol-1
反应II:CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH2
在体积为VL的两个恒容密闭容器中,分别按表所示充入一定量的CO2和H2.平衡体系中
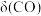 和
和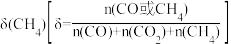 随温度变化关系如图所示。
随温度变化关系如图所示。| 容器 | 起始物质的量/mol | |
| CO2 | H2 | |
| 甲 | 0.1 | 0.3 |
| 乙 | 1 | 3 |

下列有关说法正确的是
| A.ΔH2<0 |
B.曲线b表示乙容器中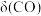 随温度的变化 随温度的变化 |
| C.M点对应H2的总转化率为66.7% |
D.590℃条件下反应10min,某容器中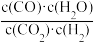 =2.4.此时,反应II的V正>V逆 =2.4.此时,反应II的V正>V逆 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在某催化剂作用下CO2和H2合成甲酸仅涉及以下反应:
I.CO2(g)+H2(g) HCOOH(g) △H1<0
HCOOH(g) △H1<0
II.CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
在2L刚性容器中,CO2(g)和H2(g)各投lmol发生反应,平衡时CO2的转化率及HCOOH和CO的选择性(产物的选择性:生成的HCOOH或CO与转化的CO2的比值)随温度变化如图所示。下列说法正确的是
I.CO2(g)+H2(g)
 HCOOH(g) △H1<0
HCOOH(g) △H1<0II.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2在2L刚性容器中,CO2(g)和H2(g)各投lmol发生反应,平衡时CO2的转化率及HCOOH和CO的选择性(产物的选择性:生成的HCOOH或CO与转化的CO2的比值)随温度变化如图所示。下列说法正确的是
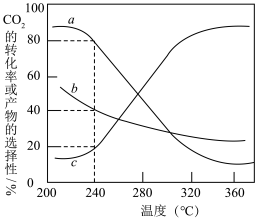
| A.△H2<0 |
| B.曲线b表示平衡时HCOOH的选择性 |
C.240℃时,反应I的平衡常数K=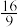 |
| D.在200℃~360℃之间,温度对反应I的影响要小于反应II |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,向一定浓度邻苯二甲酸钠( 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得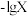 与
与 [X为
[X为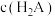 、
、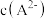 、
、 ;
;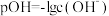 ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是
 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得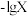 与
与 [X为
[X为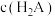 、
、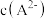 、
、 ;
;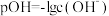 ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是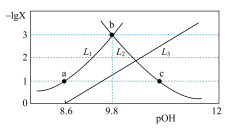
A.曲线 表示— 表示—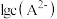 |
B.c点溶液中: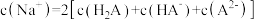 |
C.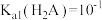 |
D.水的电离程度: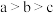 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】电位滴定法是靠电极电位的突跃来指示滴定终点。在滴定过程中,计算机对数据自动采集、处理,并利用滴定反应化学计量点前后电位突变的特性,自动寻找滴定终点。室温时,用 的
的 标准溶液滴定同浓度的
标准溶液滴定同浓度的 溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。下列说法错误的是
溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。下列说法错误的是

 的
的 标准溶液滴定同浓度的
标准溶液滴定同浓度的 溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。下列说法错误的是
溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出)。下列说法错误的是
A.滴定过程中,溶液中 逐渐减小 逐渐减小 |
B.a点溶液中: |
C.b点溶液中: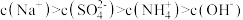 |
| D.a、b点水的电离程度:a>b |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
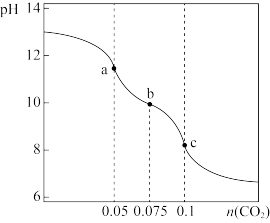
【推荐1】室温下,向V mL c mol/L的NaOH溶液中通入 气体,pH与通入气体的关系如图所示(设反应过程中溶液体积不变),下列说法错误的是
气体,pH与通入气体的关系如图所示(设反应过程中溶液体积不变),下列说法错误的是
 气体,pH与通入气体的关系如图所示(设反应过程中溶液体积不变),下列说法错误的是
气体,pH与通入气体的关系如图所示(设反应过程中溶液体积不变),下列说法错误的是
A.通入 的过程中,a、b、c三点水的电离程度 的过程中,a、b、c三点水的电离程度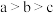 |
B.b点溶液中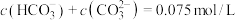 |
C.a点溶液中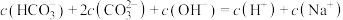 |
D.c点一定存在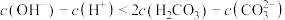 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,将浓度均为0.1mol/L 、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是
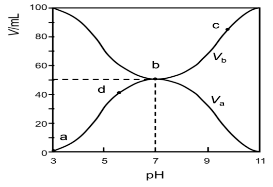

| A.b点,c(NH4+)+c(HX)=0.05mol/L |
B.c、d两点,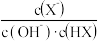 值相等 值相等 |
| C.Ka(HX)的值与Kb(NH3·H2O)的值相等 |
| D.a→d点过程中,存在c(X-)=c(NH4+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】以酚酞为指示剂,用0.1000 的NaOH溶液滴定20.00mL的二元酸
的NaOH溶液滴定20.00mL的二元酸 溶液。溶液中,pH、分布系数
溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积
随滴加NaOH溶液体积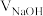 的变化关系如下图所示。
的变化关系如下图所示。
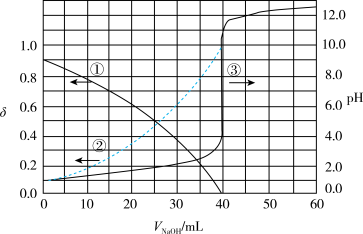
[比如 的分布系数:
的分布系数: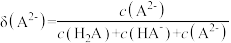 ]
]
下列叙述不正确的是
 的NaOH溶液滴定20.00mL的二元酸
的NaOH溶液滴定20.00mL的二元酸 溶液。溶液中,pH、分布系数
溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积
随滴加NaOH溶液体积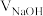 的变化关系如下图所示。
的变化关系如下图所示。
[比如
 的分布系数:
的分布系数: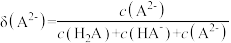 ]
]下列叙述不正确的是
A. 电离方程式可表示为 电离方程式可表示为 , , |
B. 溶液的浓度为0.1000 溶液的浓度为0.1000 |
C. 的电离常数 的电离常数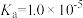 |
D.滴定终点时,溶液中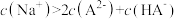 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下向 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是
 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是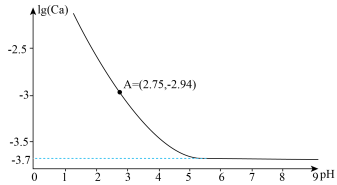
A.溶液中始终存在: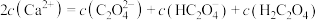 |
B.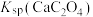 的数量级为 的数量级为 |
C.pH=7时,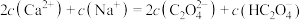 |
D.A点时,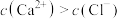 |
您最近一年使用:0次


 。若向体积均为1L的甲、乙两恒容容器中分别充入
。若向体积均为1L的甲、乙两恒容容器中分别充入 和
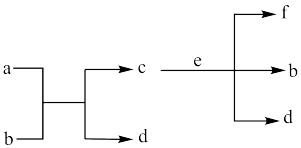
和 其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是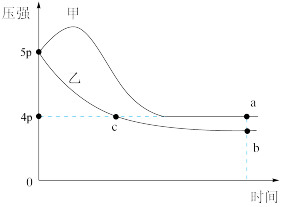

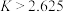







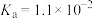
 、
、 、
、 、
、 结合质子的能力由大到小的顺序为
结合质子的能力由大到小的顺序为
 溶液中通入
溶液中通入 时不会反应生成
时不会反应生成 ,所得溶液的
,所得溶液的 ,则混合液中
,则混合液中