下列关于2SO2(g)+O2(g) 2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
 2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是| A.该反应的∆S>0 |
| B.根据∆G,高温条件下反应可以自发进行 |
| C.生产过程中将SO3分离出去,逆反应速率减慢 |
| D.其他条件不变,增大压强,平衡右移,平衡常数增大 |
更新时间:2022-09-21 15:00:47
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在一定温度下,将2 mol SO2和1 mol O2充入一定容积的密闭容器中,在催化剂作用下发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH=-197kJ/mol,下列说法中正确的是
2SO3(g) ΔH=-197kJ/mol,下列说法中正确的是
 2SO3(g) ΔH=-197kJ/mol,下列说法中正确的是
2SO3(g) ΔH=-197kJ/mol,下列说法中正确的是| A.为提高SO2转化率,可以再加入SO2 | B.平衡时放出197kJ热量 |
| C.平衡时再充入O2,则v正增大,v逆减小 | D.平衡时SO2的浓度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.将纯铁片放入稀硫酸中,反应缓慢,再加入少量硫酸铜溶液,可加快产生氢气的速率 |
| B.稀盐酸跟锌片反应,加入少量的氯化钠固体,反应速率不变 |
| C.反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
| D.用铁片和稀硫酸反应制取氢气时,改用98%的硫酸可加快产生氢气的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】对水样中M的分解速率的影响因素进行研究。在相同温度下,M的物质的量浓度 [c(M)]随时间(t) 变化的有关实验数据如下图所示,下列说法不正确 的是

| A.水样的PH越小,M的分解速率越快 |
| B.水样中添加Cu2+,能加快M的分解速率 |
| C.由②③得,反应物浓度越大,M的分解速率越快 |
| D.在0~20min内,②中M的平均分解速率为0.015mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在一个恒容密闭容器中通入一定量的A、B气体,在一定条件下发生反应: 。达到平衡后,只改变一个条件
。达到平衡后,只改变一个条件 ,下列物理量
,下列物理量 的变化一定符合图中曲线的
的变化一定符合图中曲线的
 。达到平衡后,只改变一个条件
。达到平衡后,只改变一个条件 ,下列物理量
,下列物理量 的变化一定符合图中曲线的
的变化一定符合图中曲线的| 选项 |  |  |  |
| A | 再通入A | B的转化率 | |
| B | 再通入C | A的体积分数 | |
| C | 通入氦气 | C的物质的量 | |
| D | 升高温度 | 混合气体的平均摩尔质量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实或现象不能用勒夏特列原理解释的是
| A.新制氯水中加入氢氧化钠浓溶液,颜色褪去 |
| B.Fe(SCN)3稀溶液中滴入几滴饱和氯化铁溶液,颜色变深 |
C.对反应“ ”,压缩反应容器体积,颜色变深 ”,压缩反应容器体积,颜色变深 |
| D.氨水应放置低温处密闭保存 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某密闭容器中,按物质的量之比1:1充入X、Y两种气体,发生反应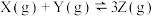
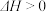 ,达到平衡后,下列有关说法正确的是
,达到平衡后,下列有关说法正确的是
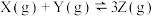
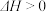 ,达到平衡后,下列有关说法正确的是
,达到平衡后,下列有关说法正确的是| A.继续通入少量物质的量之比为1:1的X、Y气体,保持容器容积不变,达到新平衡时,Z的体积分数增大 |
| B.其他条件不变,升高温度,正逆反应速率都增大,平衡时Z的体积分数比原平衡的体积分数大,平衡常数增大 |
| C.其他条件不变,将容积压缩至原来的一半,平衡逆向移动,平衡时X的体积分数比原平衡的体积分数大,平衡常数减小 |
| D.保持容器容积不变,增加Z的量,平衡逆向移动,平衡时Z的浓度比原平衡的小,体积分数比原平衡的体积分数小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将等量且物质的量相等的铁和水蒸气分别充入两个不同压强下的恒温密闭容器中,发生反应: ,物质的量n随时间t变化的曲线如图所示,下列说法正确的是
,物质的量n随时间t变化的曲线如图所示,下列说法正确的是

 ,物质的量n随时间t变化的曲线如图所示,下列说法正确的是
,物质的量n随时间t变化的曲线如图所示,下列说法正确的是
A. |
B. |
C.c点和d点的平衡常数: |
D.a、b、c、d四点混合气体的相对分子质量: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于化学反应的客观事实描述及其原理分析,均正确的是
| 选项 | 客观事实 | 原理分析 |
| A | 室温下将 与 与 混合,未见有 混合,未见有 生成 生成 | 室温下 |
| B | 室温下电解水,可得到 和 和 | 室温下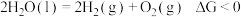 |
| C | 工业利用高温下反应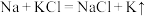 制备金属钾 制备金属钾 | 室温下金属性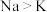 |
| D | 工业合成聚乙烯温度一般控制在 以下 以下 | 乙烯的加聚反应 ,过度升温不利 ,过度升温不利 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以下说法中正确的是
| A.所有∆H<0的反应均是自发反应 |
| B.高锰酸钾加热分解是一个熵减小的过程 |
| C.冰在室温下自动熔化成水,是熵增的过程 |
| D.自发进行的反应一定能迅速进行 |
您最近一年使用:0次



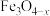 催化反应
催化反应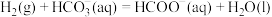 的部分机理如图所示。下列说法正确的是
的部分机理如图所示。下列说法正确的是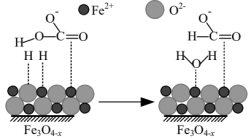


 表面的
表面的 与
与 中的羟基结合生成水
中的羟基结合生成水

