25℃时,HA的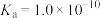 ,醋酸
,醋酸 ,下列说法正确的是
,下列说法正确的是
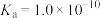 ,醋酸
,醋酸 ,下列说法正确的是
,下列说法正确的是A.相同温度下,等pH的NaA和 溶液中, 溶液中,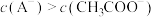 |
B.将浓度均为 的NaA和NaOH溶液加热,两种溶液的pH均变大 的NaA和NaOH溶液加热,两种溶液的pH均变大 |
C.25℃时, 的HA溶液中加少量NaA固体,水的电离程度变小 的HA溶液中加少量NaA固体,水的电离程度变小 |
D.25℃时,HA溶液与NaOH溶液混合,测得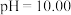 ,则此时溶液中 ,则此时溶液中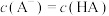 |
更新时间:2023-03-10 17:51:25
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知常温时HClO的 ,HF的
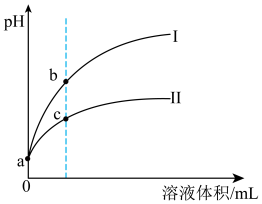
,HF的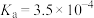 ,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
 ,HF的
,HF的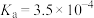 ,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
,现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是
| A.曲线Ⅰ为次氯酸稀释时pH变化曲线 |
| B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗次氯酸的体积较小 |
| C.a点时,若都加入相同大小的锌粒,此时与氢氟酸反应的速率大 |
| D.溶液中水的电离程度:a>b>c |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下,下列溶液呈酸性且能促进水的电离的是
| A.pH=4的HF溶液 | B.0.1 mol·L-1的KHSO4溶液 |
| C.0.1 mol·L-1的NH4NO3溶液 | D.0.1 mol·L-1的Na2CO3溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.常温下pH=2的HA溶液与pH=12的BOH等体积混合,溶液pH>7,则BOH为强碱 |
B.物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中, 前者大于后者 前者大于后者 |
| C.0.l mol•L-1 氨水的pH=a,加入适量的氯化铵固体可使溶液pH=a+l |
| D.相同温度下,pH 相等的氨水、CH3COONa 溶液中,水的电离程度相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时H2S的Ka1(H2S)=9×10-8,Ka2(H2S)=1.1×10-12。下列说法正确的是
| A.相同温度下,Na2S溶液pH值大于NaHS溶液 |
| B.常温下,将pH=6的H2S溶液稀释100倍,pH可能为8 |
C.往H2S溶液中滴入NaOH溶液的过程中, 一直减小 一直减小 |
| D.25℃时,等浓度Na2S和NaHS混合溶液,水电离出的氢氧根离子浓度为1.1×10-12mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
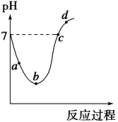
【推荐3】根据图象所得结论正确的是
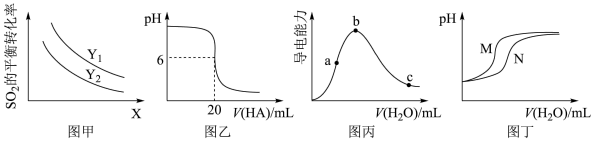

A.图甲是反应2SO2(g)+O2(g) 2SO3(g)ΔH<0中SO2的平衡转化率随温度、压强的变化曲线,说明X代表温度,Y代表压强,且Y1>Y2 2SO3(g)ΔH<0中SO2的平衡转化率随温度、压强的变化曲线,说明X代表温度,Y代表压强,且Y1>Y2 |
| B.图乙是室温下用0.1000mol•L-1的一元酸HA滴定20.00mL0.1000mol•L-1的一元碱BOH的滴定曲线,说明BOH是强碱 |
| C.图丙是室温下稀释冰醋酸时溶液的导电能力随加入水的体积的变化曲线,说明醋酸的电离程度:b>a>c |
| D.图丁是室温下稀释相同体积、相同pH的稀盐酸和稀醋酸时溶液的pH随加入水的体积的变化曲线,说明曲线N代表的是盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列物质在水溶液中的电离方程式正确的是( )
A.H2CO3 2H++CO32— 2H++CO32— | B.NaHSO4===Na++H++SO42— |
C.NaHCO3 Na++H++CO32— Na++H++CO32— | D.CH3COOH===H++CH3COO- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】25℃时,下列说法错误的是
A.室温下向10 mL 0. 1 mol/L的氨水中加水稀释后,溶液中 的值不变 的值不变 |
| B.欲证明HA为弱酸,可将pH=3的HA溶液稀释为原体积的10倍,若测得溶液pH=4,可证明HA为弱酸 |
| C.向H2S溶液中加入CuSO4溶液时, H2S电离平衡向右移动 |
| D.在1 mol· L-1(NH4)2S溶液中存在:c(NH3·H2O) +c(OH- )=c(HS-) +2c(H2S)+c(H+ ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】现有常温下的四份溶液,下列说法不正确的是
| 序号 | ① | ② | ③ | ④ |
| 溶液 | 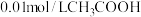 | 0.01mol/L HCl | pH=12 氨水 | pH=12 NaOH |
A.②④溶液中水电离的氢离子均为  |
| B.②③混合,若pH=7,则消耗溶液的体积②<③ |
C.①④等体积混合后,所得溶液中 |
| D.向③④中分别加入适量的氯化铵晶体后,两溶液的pH均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数δ(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法正确的是
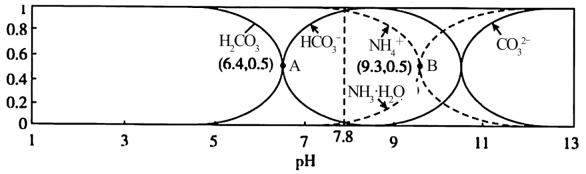

A.当溶液的pH=9时,溶液中存在下列关系:c(NH )>c(HCO )>c(HCO )>c(NH3·H2O)>c(CO )>c(NH3·H2O)>c(CO ) ) |
B.NH4HCO3溶液中存在下列守恒关系:c(NH )+c(NH3·H2O)+c(H+)=c(OH-)+2c(CO )+c(NH3·H2O)+c(H+)=c(OH-)+2c(CO )+c(H2CO3) )+c(H2CO3) |
C.往该溶液中逐滴滴加氢氧化钠时NH 和HCO 和HCO 的δ均逐渐减小 的δ均逐渐减小 |
| D.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3) |
您最近一年使用:0次


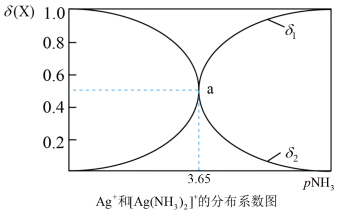
 [Ag(NH3)2]+。溶液中含银的两种微粒的物质的量分数δ(X)随pNH3的变化关系如图所示,其中
[Ag(NH3)2]+。溶液中含银的两种微粒的物质的量分数δ(X)随pNH3的变化关系如图所示,其中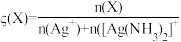 ,pNH3=-1g[c(NH3)]。下列说法正确的是
,pNH3=-1g[c(NH3)]。下列说法正确的是