常温下,向20mL0.1mol/LH2S溶液中缓慢加入少量MSO4粉末(已知MS难溶,忽略溶液体积变化),溶液中 与
与 的变化关系如图所示(坐标未按比例画出),已知:
的变化关系如图所示(坐标未按比例画出),已知:
 。下列有关说法正确的是( )
。下列有关说法正确的是( )
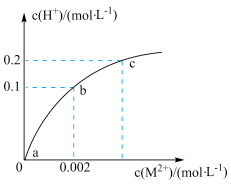
 与
与 的变化关系如图所示(坐标未按比例画出),已知:
的变化关系如图所示(坐标未按比例画出),已知:
 。下列有关说法正确的是( )
。下列有关说法正确的是( )
A.a点溶液叫 约为 约为 | B.a、b、c三点中由水电离的 最大的点是 最大的点是 点 点 |
C.b点溶液中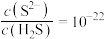 | D.c点溶液中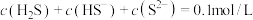 |
更新时间:2023-10-12 22:05:36
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】液氨与水性质相似,也存在微弱的电离:2NH3 NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
 NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
NH4++NH2—,其离子积常数K=c(NH4+)·c(NH2—)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是| A.液氨的电离平衡 | B.液氨的离子积常数 |
| C.c(NH4+) | D.c(NH2—) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】常温下,HF和CH3COOH的电离常数分别为1.8×10-4和1.8×10-5,将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示,下列说法正确的是
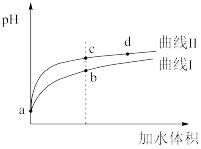

| A.溶液中水的电离程度:b点<c点 |
| B.酸的电离程度:c点>d点 |
| C.曲线II代表CH3COOH酸 |
| D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】常温下,二氯乙酸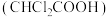 的电离常数为
的电离常数为 ,
, 。下列说法错误的是
。下列说法错误的是
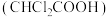 的电离常数为
的电离常数为 ,
, 。下列说法错误的是
。下列说法错误的是A.同浓度乙酸溶液的pH大于二氯乙酸溶液,则 的 的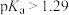 |
B.随温度升高 溶液的pH会减小,(在该温度范围内, 溶液的pH会减小,(在该温度范围内, 始终不逸出) 始终不逸出) |
C.加水稀释二氯乙酸溶液,溶液中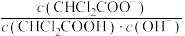 逐渐增大 逐渐增大 |
| D.二氟乙酸的酸性比二氯乙酸强的原因是氟的电负性比氯大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,0.1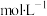 氨水pH=11,0.1
氨水pH=11,0.1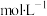 醋酸pH=3,下列说法正确的是
醋酸pH=3,下列说法正确的是
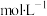 氨水pH=11,0.1
氨水pH=11,0.1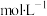 醋酸pH=3,下列说法正确的是
醋酸pH=3,下列说法正确的是A.将0.1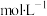 氨水稀释10倍,pH<10 氨水稀释10倍,pH<10 |
B.0.1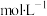 醋酸溶液中, 醋酸溶液中,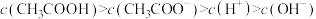 |
C.常温下, 的电离平衡常数与 的电离平衡常数与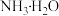 的相等 的相等 |
D. 溶液因水解呈酸性 溶液因水解呈酸性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列选项中不正确的是 

A.等物质的量浓度的下列溶液中 , , , , , ,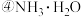 , , 由大到小的顺序是 由大到小的顺序是 |
B. 时, 时, 溶液 溶液 和 和 溶液 溶液 混合,若 混合,若 ,则混合溶液的pH一定小于7 ,则混合溶液的pH一定小于7 |
C.室温下,向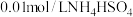 溶液中滴加NaOH溶液至中性: 溶液中滴加NaOH溶液至中性: |
D.对于反应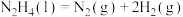 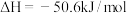 ,理论上在任何温度下都能自发进行 ,理论上在任何温度下都能自发进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】如果Fe3+、 、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是
、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是
 、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是
、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是| A.Na+ | B. | C. | D.Cl- |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】常温下, 某一元酸(
某一元酸( )溶液中
)溶液中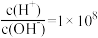 ,下列叙述
,下列叙述不正确 的是
 某一元酸(
某一元酸( )溶液中
)溶液中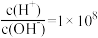 ,下列叙述
,下列叙述A.该溶液与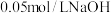 溶液等体积混合后: 溶液等体积混合后: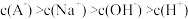 |
B.常温下 的电离平衡常数约为 的电离平衡常数约为 |
C.该溶液中水电离出的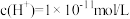 |
D.向该溶液中加入一定量水稀释,溶液中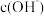 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】常温下,向20mL0.1mol/L氨水中逐滴加入0.1mol/L盐酸,测得溶液的pH随加入盐酸的体积变化如图所示。下列说法正确的是
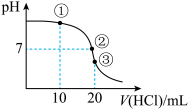

A.①溶液中:c(Cl-)=2c( )+2c(NH3·H2O) )+2c(NH3·H2O) |
B.②溶液中:c( )= c(Cl-)= c(OH-)= c(H+) )= c(Cl-)= c(OH-)= c(H+) |
C.③溶液中:c(H+)= c(OH-)+ c( )+c(NH3·H2O) )+c(NH3·H2O) |
D.滴定过程中可能出现:c(NH3·H2O)>c( )>c(OH-)>c(Cl-)>c(H+) )>c(OH-)>c(Cl-)>c(H+) |
您最近一年使用:0次

 )+2c(
)+2c( )+3c(
)+3c( )+ c(OH−)
)+ c(OH−)

