制备水煤气的反应C(s)+H2O(g)=H2(g)+CO(g) ΔH>0,下列说法正确的是
| A.升高温度,平衡逆向移动 |
| B.升高温度,反应速率增大 |
| C.恒温下,增大总压,H2O(g)的平衡转化率不变 |
| D.恒温恒压下,加入催化剂,平衡常数增大 |
更新时间:2023-11-01 19:51:55
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
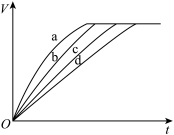
【推荐1】等质量的铁与过量的稀盐酸在不同的实验条件下反应,产生 的体积V与时间t的关系如图所示,则曲线a所对应的实验组别是
的体积V与时间t的关系如图所示,则曲线a所对应的实验组别是
 的体积V与时间t的关系如图所示,则曲线a所对应的实验组别是
的体积V与时间t的关系如图所示,则曲线a所对应的实验组别是
组别 |
| 温度/℃ | 铁的状态 |
A |
| 30 | 块状 |
B |
| 30 | 块状 |
C |
| 50 | 块状 |
D |
| 50 | 粉末状 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】NO和CO都是汽车尾气里的有害物质,它们能缓缓地反应生成N2和CO2,化学方程式为2NO+2CO N2+2CO2,对此反应,下列叙述错误的是( )
N2+2CO2,对此反应,下列叙述错误的是( )
 N2+2CO2,对此反应,下列叙述错误的是( )
N2+2CO2,对此反应,下列叙述错误的是( )| A.使用正催化剂能加大反应速率 |
| B.改变反应物的压强对反应速率产生影响 |
| C.冬天气温低,反应速率降低,对人体危害更大 |
| D.无论外界条件怎样改变,均对此化学反应的速率无影响 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】某温度下,反应H2(g)+I2(g)⇌2HI(g);△H>0.在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是
| A.恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B.恒压,充入HI(g),开始时正反应速率减小 |
| C.恒容,升高温度,正反应速率增大 |
| D.恒容,充入H2,I2(g)的体积分数降低 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列叙述中,不能用勒夏特列原理解释的是
| A.打开汽水瓶盖时有大量气泡冒出 |
B.装有 的密闭容器,加热后气体颜色变深 的密闭容器,加热后气体颜色变深 |
C.用排饱和食盐水方法收集 |
| D.加入催化剂有利于氨的合成 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐3】碳及其化合物在工农业生产中有着广泛的应用。工业上用CH4与H2O、CO2重整生产H2,CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g) CO(g)+3H2(g),下列说法正确的是
CO(g)+3H2(g),下列说法正确的是
 CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH=+161.1kJ·mol-1。CO是常见的还原剂,可用CH3COO[Cu(NH3)2]溶液吸收CO。CO2可以用于生产CH4、CH3OCH3等有机物,CO2还是侯氏制碱的原料。对于反应CH4(g)+H2O(g) CO(g)+3H2(g),下列说法正确的是
CO(g)+3H2(g),下列说法正确的是A.反应的平衡常数可表示为K= |
| B.1molCO和3molH2充分反应时放出的热量为161.1kJ |
| C.达平衡时缩小容器体积,正反应速率增大,逆反应速率减小 |
D.其他条件相同,增大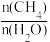 ,CH4的转化率下降 ,CH4的转化率下降 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】下列可逆反应达到平衡后,加压和升高温度均可使平衡向逆反应方向移动的是
| A.4NH3(g)+5O2(g) ⇌4NO(g)+6H2O(g) ΔH<0 |
| B.A2(g)+B2(g) ⇌2AB(g) ΔH<0 |
| C.W(g) ⇌Z(g) ΔH<0 |
| D.2SO3(g) ⇌2SO2(g)+O2(g) ΔH>0 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】压强变化不会使下列化学反应的平衡发生移动的是( )
A. | B. |
C. | D.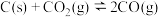 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】在某温度下,已知反应Ni(s)+H2O(g)  NiO(s)+H2(g)的平衡常数K=2.059,当水蒸气和氢气的物质的量浓度相等时,此反应
NiO(s)+H2(g)的平衡常数K=2.059,当水蒸气和氢气的物质的量浓度相等时,此反应
 NiO(s)+H2(g)的平衡常数K=2.059,当水蒸气和氢气的物质的量浓度相等时,此反应
NiO(s)+H2(g)的平衡常数K=2.059,当水蒸气和氢气的物质的量浓度相等时,此反应| A.已达平衡状态 | B.未达平衡状态,反应正向进行 |
| C.未达平衡状态,反应逆向进行 | D.无法确定 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】对于可逆反应2SO2+O2 2SO3,在一定温度下平衡常数为K,下列变化中,能使K发生变化的是
2SO3,在一定温度下平衡常数为K,下列变化中,能使K发生变化的是
| A.将SO2的浓度增大 | B.增大体系的压强 |
| C.使用合适的催化剂 | D.升高体系的温度 |
您最近一年使用:0次

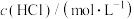


 ,反应过程能量变化如下图。下列说法
,反应过程能量变化如下图。下列说法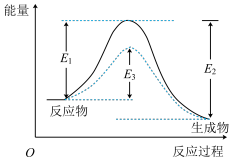
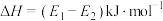
 下降为
下降为 ,反应速率增大
,反应速率增大 氧化成
氧化成 ,需要使用催化剂
,需要使用催化剂

