常温下,用0.1000mol/L的盐酸滴定20.00mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积VHCl的变化关系如图所示。[比如B+的分布系数:

下列叙述正确的是


下列叙述正确的是
| A.滴定时,可以选择酚酞作指示剂 |
| B.BOH的电离常数Kb=1.0×10−5 |
| C.滴定过程中,水的电离程度:n<m<p |
| D.p点溶液中,粒子浓度大小为c(Cl-)>c(B+)=c(BOH) |
2023高三·全国·专题练习 查看更多[1]
(已下线)电离 水解 溶解平衡图像
更新时间:2024-01-11 07:43:51
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在25℃时,将 1.0 L wmol/L CH3COOH 溶液与 0.1 mol NaOH固体混合,充分反应。然后向混合液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。 下列叙述正确的是

| A.a、b、c对应的混合液中,水的电离程度由大到小的顺序是c>a>b |
| B.b点混合液中 c(Na+) >c(CH3COO-) |
C.加入CH3COOH过程中, 增大 增大 |
D.25℃时,CH3COOH的电离平衡常数Ka= mol/L mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1盐酸,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加盐酸体积的关系如图所示,下列说法不正确的是( )


| A.常温下,Kb(NH3·H2O)约为1×10-5 |
| B.b=20.00 |
| C.R、Q两点对应溶液均呈中性 |
| D.R到N、N到Q所加盐酸体积不相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L—1NaOH溶液滴定20mL0.l mol·L—1H2A溶液的滴定曲线如右图所示(曲线上的数字为pH)。下列说法正确的是


| A.a点所得溶液中c(H2A)+c(A2—)+c(HA—)=0.1 mol·L—1 |
| B.b点所得溶液中:c(H2A)+2c(H+)=c(A2—)+2c(OH—) |
| C.对应溶液的电导率:a<b<c<d |
| D.对应溶液水的电离程度:a>b>c>d |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,向20ml,0.1mol·L-1CH3COOH溶液中滴加0.1mol·L-1的NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是


| A.c点表示CH3COOH和NaOH恰好反应完全 |
| B.a点表示的溶液中由水电离出的H+浓度为1.0×10-11mol·L-1 |
| C.b点表示的溶液中c(CH3COO-)>c(Na+) |
| D.b、d点表示的溶液中[c(CH3COO-)•c(H+)]/c(CH3COOH)相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,向二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示。下列有关说法错误的是


A.曲线M表示pH与lg 的变化关系 的变化关系 |
| B.Ka2(H2Y)的数量级为10-5 |
| C.d点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(K+) |
| D.交点e的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知:pKa=-lgKa,25℃时,H2XO3的pKa1=10-1.85,pKa2=10-7.19,常温下,用0.1mol/LNaOH溶液滴定20mL0.1mol/LH2XO3溶液的滴定曲线如图所示下列说法不正确的是
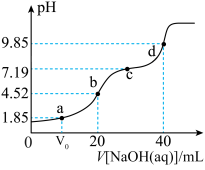

A.a点溶液中:c(H2XO3)=c(HXO ) ) |
B.b点溶液中:c(H2XO3)+c(H+)=c(XO )+c(OH-) )+c(OH-) |
C.c点溶液中:c(Na+)=3c(HXO ) ) |
D.d点溶液中:c(Na+)>c(XO )>c(OH-)>c(HXO )>c(OH-)>c(HXO )>c(H+) )>c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】在25℃时,下列溶液的pH或微粒的物质的量浓度关系正确的是
| A.将0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,则充分反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-) |
| B.某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度的大小关系一定是:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) |
| C.将pH=4的醋酸溶液与pH=10的KOH溶液等体积混合,则充分反应后的混合液:c(CH3COO-)>c(H+)>c(K+)>c(OH-) |
| D.某物质的溶液中由水电离出c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】甘氨酸 是人体必需氨基酸之一、在
是人体必需氨基酸之一、在 时,
时, 、
、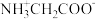 和
和 的分布分数【如
的分布分数【如 】与溶液
】与溶液 关系如图。下列说法错误的是
关系如图。下列说法错误的是

 是人体必需氨基酸之一、在
是人体必需氨基酸之一、在 时,
时, 、
、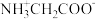 和
和 的分布分数【如
的分布分数【如 】与溶液
】与溶液 关系如图。下列说法错误的是
关系如图。下列说法错误的是
| A.甘氨酸具有两性 |
B.曲线c代表 |
C.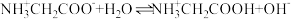 的平衡常数 的平衡常数 |
D. |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,保持某含少量 浊液的水体中
浊液的水体中 与空气中
与空气中 的平衡,调节水体pH,水体中
的平衡,调节水体pH,水体中 与pH的关系如图所示(其中X为
与pH的关系如图所示(其中X为 、
、 、
、 或
或 )。下列说法错误的是
)。下列说法错误的是

 浊液的水体中
浊液的水体中 与空气中
与空气中 的平衡,调节水体pH,水体中
的平衡,调节水体pH,水体中 与pH的关系如图所示(其中X为
与pH的关系如图所示(其中X为 、
、 、
、 或
或 )。下列说法错误的是
)。下列说法错误的是
A.曲线Ⅱ表示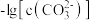 与pH的关系 与pH的关系 |
B.该温度下, 的电离常数 的电离常数 的数量级为 的数量级为 |
C.向水体中加入适量 固体,可使溶液由b点变到c点 固体,可使溶液由b点变到c点 |
D.a点的水体中: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知:①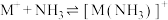

②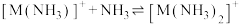

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是
{分布分数 }
}
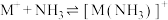

②
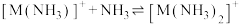

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是{分布分数
 }
}
A. |
B.曲线b代表 |
C.加水稀释,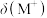 减小 减小 |
D.当 时, 时, 为含M粒子的主要存在形式 为含M粒子的主要存在形式 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,用0.01mol•L-1氨水滴定20mL浓度均为0.01mol•L-1的HCI和HCOOH混合溶液。相对导电能力随加入氨水体积的变化趋势如图所示。已知Ka(HCOOH)=1.8×10-4。下列有关叙述正确的是


| A.a点溶液的pH为1.7 |
B.b点溶液中:c(HCOO-)+c(Cl-)=c(NH ) ) |
C.c点溶液中:c(Cl-)>c(NH )>c(HCOO-) )>c(HCOO-) |
| D.滴定至pH=4-lg1.8时,HCOOH的电离度达到50% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】常温时,采用甲基橙和酚酞双指示剂,用盐酸滴定Na2CO3溶液,溶液中 lgc(H2CO3)、 lgc(HCO )、lgc(CO
)、lgc(CO )、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
 )、lgc(CO
)、lgc(CO )、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是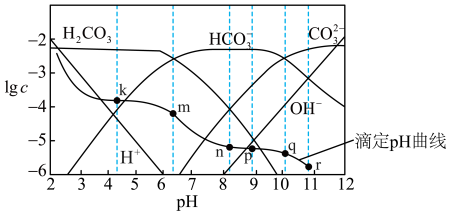
| A.整个滴定过程中可先用酚酞再用甲基橙作指示剂 |
| B.n点的pH为m点和q点pH的平均值 |
C.r点溶液中:c(OH-) = c(H+ )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.r点到 k 点对应的变化过程中,溶液中水的电离程度一直减小 |
您最近一年使用:0次



