利用软锰矿(主要成分是 ,其中还含有少量
,其中还含有少量 、MgO、CaO、
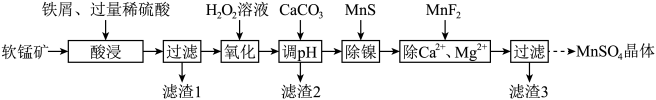
、MgO、CaO、 )生产高纯硫酸锰晶体的一种工艺流程如下:
)生产高纯硫酸锰晶体的一种工艺流程如下:
已知:常温下, ,
, ,
, ,
, 。
。
回答下列问题:
(1)“酸浸”前将矿石粉碎的目的是_______ ;“酸浸”后溶液中检测到 、
、 ,则此过程中铁屑与软锰矿反应的化学方程式为
,则此过程中铁屑与软锰矿反应的化学方程式为________ ;“滤渣1”的主要成分为________ (填化学式)。
(2)“氧化”时发生反应的离子方程式为___________ ,“调pH”的目的是___________ 。
(3)“除镍”时,使用MnS作为沉淀剂的原因是___________ 。
(4)加入 使
使 、
、 的浓度均不高于
的浓度均不高于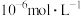 ,此时溶液中
,此时溶液中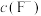 至少为
至少为_______  。
。
(5)硫酸锰的溶解度随温度变化关系如图所示,从“除 、
、 ”所得滤液中获得硫酸锰晶体的方法是
”所得滤液中获得硫酸锰晶体的方法是________ 。

 ,其中还含有少量
,其中还含有少量 、MgO、CaO、
、MgO、CaO、 )生产高纯硫酸锰晶体的一种工艺流程如下:
)生产高纯硫酸锰晶体的一种工艺流程如下:
已知:常温下,
 ,
, ,
, ,
, 。
。回答下列问题:
(1)“酸浸”前将矿石粉碎的目的是
 、
、 ,则此过程中铁屑与软锰矿反应的化学方程式为
,则此过程中铁屑与软锰矿反应的化学方程式为(2)“氧化”时发生反应的离子方程式为
(3)“除镍”时,使用MnS作为沉淀剂的原因是
(4)加入
 使
使 、
、 的浓度均不高于
的浓度均不高于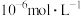 ,此时溶液中
,此时溶液中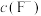 至少为
至少为 。
。(5)硫酸锰的溶解度随温度变化关系如图所示,从“除
 、
、 ”所得滤液中获得硫酸锰晶体的方法是
”所得滤液中获得硫酸锰晶体的方法是
23-24高三上·辽宁朝阳·期末 查看更多[3]
更新时间:2024-01-22 14:30:59
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
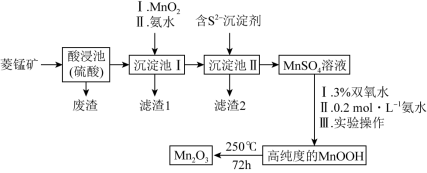
【推荐1】Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图:
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为_______ 价。
(2)向“沉淀池I”中加入MnO2,MnO2的作用是_______ ,在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为_______ (当溶液中某离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为_______ 。
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。_______ 。
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为_______ g•cm-3(列出计算式即可)。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池I”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。
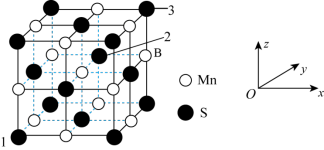
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO等)制备草酸镍晶体的流程如下:
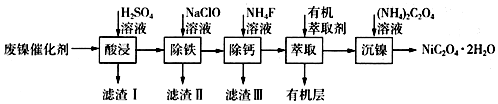
(1)请写出一种能提高“酸浸”速率的措施:___________________________________ ;滤渣I的成分是CaSO4和____________________ (填化学式)。
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH的关系如图所示:
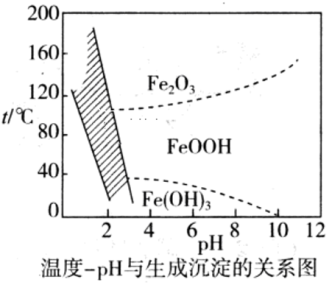
①若控制温度40℃、pH=8,则滤渣II的主要成分为___________ (填化学式)。
②若控制温度80℃、pH=2,可得到黄铁矾钠[Na2Fe6(SO4)4(OH)12]沉淀(图中阴影部分),写出生成黄铁矾钠的离子方程式:___________________________________________ 。
(3)已知除铁后所得100 mL溶液中c(Ca2+)=0.01mol·L-1,加入100 mL NH4F溶液,使Ca2+恰好沉淀完全即溶液中c(Ca2+)=1×10-5 mol·L-1,则所加c(NH4F)=_______ mol·L-1。[已知Ksp(CaF2)=5.29×10-9]
(4)加入有机萃取剂的作用是________________________ 。

(1)请写出一种能提高“酸浸”速率的措施:
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH的关系如图所示:

①若控制温度40℃、pH=8,则滤渣II的主要成分为
②若控制温度80℃、pH=2,可得到黄铁矾钠[Na2Fe6(SO4)4(OH)12]沉淀(图中阴影部分),写出生成黄铁矾钠的离子方程式:
(3)已知除铁后所得100 mL溶液中c(Ca2+)=0.01mol·L-1,加入100 mL NH4F溶液,使Ca2+恰好沉淀完全即溶液中c(Ca2+)=1×10-5 mol·L-1,则所加c(NH4F)=
(4)加入有机萃取剂的作用是
您最近一年使用:0次
【推荐3】以菱锌矿(主要含有 ,另含有少量
,另含有少量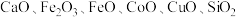 等)为原料电解制
等)为原料电解制 的流程如图:
的流程如图:
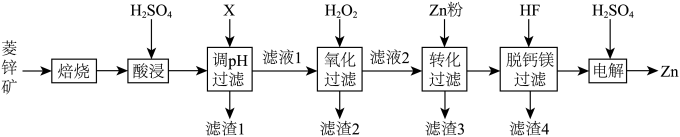
相关难溶物溶度积常数如下表:
(1)“酸浸”时为提高锌的浸出率,可采取的措施有_______ (写出一种即可)。
(2)“调 过滤”中,物质X最适宜选择
过滤”中,物质X最适宜选择_______ (填标号)。
A. B.
B. C.
C.
(3)“氧化过滤”中, 转化为
转化为 的离子方程式为
的离子方程式为_______ 。若反应结束时,溶液 为5,则残留的
为5,则残留的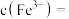
_______  。
。
(4)“转化过滤”中,除去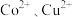 速率先慢后快的原因是
速率先慢后快的原因是_______ 。
(5)“脱钙镁过滤”后,溶液中
_______ 。
(6)“电解”装置示意如图。
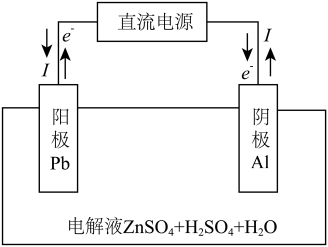
①开始通电时,阳极表面形成 ,保护阳极不被酸性电解液腐蚀,相应的电极反应式为
,保护阳极不被酸性电解液腐蚀,相应的电极反应式为_______ 。
②电解过程中,电解液中 含量应维持在
含量应维持在 ,
, 含量不宜过高的原因是
含量不宜过高的原因是_______ 。
 ,另含有少量
,另含有少量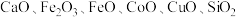 等)为原料电解制
等)为原料电解制 的流程如图:
的流程如图:
相关难溶物溶度积常数如下表:
| 物质 |  |  |  |  |
 | 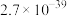 | 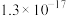 |  |  |
(1)“酸浸”时为提高锌的浸出率,可采取的措施有
(2)“调
 过滤”中,物质X最适宜选择
过滤”中,物质X最适宜选择A.
 B.
B. C.
C.
(3)“氧化过滤”中,
 转化为
转化为 的离子方程式为
的离子方程式为 为5,则残留的
为5,则残留的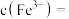
 。
。(4)“转化过滤”中,除去
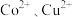 速率先慢后快的原因是
速率先慢后快的原因是(5)“脱钙镁过滤”后,溶液中

(6)“电解”装置示意如图。

①开始通电时,阳极表面形成
 ,保护阳极不被酸性电解液腐蚀,相应的电极反应式为
,保护阳极不被酸性电解液腐蚀,相应的电极反应式为②电解过程中,电解液中
 含量应维持在
含量应维持在 ,
, 含量不宜过高的原因是
含量不宜过高的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】 广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备
广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备 的工艺流程如下:
的工艺流程如下:
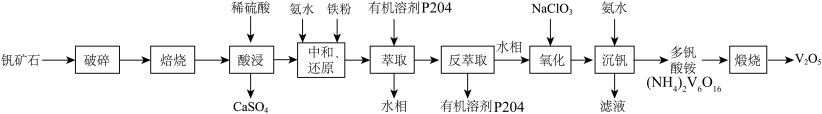
已知:ⅰ.“焙烧”后,固体中主要含有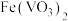 、
、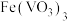 、
、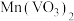 、
、 ;“酸浸”后钒以
;“酸浸”后钒以 形式存在,“中和、还原”后钒以
形式存在,“中和、还原”后钒以 形式存在。
形式存在。
ⅱ.有机溶剂P204对四价钒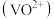 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 。
。
ⅲ.多钒酸铵微溶于冷水,易溶于热水。
ⅳ.该工艺条件下,溶液中金属离子(浓度均为 )开始沉淀和完全沉淀的pH如下表所示:
)开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“破碎”的目的是______ 。
(2)“中和、还原”时, 参与反应的离子方程式为
参与反应的离子方程式为______ 。
(3)钒的浸出率与焙烧温度、硫酸加入量的关系如图1、2所示,适宜的工艺条件为______ 。洗涤多钒酸铵时要用冰水洗涤,目的是______ 。
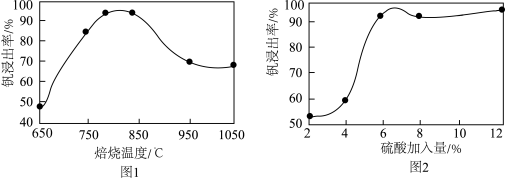
(4)“氧化”时,每消耗 (本身被还原为
(本身被还原为 ),可得到
),可得到
______ mol。
(5)流程中可循环使用的物质有______ 。
(6)“萃取”分离后,所得“水相”中含有丰富的金属资源,经三道工序可回收 溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂:
溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂: 溶液、
溶液、 、
、 溶液、
溶液、 溶液)
溶液)______ 。
 广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备
广泛用于冶金、化工等行业,主要用于冶炼钒铁。以钒矿石为原料制备 的工艺流程如下:
的工艺流程如下:
已知:ⅰ.“焙烧”后,固体中主要含有
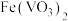 、
、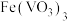 、
、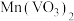 、
、 ;“酸浸”后钒以
;“酸浸”后钒以 形式存在,“中和、还原”后钒以
形式存在,“中和、还原”后钒以 形式存在。
形式存在。ⅱ.有机溶剂P204对四价钒
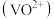 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 。
。ⅲ.多钒酸铵微溶于冷水,易溶于热水。
ⅳ.该工艺条件下,溶液中金属离子(浓度均为
 )开始沉淀和完全沉淀的pH如下表所示:
)开始沉淀和完全沉淀的pH如下表所示:| 金属离子 |  |  |  |  |
| 开始沉淀pH | 1.9 | 7.0 | 11.9 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 13.9 | 10.1 |
(1)“破碎”的目的是
(2)“中和、还原”时,
 参与反应的离子方程式为
参与反应的离子方程式为(3)钒的浸出率与焙烧温度、硫酸加入量的关系如图1、2所示,适宜的工艺条件为

(4)“氧化”时,每消耗
 (本身被还原为
(本身被还原为 ),可得到
),可得到
(5)流程中可循环使用的物质有
(6)“萃取”分离后,所得“水相”中含有丰富的金属资源,经三道工序可回收
 溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂:
溶液。请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂: 溶液、
溶液、 、
、 溶液、
溶液、 溶液)
溶液)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】分银渣是电解铜的阳极泥提取贵金属后的尾渣,含有铅( )、钡(
)、钡( )、锡(
)、锡( )以及金(Au)、银(Ag)等贵重金属,具有较高的综合利用价值。一种提取流程如下。
)以及金(Au)、银(Ag)等贵重金属,具有较高的综合利用价值。一种提取流程如下。
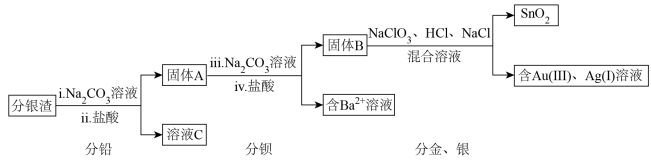
已知:1. 不溶于水、醇、稀酸和碱液。
不溶于水、醇、稀酸和碱液。
2.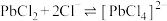 ;
; 。
。
3.部分难溶电解质的溶度积(25℃)如表。
(1)写出步骤ⅰ的主反应的离子方程式并说明该反应能够发生的原因___________ 。
(2)结合化学用语推测步骤ⅱ的作用是___________ 。
(3)依据流程,下列说法正确的是___________ 。
a.步骤ⅰ中 用量越多越好
用量越多越好
b.步骤ⅲ发生的反应为: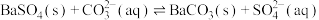
c.固体A需用饱和 溶液循环多次进行洗涤
溶液循环多次进行洗涤
(4)固体B在混合溶液中同步浸出Au、Ag生成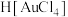 和
和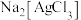 ,化学方程式分别为:①
,化学方程式分别为:①___________ ;②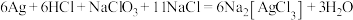 。
。
(5)用锌粉可将 中的Au以单质形式置换出来。若将
中的Au以单质形式置换出来。若将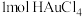 完全还原,则参加反应的Zn的物质的量是
完全还原,则参加反应的Zn的物质的量是___________  。
。
(6)工业上采用碘酸钾滴定法测定 中Sn元素的含量,其方法为:将
中Sn元素的含量,其方法为:将 样品灰化后用
样品灰化后用 熔融,将熔融物酸溶后,再用还原铁粉将
熔融,将熔融物酸溶后,再用还原铁粉将 转化为
转化为 ,加入指示剂,用
,加入指示剂,用 标准溶液进行滴定,滴定反应离子方程式为(均未配平):
标准溶液进行滴定,滴定反应离子方程式为(均未配平):
ⅰ.
ⅱ.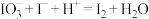
①该滴定反应达到滴定终点的现象为___________ 。
②称取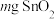 样品,用上述方法滴定,若滴定终点时消耗
样品,用上述方法滴定,若滴定终点时消耗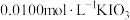 标准溶液
标准溶液 ,则测得
,则测得 纯度为
纯度为___________ %。
 )、钡(
)、钡( )、锡(
)、锡( )以及金(Au)、银(Ag)等贵重金属,具有较高的综合利用价值。一种提取流程如下。
)以及金(Au)、银(Ag)等贵重金属,具有较高的综合利用价值。一种提取流程如下。
已知:1.
 不溶于水、醇、稀酸和碱液。
不溶于水、醇、稀酸和碱液。2.
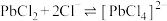 ;
; 。
。3.部分难溶电解质的溶度积(25℃)如表。
| 物质 |  |  |  |  |  |
 | 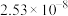 | 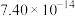 | 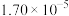 |  | 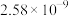 |
(2)结合化学用语推测步骤ⅱ的作用是
(3)依据流程,下列说法正确的是
a.步骤ⅰ中
 用量越多越好
用量越多越好b.步骤ⅲ发生的反应为:
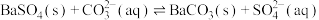
c.固体A需用饱和
 溶液循环多次进行洗涤
溶液循环多次进行洗涤(4)固体B在混合溶液中同步浸出Au、Ag生成
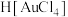 和
和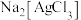 ,化学方程式分别为:①
,化学方程式分别为:①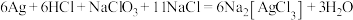 。
。(5)用锌粉可将
 中的Au以单质形式置换出来。若将
中的Au以单质形式置换出来。若将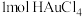 完全还原,则参加反应的Zn的物质的量是
完全还原,则参加反应的Zn的物质的量是 。
。(6)工业上采用碘酸钾滴定法测定
 中Sn元素的含量,其方法为:将
中Sn元素的含量,其方法为:将 样品灰化后用
样品灰化后用 熔融,将熔融物酸溶后,再用还原铁粉将
熔融,将熔融物酸溶后,再用还原铁粉将 转化为
转化为 ,加入指示剂,用
,加入指示剂,用 标准溶液进行滴定,滴定反应离子方程式为(均未配平):
标准溶液进行滴定,滴定反应离子方程式为(均未配平):ⅰ.

ⅱ.
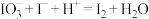
①该滴定反应达到滴定终点的现象为
②称取
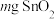 样品,用上述方法滴定,若滴定终点时消耗
样品,用上述方法滴定,若滴定终点时消耗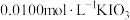 标准溶液
标准溶液 ,则测得
,则测得 纯度为
纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】氧化亚钴(CoO)通常作为生产硬质合金、超耐热合金、绝缘材料和磁性材料的主要原料以及催化剂和染料。以铜钴矿石[主要成分为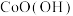 、
、 、
、 和
和 及少量Fe、Mg、Ca的氧化物]为原料制备CoO的工艺流程如图所示(钴元素的性质与铁元素类似)。
及少量Fe、Mg、Ca的氧化物]为原料制备CoO的工艺流程如图所示(钴元素的性质与铁元素类似)。
(1)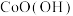 中钴元素的化合价为
中钴元素的化合价为_______ ,浸泡前矿石需要粉碎,粉碎的好处是_______ 。
(2)料渣1的主要成分是_______ ,写出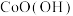 被还原时的离子方程式:
被还原时的离子方程式:_______ 。
(3)已知常温时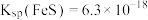 ,常温下“除铜”反应的平衡常数为
,常温下“除铜”反应的平衡常数为 ,则
,则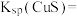
_______ ,除铁过程反应的离子方程式为_______ 。
(4)操作X的内容是_______ ,沉钴时碳元素一部分转化为沉淀,另一部分转化为_______ 。
(5)若Wkg矿石经过一系列处理后得到akgCoO,若转化过程中钴的利用率为b%,则矿石中钴元素的百分含量为_______ 。
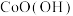 、
、 、
、 和
和 及少量Fe、Mg、Ca的氧化物]为原料制备CoO的工艺流程如图所示(钴元素的性质与铁元素类似)。
及少量Fe、Mg、Ca的氧化物]为原料制备CoO的工艺流程如图所示(钴元素的性质与铁元素类似)。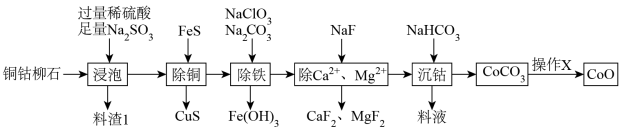
(1)
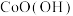 中钴元素的化合价为
中钴元素的化合价为(2)料渣1的主要成分是
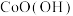 被还原时的离子方程式:
被还原时的离子方程式:(3)已知常温时
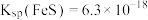 ,常温下“除铜”反应的平衡常数为
,常温下“除铜”反应的平衡常数为 ,则
,则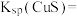
(4)操作X的内容是
(5)若Wkg矿石经过一系列处理后得到akgCoO,若转化过程中钴的利用率为b%,则矿石中钴元素的百分含量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
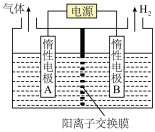
【推荐1】锂离子电池应用十分广泛,从废旧钻酸锂(LiCoO2)锂离子电池中回收铝、铁、钴、锂等元素成了重要的研究课题。现欲利用图19所示的工艺流程回收废旧电池中的某些金属资源(部分条件未给出)。回答下列问题:

已知:①滤液1中阳离子有H+、Co2+、Fe2+、Al3+、Li+等;
②两种物质不同温度下的溶解度如下表所示:
(1)钴酸锂( LiCoO2)钴元素的化合价为___________ 。
(2)浸泡时加入Na2SO3的主要目的是______________________ ;可用盐酸代替H2SO4和Na2SO3的混合液,但缺点是______________________ 。
(3)滤液1中加入NaClO3的主要目的是______________________ (用离子方程式表示)。
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mo·L-1时已沉淀完全)加入氨水调节pH的最小值是___________ 。【已知:Ksp[Fe(OH)3]=1.0×10-39,Ksp[Al(OH)3]=2.7×10-34,1g3=0.52】
(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是___________ 。
(6)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图所示的装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为___________ (填化学式)溶液;阳极电极反应式为______________________ ;电解过程中Li+向___________ (填“A”或“B”)电极迁移。

已知:①滤液1中阳离子有H+、Co2+、Fe2+、Al3+、Li+等;
②两种物质不同温度下的溶解度如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(2)浸泡时加入Na2SO3的主要目的是
(3)滤液1中加入NaClO3的主要目的是
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mo·L-1时已沉淀完全)加入氨水调节pH的最小值是
(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是
(6)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图所示的装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】绿柱石(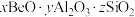 )获取BeO的常用方法有酸浸法和氟化法两种,其操作流程如图:
)获取BeO的常用方法有酸浸法和氟化法两种,其操作流程如图:
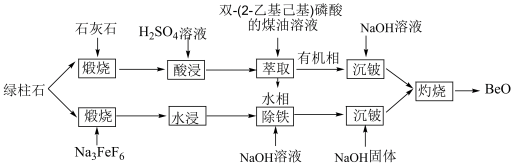
(1)为了提高“煅烧”反应的转化率,可采用的措施有___________ (写一条)。
(2)“萃取”后,水相中主要含的金属离子为___________ (填离子符号);已知Be在有机相和水相中分配比(即萃取的浓度比)约为2∶1,为了使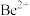 的萃取率达到99%以上,可采用的有效措施有
的萃取率达到99%以上,可采用的有效措施有___________ (写一条)。
(3)加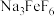 “煅烧”时,有
“煅烧”时,有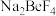 生成,则煅烧时发生的化学方程式为
生成,则煅烧时发生的化学方程式为___________ ;产物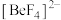 的VSEPR模型为
的VSEPR模型为___________ 。
(4)加入NaOH“除铁”时,是为了除去过量的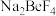 ,则发生的离子方程式为
,则发生的离子方程式为___________ 。
(5)加入NaOH“沉铍”时,为使得沉铍率达到99.9%,应调节溶液的pH值为___________ (计算结果保留至小数点后一位)。已知:沉铍前,溶液中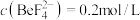 ,
,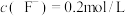 ;
; ,
,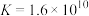 ;
;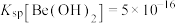 ;
; 。
。
(6)绿柱石属于硅酸盐材料,其晶体结构中含有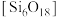 环状硅酸盐单元;z轴方向上,相邻两层
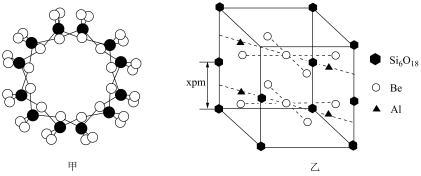
环状硅酸盐单元;z轴方向上,相邻两层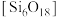 环投影图如图甲,晶胞结构如图乙。
环投影图如图甲,晶胞结构如图乙。
①z轴方向上,晶胞参数c为2xpm,而不是xpm的原因是___________ 。
②绿柱石的化学式为___________ 。
③已知:晶体中,Be、Al、Si均和氧配位,Be和Si的配位数均为4,氧的配位数有两种,分别为2和3,两种氧的个数比为1∶2.通过计算可确定Al的配付数应为___________ 。
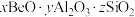 )获取BeO的常用方法有酸浸法和氟化法两种,其操作流程如图:
)获取BeO的常用方法有酸浸法和氟化法两种,其操作流程如图:
(1)为了提高“煅烧”反应的转化率,可采用的措施有
(2)“萃取”后,水相中主要含的金属离子为
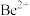 的萃取率达到99%以上,可采用的有效措施有
的萃取率达到99%以上,可采用的有效措施有(3)加
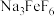 “煅烧”时,有
“煅烧”时,有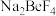 生成,则煅烧时发生的化学方程式为
生成,则煅烧时发生的化学方程式为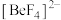 的VSEPR模型为
的VSEPR模型为(4)加入NaOH“除铁”时,是为了除去过量的
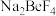 ,则发生的离子方程式为
,则发生的离子方程式为(5)加入NaOH“沉铍”时,为使得沉铍率达到99.9%,应调节溶液的pH值为
 ,
,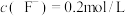 ;
; ,
,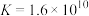 ;
;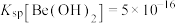 ;
; 。
。(6)绿柱石属于硅酸盐材料,其晶体结构中含有
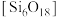 环状硅酸盐单元;z轴方向上,相邻两层
环状硅酸盐单元;z轴方向上,相邻两层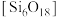 环投影图如图甲,晶胞结构如图乙。
环投影图如图甲,晶胞结构如图乙。①z轴方向上,晶胞参数c为2xpm,而不是xpm的原因是
②绿柱石的化学式为
③已知:晶体中,Be、Al、Si均和氧配位,Be和Si的配位数均为4,氧的配位数有两种,分别为2和3,两种氧的个数比为1∶2.通过计算可确定Al的配付数应为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】为充分利用资源,变废为宝,可从废旧CPU[含Au(金)、Ag、Cu和Pt(铂)]中回收Au,其化工流程如图:
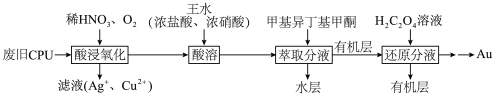
回答下列问题
(1)“酸浸氧化”中,为了提高反应速率,可以采取的措施是___________ (写出一种即可)。
(2)“酸浸氧化”中,通入氧气的目的是___________ 。
(3)“酸溶”时,Pt、Au分别转化为H2PtCl6和HAuCl4,同时有NO生成。Pt溶解的化学方程式是___________ 。
(4)“萃取分液”后的“水层”中可回收的金属是___________ 。
(5)从“还原分液”后的“有机层”中回收甲基异丁基甲酮,采用的方法是___________ 。
(6)理论上消耗1mol草酸(H2C2O4)可得到Au的质量为___________ g(结果保留一位小数)。
(7)提取“滤液”中的Ag+会涉及反应AgCl(s)+2NH3 [Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为
[Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为 ___________ 。已知:①[Ag(NH3)2]+ Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。

回答下列问题
(1)“酸浸氧化”中,为了提高反应速率,可以采取的措施是
(2)“酸浸氧化”中,通入氧气的目的是
(3)“酸溶”时,Pt、Au分别转化为H2PtCl6和HAuCl4,同时有NO生成。Pt溶解的化学方程式是
(4)“萃取分液”后的“水层”中可回收的金属是
(5)从“还原分液”后的“有机层”中回收甲基异丁基甲酮,采用的方法是
(6)理论上消耗1mol草酸(H2C2O4)可得到Au的质量为
(7)提取“滤液”中的Ag+会涉及反应AgCl(s)+2NH3
 [Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为
[Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为  Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硒被誉为“生命元素”。亚硒酸钙(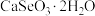 ,难溶于水)常作饲料添加剂,
,难溶于水)常作饲料添加剂, 常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
①含硒废料的主要成分是 和
和 ;“焙烧”时固体产物为
;“焙烧”时固体产物为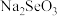 、
、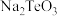 和
和 。
。
② 易溶于水,
易溶于水, 难溶于水。
难溶于水。
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为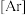
___________ 。
(2)利用“浸渣”可以制备胆矾,其操作步骤是加入足量稀硫酸溶解,再通入热空气。通入热空气的目的是___________ (用离子方程式表示)。
(3)上述参加反应的双氧水远小于实际消耗的双氧水(反应温度在 ),其主要原因是
),其主要原因是___________ 。
(4)硒酸分解制备 的副产物有
的副产物有___________ (填化学式)。
(5)已知 、
、 的熔点分别为
的熔点分别为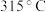 、
、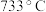 ,其熔点差异的主要原因是
,其熔点差异的主要原因是___________ 。
(6)测定 产品纯度。称取
产品纯度。称取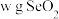 产品溶于水配制成
产品溶于水配制成 溶液,取
溶液,取 于锥形瓶中,加入足量
于锥形瓶中,加入足量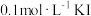 溶液和适量稀硝酸,充分反应后,滴加3滴
溶液和适量稀硝酸,充分反应后,滴加3滴 淀粉溶液,用
淀粉溶液,用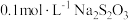 溶液滴定至终点时消耗
溶液滴定至终点时消耗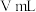 滴定液。发生有关反应:
滴定液。发生有关反应:
①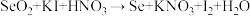 (未配平)
(未配平)
②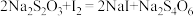
该 产品中硒元素的质量分数为
产品中硒元素的质量分数为___________ %。如果大量空气进入锥形瓶,可能导致测得的结果___________ (填“偏高”“偏低”或“无影响”)。
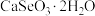 ,难溶于水)常作饲料添加剂,
,难溶于水)常作饲料添加剂, 常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题: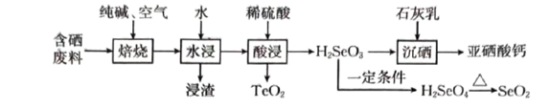
①含硒废料的主要成分是
 和
和 ;“焙烧”时固体产物为
;“焙烧”时固体产物为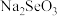 、
、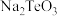 和
和 。
。②
 易溶于水,
易溶于水, 难溶于水。
难溶于水。(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为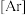
(2)利用“浸渣”可以制备胆矾,其操作步骤是加入足量稀硫酸溶解,再通入热空气。通入热空气的目的是
(3)上述参加反应的双氧水远小于实际消耗的双氧水(反应温度在
 ),其主要原因是
),其主要原因是(4)硒酸分解制备
 的副产物有
的副产物有(5)已知
 、
、 的熔点分别为
的熔点分别为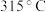 、
、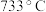 ,其熔点差异的主要原因是
,其熔点差异的主要原因是(6)测定
 产品纯度。称取
产品纯度。称取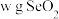 产品溶于水配制成
产品溶于水配制成 溶液,取
溶液,取 于锥形瓶中,加入足量
于锥形瓶中,加入足量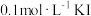 溶液和适量稀硝酸,充分反应后,滴加3滴
溶液和适量稀硝酸,充分反应后,滴加3滴 淀粉溶液,用
淀粉溶液,用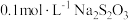 溶液滴定至终点时消耗
溶液滴定至终点时消耗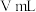 滴定液。发生有关反应:
滴定液。发生有关反应:①
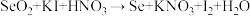 (未配平)
(未配平)②
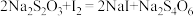
该
 产品中硒元素的质量分数为
产品中硒元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某地煤矸石经预处理后主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO及钙镁的化合物等。某实验小组利用其提取Al(OH)3。
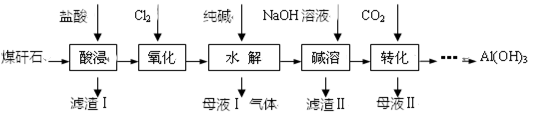
(1)“酸浸”过程中发生的主要反应的离子方程式为______________ 。为提高“酸浸”时铝浸出率,可采取的措施之一是______________________________ 。
(2)“氧化”的目的是____________ 。检验Fe3+已水解完全的方法是_____________ 。
(3)滤渣Ⅱ的主要成分是CaCO3、Mg(OH)2和_____________________________________ 。
(4)①上述流程中可循环利用的物质的化学式是_________________________________ 。
②“转化”时主要反应的离子方程式为_______________________________________ 。
(5)Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得产品Al(OH)3,从氧化后的溶液开始,若只用纯碱一种试剂,后续操作是_____________ 。

(1)“酸浸”过程中发生的主要反应的离子方程式为
(2)“氧化”的目的是
(3)滤渣Ⅱ的主要成分是CaCO3、Mg(OH)2和
(4)①上述流程中可循环利用的物质的化学式是
②“转化”时主要反应的离子方程式为
(5)Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得产品Al(OH)3,从氧化后的溶液开始,若只用纯碱一种试剂,后续操作是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】某地煤矸石经预处理后主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO及MgO。实验小组设计如下流程用其制备碱式硫酸铝[Al2(OH)4SO4]:
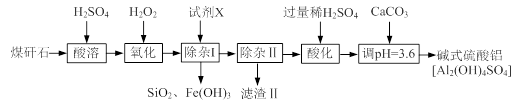
(1)为提高“酸浸”时铝浸出率,可采取的措施之一是_____ 。
(2)氧化时应控制反应温度在10℃~20℃,其原因是_____ ,“氧化”时可用MnO2替代,发生的离子方程式_____ 。
(3)试剂X为_____ ,设计一个简单的实验,证明铁元素已被沉淀完全:_____ 。
(4)加入CaCO3制备碱式硫酸铝的化学方程式_____ 。
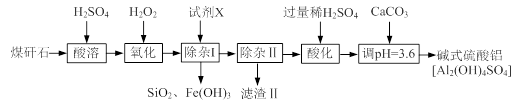
(1)为提高“酸浸”时铝浸出率,可采取的措施之一是
(2)氧化时应控制反应温度在10℃~20℃,其原因是
(3)试剂X为
(4)加入CaCO3制备碱式硫酸铝的化学方程式
您最近一年使用:0次



