氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如下所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以[Zn(NH3)4 ]2+、[Cu(NH3)4] 2+、[Cd(NH3)4 ]2+、[AsCl5 ]2-的形式存在。
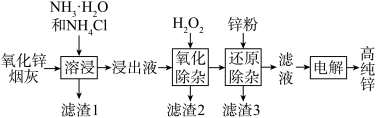
回答下列问题:
(1)当NH3•H2O和NH4Cl的混合溶液中存在c(NH )=c(Cl-)时,溶液呈
)=c(Cl-)时,溶液呈___________ (填“酸”、“碱”或“中”)性,[Cd(NH3)4]2+中Cd的化合价为___________ 。
(2)“溶浸”时,氧化锌参与反应的相关离子方程式为ZnO+2NH3•H2O+2NH =[Zn(NH3)4] 2++3H2O,“溶浸”时温度不宜过高,其原因是
=[Zn(NH3)4] 2++3H2O,“溶浸”时温度不宜过高,其原因是___________ ,1mol [Zn(NH3)4]Cl2配合物中含有共价键的数目为___________ 。
(3)“氧化除杂”中,[AsCl5]2-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性, 该反应的离子方程式为___________ 。
(4)“滤渣3”的主要成分为___________ 。
(5)“电解”时[Zn(NH3)4]2+在阴极放电的电极反应式为___________ 。
(6)硫化锌(ZnS)是常见的硫化物,其一种晶胞结构如图所示。
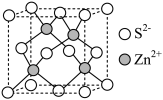
①设晶胞边长为a pm,NA为阿伏加德罗常数的值,则该晶体的密度为___________ g•cm-3(用含a、NA的代数式表示)。
②将0.05mol ZnS完全溶解于500 mL盐酸中,忽略溶液体积的变化,所得溶液中c(S2-)不高于___________ mol•L-1。[已知:Ksp(ZnS)=2.5×10-23]

回答下列问题:
(1)当NH3•H2O和NH4Cl的混合溶液中存在c(NH
 )=c(Cl-)时,溶液呈
)=c(Cl-)时,溶液呈(2)“溶浸”时,氧化锌参与反应的相关离子方程式为ZnO+2NH3•H2O+2NH
 =[Zn(NH3)4] 2++3H2O,“溶浸”时温度不宜过高,其原因是
=[Zn(NH3)4] 2++3H2O,“溶浸”时温度不宜过高,其原因是(3)“氧化除杂”中,[AsCl5]2-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性, 该反应的离子方程式为
(4)“滤渣3”的主要成分为
(5)“电解”时[Zn(NH3)4]2+在阴极放电的电极反应式为
(6)硫化锌(ZnS)是常见的硫化物,其一种晶胞结构如图所示。

①设晶胞边长为a pm,NA为阿伏加德罗常数的值,则该晶体的密度为
②将0.05mol ZnS完全溶解于500 mL盐酸中,忽略溶液体积的变化,所得溶液中c(S2-)不高于
更新时间:2024/03/04 22:19:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上常用辉铜矿(主要成分为Cu2S,含有Fe2O3、CaO、SiO2等杂质)制备重要催化剂CuCl。工艺如下:
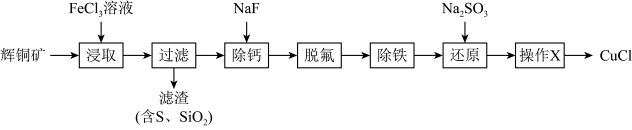
已知:①CuCl为难溶于水的白色固体
②部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
请回答下列问题:
(1)“浸取”过程中Cu2S转化为可溶性铜盐的离子方程式为:___________ 。
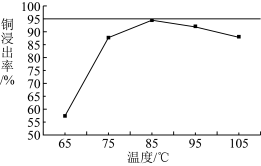
(2)“浸取“是该工艺的第一步,提高浸出率可提高最终产品产率。工程师研究发现单独加入FeCl3溶液时Cu2+浸出率很低,但同时加入FeCl3溶液和H2O2时可提高Cu2+浸出率,写出H2O2与Fe2+反应的离子方程式___________ 。进一步研究发现,加入H2O2后随温度升高,一定时间后Cu2+浸出率随温度变化的曲线如图。请分析温度高于85℃,Cu2+浸出率下降的原因___________ 。
(3)已知Ksp(CaF2)=4.0×10−11经测定“浸出液”中Ca2+浓度为4.0×10−3mol·L−1,加入NaF除去溶液中Ca2+,当溶液中c(F-)=1.0×10−3mol·L−1时,除钙率为___________ 。
(4)“除铁”过程包括氧化Fe2+、加入CuO调节pH等过程,为达到“除铁”目的需调节溶液pH范围为___________ 。
(5)“还原”过程中反应的离子方程式为:___________ 。
(6)通过“操作X”___________ ,___________ ,___________ (填操作名称),最终得到CuCl产品。

已知:①CuCl为难溶于水的白色固体
②部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Cu2+ | 4.4 | 6.4 |
请回答下列问题:
(1)“浸取”过程中Cu2S转化为可溶性铜盐的离子方程式为:
(2)“浸取“是该工艺的第一步,提高浸出率可提高最终产品产率。工程师研究发现单独加入FeCl3溶液时Cu2+浸出率很低,但同时加入FeCl3溶液和H2O2时可提高Cu2+浸出率,写出H2O2与Fe2+反应的离子方程式

(3)已知Ksp(CaF2)=4.0×10−11经测定“浸出液”中Ca2+浓度为4.0×10−3mol·L−1,加入NaF除去溶液中Ca2+,当溶液中c(F-)=1.0×10−3mol·L−1时,除钙率为
(4)“除铁”过程包括氧化Fe2+、加入CuO调节pH等过程,为达到“除铁”目的需调节溶液pH范围为
(5)“还原”过程中反应的离子方程式为:
(6)通过“操作X”
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
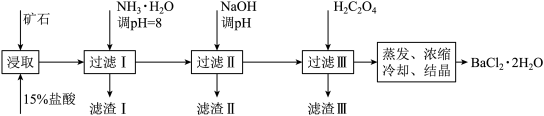
【推荐2】某矿石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用该矿石制备BaCl2•2H2O的流程如图,且三次滤渣的主要成分各不相同:
如表为常温时各离子转化为氢氧化物沉淀时的pH:
(1)用15%盐酸浸取前需充分研磨,目的是______ 。
(2)滤渣Ⅰ的主要成分为______ ;加入NaOH调pH的范围为______ ;加入H2C2O4时应避免过量的原因是______ 。[已知难溶物质:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9]
(3)已知:25℃时,Ksp(BaCO3)=5.4×10-9,Ksp(CaCO3)=2.7×10-9。向CaCO3固体的溶液中加入高浓度的BaCl2溶液,有BaCO3沉淀生成,请写出该反应的离子方程式______ ,该反应的平衡常数K=______ 。
(4)取制得的BaCl2•2H2O(含少量杂质)2.5g配成100mL溶液,取10.00mL该溶液于烧杯中,加入足量(NH4)2C2O4溶液,过滤,洗涤,将得到的BaC2O4沉淀用过量稀硫酸溶液溶解,过滤除去BaSO4沉淀,将所得的H2C2O4溶液移入锥形瓶,用0.05mol/L高锰酸钾标准液滴定至终点。
已知:Ba2++C2O42-═BaC2O4↓
BaC2O4+2H++SO42-═BaSO4↓+H2C2O4
5H2C2O4+2MnO4-+16H+═10CO2↑+2Mn2++8H2O
①滴定中盛放高锰酸钾标准液的仪器为______ ,滴入最后一滴高锰酸钾溶液,锥形瓶中溶液颜色______ ,即说明达到滴定终点。
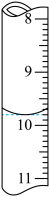
②若滴定前滴定管的读数为1.80mL,滴定终点时滴定管中液面如图,请计算BaCl2•2H2O的纯度为______ (保留3位有效数字)。

如表为常温时各离子转化为氢氧化物沉淀时的pH:
| Fe3+ | Mg2+ | Ca2+ | |
| 开始沉淀时的pH | 1.9 | 9.1 | 11.9 |
| 完全沉淀时的pH | 3.2 | 11.1 | 13.9 |
(1)用15%盐酸浸取前需充分研磨,目的是
(2)滤渣Ⅰ的主要成分为
(3)已知:25℃时,Ksp(BaCO3)=5.4×10-9,Ksp(CaCO3)=2.7×10-9。向CaCO3固体的溶液中加入高浓度的BaCl2溶液,有BaCO3沉淀生成,请写出该反应的离子方程式
(4)取制得的BaCl2•2H2O(含少量杂质)2.5g配成100mL溶液,取10.00mL该溶液于烧杯中,加入足量(NH4)2C2O4溶液,过滤,洗涤,将得到的BaC2O4沉淀用过量稀硫酸溶液溶解,过滤除去BaSO4沉淀,将所得的H2C2O4溶液移入锥形瓶,用0.05mol/L高锰酸钾标准液滴定至终点。
已知:Ba2++C2O42-═BaC2O4↓
BaC2O4+2H++SO42-═BaSO4↓+H2C2O4
5H2C2O4+2MnO4-+16H+═10CO2↑+2Mn2++8H2O
①滴定中盛放高锰酸钾标准液的仪器为
②若滴定前滴定管的读数为1.80mL,滴定终点时滴定管中液面如图,请计算BaCl2•2H2O的纯度为

您最近半年使用:0次
【推荐3】红土镍矿渣主要成分包含铁、钴、镍、锰、铬、硅的氧化物,为节约和充分利用资源,利用如下流程进行分离回收。已知该温度下Co(OH)2、Fe(OH)3的溶度积分别是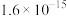 、
、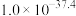 。回答下列问题:
。回答下列问题:
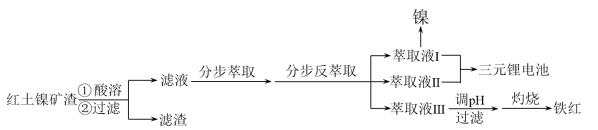
(1)酸溶时,需将红土镍矿渣研成粉末,目的是_______ 。
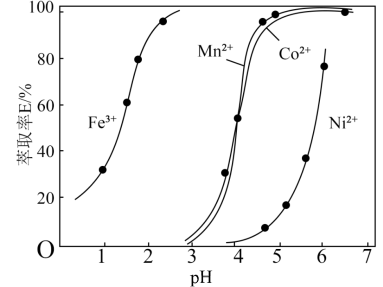
(2)各种离子萃取率与pH关系如图。分步萃取前需通入适量氧气,目的是_______ ,分步萃取浸出金属离子先后顺序为_______ 、_______ 、_______ ,当调pH=4.60时,溶液中
_______ 。
(3)萃取液I电解制取镍的阴极电极反应式为_______ 。
(4)三元锂电池化学式为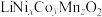 ,其中
,其中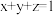 ,Ni、Co、Mn的化合价分别为+2、+3、+4,则
,Ni、Co、Mn的化合价分别为+2、+3、+4,则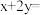
_______ (用含z的代数式表示)。
(5)写出铁红的一种用途:_______ 。
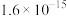 、
、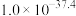 。回答下列问题:
。回答下列问题:
(1)酸溶时,需将红土镍矿渣研成粉末,目的是
(2)各种离子萃取率与pH关系如图。分步萃取前需通入适量氧气,目的是


(3)萃取液I电解制取镍的阴极电极反应式为
(4)三元锂电池化学式为
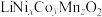 ,其中
,其中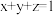 ,Ni、Co、Mn的化合价分别为+2、+3、+4,则
,Ni、Co、Mn的化合价分别为+2、+3、+4,则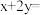
(5)写出铁红的一种用途:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2、CuO和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
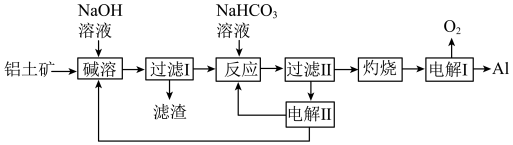
已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀,过滤所得滤液中溶质的主要成分为Na[Al(OH)4]。
(1)基态Al原子的L层电子排布图为___________ 。基态Si原子核外共有___________ 种空间运动状态的电子。
(2)基态Fe原子的核外电子排布式为___________ 。
(3)C、Na、O、Cu的第一电离能由大到小的顺序为___________ 。
(4)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________ 。
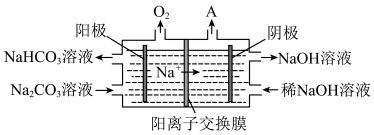
(5)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为___________ ,阴极产生的物质A的化学式为___________ 。

已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀,过滤所得滤液中溶质的主要成分为Na[Al(OH)4]。
(1)基态Al原子的L层电子排布图为
(2)基态Fe原子的核外电子排布式为
(3)C、Na、O、Cu的第一电离能由大到小的顺序为
(4)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是
(5)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列方程式
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:___________ 。
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:___________ 。
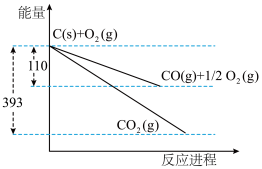
②固体C和CO2气体生成CO气体的热化学方程式:___________ 。
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:___________ 。
(4)某碱性电池的电池反应为3Zn+2K2FeO4 Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:___________ 。
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:

②固体C和CO2气体生成CO气体的热化学方程式:
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:
(4)某碱性电池的电池反应为3Zn+2K2FeO4
 Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】自然界中存在大量元素,在工农业生产中有广泛应用。回答下列问题:
(1)人工合成的蓝宝石晶体(Al2O3)是目前半导体工业中应用最广泛的材料。
①基态Al原子中有______ 种运动状态不同的电子,核外电子占据最高能级的符号是_____ ,占据该能级电子的电子云轮廓图形状为_______ 。
②比较第一电高能:Mg______ Al(填“>”、”<”或“=”)。在现代化学中,常利用_________ 上的特征谱线来鉴定元素,称为光谱分析。
(2)羰基硫(COS)存在于许多种植物中,杀虫效果显著。
①1molCOS分子中含有σ键的数目为_____ ,其中心原子的杂化方式为_____ 。
②CS2、CO2、COS的分解温度由低到高的顺序为_____ 。
(3)NaCl 和MgO都属于离子化合物.NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是_______________ 。
(4)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

则:①距离一个Fe原子最近的Mg原子个数是______ ,与此晶胞结构相似的常见的离子晶体是______ (填名称)。
②若该晶体储氢时,H2分子在晶胞的体心和棱心位置,晶胞的参数为dnm,则距离最近的两个H2分子之间的距离为______ cm;含铁56g的该储氢合金可储存标准状况下H2的体积为____ L。
(1)人工合成的蓝宝石晶体(Al2O3)是目前半导体工业中应用最广泛的材料。
①基态Al原子中有
②比较第一电高能:Mg
(2)羰基硫(COS)存在于许多种植物中,杀虫效果显著。
①1molCOS分子中含有σ键的数目为
②CS2、CO2、COS的分解温度由低到高的顺序为
(3)NaCl 和MgO都属于离子化合物.NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是
(4)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

则:①距离一个Fe原子最近的Mg原子个数是
②若该晶体储氢时,H2分子在晶胞的体心和棱心位置,晶胞的参数为dnm,则距离最近的两个H2分子之间的距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】磷是人体含量较多的元素之一,磷的化合物在药物生产和农药制造等方面用途非常广泛。回答下列问题:
(1) 可用于制造火柴,其分子结构如图甲所示。
可用于制造火柴,其分子结构如图甲所示。

①第一电离能:磷___________ 硫(填“>”或“<”),
② 分子中硫原子的杂化轨道类型为
分子中硫原子的杂化轨道类型为___________ 。
③每个 分子中含孤电子对的数目为
分子中含孤电子对的数目为___________ 。
(2)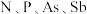 均是第
均是第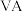 族的元素。
族的元素。
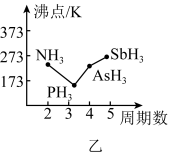
①上述元素的氢化物的沸点关系如图乙所示,沸点: ,其原因是
,其原因是___________
②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为___________ 。

(3)磷化铝熔点为2000℃,磷化铝晶胞结构如图丁所示。

①图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为___________ 。
②磷化铝晶体的密度为 ,用
,用 表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为
表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为___________ cm。
(1)
 可用于制造火柴,其分子结构如图甲所示。
可用于制造火柴,其分子结构如图甲所示。
①第一电离能:磷
②
 分子中硫原子的杂化轨道类型为
分子中硫原子的杂化轨道类型为③每个
 分子中含孤电子对的数目为
分子中含孤电子对的数目为(2)
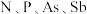 均是第
均是第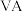 族的元素。
族的元素。①上述元素的氢化物的沸点关系如图乙所示,沸点:
 ,其原因是
,其原因是
②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为

(3)磷化铝熔点为2000℃,磷化铝晶胞结构如图丁所示。

①图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为
②磷化铝晶体的密度为
 ,用
,用 表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为
表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜及其化合物有许多特殊用途,最近科研人员用CuP2作电极电催化CO2,CO2经甲酸盐、乙醛最终转化为1-丁醇,铜则转化为Cu3(PO4)2和Cu2O。回答下列问题:。
(1)基态磷原子的价电子排布图为___________ ,基态Cu原子电子占据最高能级的电子云轮廓图为___________ 形。
(2)Cu、O、P三种元素中,电负性由大到小的顺序为___________ ,C、O、P最简单氢化物的沸点由大到小的顺序为___________ 。(用“>”连接氢化物化学式)。
(3) 的空间构型为
的空间构型为___________ ,其中P采取___________ 杂化方式。
(4)1-丁醇、1-氯丁烷的沸点依次为118°C、78.2°C,前者沸点较高的原因是___________ 。
(5)Cu、Mn、Al形成的一种金属间化合物的晶体结构如图所示。已知晶胞参数为apm,内部正方形的边长为bpm,NA表示阿伏加德罗常数。

该晶体的密度为___________ (用含a、NA的代数式表示);P、Q间的距离为___________ pm。
(1)基态磷原子的价电子排布图为
(2)Cu、O、P三种元素中,电负性由大到小的顺序为
(3)
 的空间构型为
的空间构型为(4)1-丁醇、1-氯丁烷的沸点依次为118°C、78.2°C,前者沸点较高的原因是
(5)Cu、Mn、Al形成的一种金属间化合物的晶体结构如图所示。已知晶胞参数为apm,内部正方形的边长为bpm,NA表示阿伏加德罗常数。

该晶体的密度为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】高纯度氧化铝有广泛的用途,某研究小组研究用以下流程制取高纯度氧化铝:
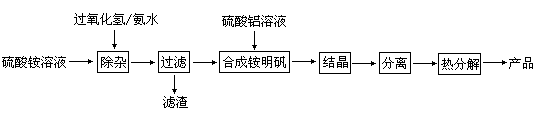
根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式____________________________ 。
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10—38,除杂后溶液中c(Fe3+)约为_____________ 。
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是________________________ 。
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是____________ 。
(5)“分离”操作的名称是_____________ (填字母代号)。
A.蒸馏 B.分液 C.过滤
(6)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是__________ ,离子浓度最小的离子是____________ 。

根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10—38,除杂后溶液中c(Fe3+)约为
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水)。母液不能蒸干的原因是
(5)“分离”操作的名称是
A.蒸馏 B.分液 C.过滤
(6)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某兴趣小组用铬铁矿( ,含
,含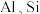 氧化物等杂质)为主要原料制备
氧化物等杂质)为主要原料制备 晶体,流程如下:
晶体,流程如下:
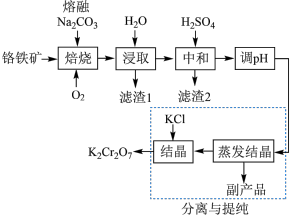
(1)焙烧的目的是将 转化为
转化为 和
和 ,并将
,并将 氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是
氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是___________ 。
(2)滤渣2的主要成分是 和
和___________ 。
(3)流程中调溶液的 使之变
使之变___________ (填“大”或“小”),原因是___________ (用离子方程式表示)。
(4)蒸发结晶所产生的副产品是___________ 。
 ,含
,含 氧化物等杂质)为主要原料制备
氧化物等杂质)为主要原料制备 晶体,流程如下:
晶体,流程如下:
(1)焙烧的目的是将
 转化为
转化为 和
和 ,并将
,并将 氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是
氧化物转化为可溶性钠盐。焙烧时气体与矿料逆流而行,目的是(2)滤渣2的主要成分是
 和
和(3)流程中调溶液的
 使之变
使之变(4)蒸发结晶所产生的副产品是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】硫是一种重要的非金属元素,化工生产中通过控制化学反应条件而实现含硫物质的相互转化。回答下列问题:
Ⅰ.电化学溶解-沉淀法是一种回收利用H2S的新方法,其工艺原理如图所示:

已知:Zn与强酸、强碱都能反应生成H2;Zn2+在过量的强碱溶液中以[Zn(OH)4]2-形式存在。
(1)锌棒连接直流电源的_______ 极,电极反应方程式为_______ 。
(2)反应器中反应的离子方程式为_______ 。
Ⅱ.生成的ZnS可制立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。成品中S2−的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取20.00 mL 0.1000 mol·L-1的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I2用0.1050 mol·L-1 Na2S2O3溶液滴定,反应式为I2+2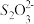 =2I−+
=2I−+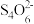 。测定时消耗Na2S2O3溶液体积V mL。
。测定时消耗Na2S2O3溶液体积V mL。
(3)Na2S2O3可利用向Na2S和Na2SO3混合溶液中通入SO2的方法制备,该方法的离子反应方程式为_______ 。
(4)上述制备的反应溶液应保持碱性环境,请用简要的文字并结合离子方程式解释其原因_______ 。
(5)Na2S2O3溶液不稳定,使用前需用K2Cr2O7、KIO3等基准物质进行标定,标定过程利用Na2S2O3具有_______ 性。
(6)该样品中S2-的百分含量为_______ (写出表达式)。若Na2S2O3溶液标定后,放置过久使用,则测定结果_______ (填“偏高”、“偏低”或“无影响”)。
III.利用沉淀间的转化,可使BaSO4中的 进入溶液中,现将0.28 mol BaSO4沉淀,每次用1L1.50mol·L-1 Na2CO3溶液处理,若使BaSO4中的
进入溶液中,现将0.28 mol BaSO4沉淀,每次用1L1.50mol·L-1 Na2CO3溶液处理,若使BaSO4中的 全部进入溶液中,需反复洗
全部进入溶液中,需反复洗_______ 次(已知Ksp(BaSO4)=1.07×10-10、Ksp(BaCO3)=2.58×10-9)。
Ⅰ.电化学溶解-沉淀法是一种回收利用H2S的新方法,其工艺原理如图所示:

已知:Zn与强酸、强碱都能反应生成H2;Zn2+在过量的强碱溶液中以[Zn(OH)4]2-形式存在。
(1)锌棒连接直流电源的
(2)反应器中反应的离子方程式为
Ⅱ.生成的ZnS可制立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。成品中S2−的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取20.00 mL 0.1000 mol·L-1的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I2用0.1050 mol·L-1 Na2S2O3溶液滴定,反应式为I2+2
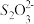 =2I−+
=2I−+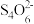 。测定时消耗Na2S2O3溶液体积V mL。
。测定时消耗Na2S2O3溶液体积V mL。(3)Na2S2O3可利用向Na2S和Na2SO3混合溶液中通入SO2的方法制备,该方法的离子反应方程式为
(4)上述制备的反应溶液应保持碱性环境,请用简要的文字并结合离子方程式解释其原因
(5)Na2S2O3溶液不稳定,使用前需用K2Cr2O7、KIO3等基准物质进行标定,标定过程利用Na2S2O3具有
(6)该样品中S2-的百分含量为
III.利用沉淀间的转化,可使BaSO4中的
 进入溶液中,现将0.28 mol BaSO4沉淀,每次用1L1.50mol·L-1 Na2CO3溶液处理,若使BaSO4中的
进入溶液中,现将0.28 mol BaSO4沉淀,每次用1L1.50mol·L-1 Na2CO3溶液处理,若使BaSO4中的 全部进入溶液中,需反复洗
全部进入溶液中,需反复洗
您最近半年使用:0次

 ,图中的离子交换膜只允许
,图中的离子交换膜只允许 通过,
通过, 、
、 、
、 均为石墨电极,
均为石墨电极, 为铜电极。工作一段时间后,断开
为铜电极。工作一段时间后,断开 ,此时
,此时
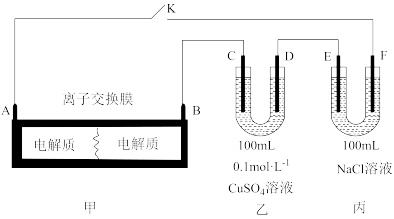
 电极为电池的
电极为电池的 电极的电极反应式为
电极的电极反应式为

