已知常温下,向 溶液中,滴入
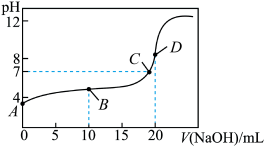
溶液中,滴入 NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)
NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)
 溶液中,滴入
溶液中,滴入 NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)
NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)
A.若A点的 ,则此温度下醋酸的电离度计算式为 ,则此温度下醋酸的电离度计算式为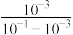 |
B.B点存在等式关系: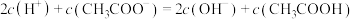 |
C.若C点加入氢氧化钠溶液amL,则常温下醋酸的电离平衡常数计算式为 |
D.若D点 ,则由水电离出的 ,则由水电离出的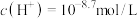 |
更新时间:2020-02-09 14:36:59
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在水电离出的c(H+)=10-14mol/L的溶液中,一定能大量共存的离子组是
| A.K+、Na+、HCO3-、Cl- | B.K+、AlO2-、Br-、Cl- |
| C.Na+、Cl-、NO3-、SO42- | D.Al3+、NH4+、Cl-、SO42- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
A.用湿润的pH试纸测定 溶液的pH 溶液的pH |
| B.广泛pH试纸测得某碱性溶液的pH为12.5 |
C.常温下1LpH=13的氢氧化钠溶液中由水电离出的 的数目为 的数目为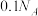 |
D. 的溶液不一定呈酸性 的溶液不一定呈酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温时,取
 和
和
 (一元酸,
(一元酸, )混合溶液20mL,用
)混合溶液20mL,用
 溶液滴定,滴定曲线如图所示,下列说法正确的是
溶液滴定,滴定曲线如图所示,下列说法正确的是

 和
和
 (一元酸,
(一元酸, )混合溶液20mL,用
)混合溶液20mL,用
 溶液滴定,滴定曲线如图所示,下列说法正确的是
溶液滴定,滴定曲线如图所示,下列说法正确的是
A. 点时,溶液中 点时,溶液中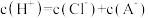 |
B. 点时, 点时, |
C. 点时, 点时, |
D. 过程中, 过程中, 的 的 保持不变 保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】控制变量是科学研究的重要方法。
已知反应: 下列条件中反应速率最快的是
下列条件中反应速率最快的是
已知反应:
 下列条件中反应速率最快的是
下列条件中反应速率最快的是| 选项 | 温度 | 0.1  溶液 溶液 | 0.1 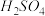 溶液 溶液 | 蒸馏水 |
| A | 15℃ | 5mL | 5mL | 5mL |
| B | 15℃ | 5mL | 5mL | 10mL |
| C | 35℃ | 5mL | 5mL | 5mL |
| D | 35℃ | 5mL | 5mL | 0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】柠檬酸H3A是一种三元弱酸。常温下向一定浓度的H3A溶液中滴加KOH溶液,溶液中lgX[X表示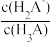 、
、 或
或 ]随pH的变化关系如图所示。下列说法正确的是
]随pH的变化关系如图所示。下列说法正确的是

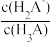 、
、 或
或 ]随pH的变化关系如图所示。下列说法正确的是
]随pH的变化关系如图所示。下列说法正确的是
| A.用KOH溶液滴定柠檬酸H3A至K2HA,可选用酚酞作指示剂 |
B.在滴加KOH溶液至P点时有 |
| C.在3.13<pH<4.76时,有c(H2A-)>c(HA2-)>c(H3A) |
| D.在4.76<pH<6.40时,有c(H+)+c(K+)=c(OH-)+c(HA2-)+2c(H2A-)+3c(A3-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知H2A为二元弱酸,25 ℃时,用Na2A溶液吸收H2A,且最终吸收H2A的量小于原溶液中Na2A的物质的量,其吸收液pH随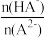 变化的关系如图所示,以下说法不正确的是
变化的关系如图所示,以下说法不正确的是
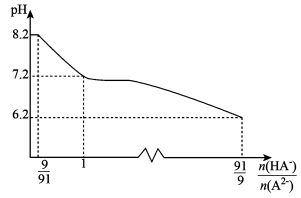
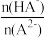 变化的关系如图所示,以下说法不正确的是
变化的关系如图所示,以下说法不正确的是
| A.向Na2A溶液加入H2A过程中,水电离的c(OH-)不断增大 |
| B.NaHA溶液中:c(H+)>c(OH-) |
| C.H2A的第二步电离常数的数量级为10-8 |
| D.当吸收液呈中性时:c(Na+)=2c(A2-)+c(HA-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】H2X为二元弱酸。20℃时,向100mL0.1mol·L-1的Na2X溶液中缓慢通入HCl(忽略溶液体积变化及H2X的挥发)。指定溶液中微粒的物质的量浓度关系一定正确的是
| A.通入HCl前:c(X2-)>c(HX-)>c(OH-)>c(H+) |
| B.若通入5×10-3molHCl,溶液呈碱性,则溶液中c(X2-)=c(HX-) |
| C.pH=7时:溶液中c(HX-)>c(Cl-) |
| D.c(Cl-)=0.1mol·L-1时:c(OH-)-c(H+)=c(H2X)-c(X2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小 减小 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氨水中加入盐酸至中性,溶液中 <1 <1 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】298K时,在20.0mL0.10mol·L-1氨水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述不正确 的是
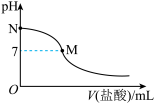
| A.该滴定过程应该选择甲基橙作为指示剂 |
| B.N点处的溶液中12<pH<14 |
C.M点处的溶液中c(NH )=c(Cl-)>c(H+)=c(OH-) )=c(Cl-)>c(H+)=c(OH-) |
D.过M点后的所得溶液中可存在如下离子浓度大小关系:c(Cl-)>c(H+)>c(NH )>c(OH-) )>c(OH-) |
您最近一年使用:0次

 K(HY),平衡正向移动,促进HY电离
K(HY),平衡正向移动,促进HY电离 值变小
值变小

