下列有关电解质溶液中粒子浓度关系正确的是( )
A.含有AgCl和AgI固体的悬浊液: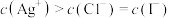 |
B. 的 的 溶液: 溶液: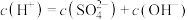 |
C.常温下, 的a. 的a. 、b. 、b. 、c. 、c. 溶液中: 溶液中: 大小顺序:a>b>c 大小顺序:a>b>c |
D.物质的量浓度之比为1:2的NaClO、 混合溶液中: 混合溶液中: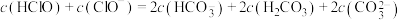 |
2020高三·全国·专题练习 查看更多[2]
更新时间:2020-02-08 11:12:28
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】室温下,0.1mol·L-1下列溶液的pH最大的是
| A.Na2CO3 | B.NaOH | C.NH4Cl | D.Na2SO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】 溶液中,如果要使
溶液中,如果要使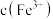 更接近于
更接近于 ,可以采取的措施是
,可以采取的措施是
 溶液中,如果要使
溶液中,如果要使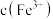 更接近于
更接近于 ,可以采取的措施是
,可以采取的措施是| A.加入适量水 | B.加入少量 溶液 溶液 | C.通入适量 气体 气体 | D.加热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法不正确的是
| A.将纯水加热,pH减小,仍呈中性 |
| B.中和物质的量相同的氢氧化钠,消耗盐酸和醋酸的物质的量相同 |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.在相同温度下,pH相等的盐酸、CH3COOH溶液,c(Cl―)=c(CH3COO―) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】室温下,下列溶液中粒子浓度关系正确的是
| A.Na2S溶液:c(Na+)> c(HS-)>c(OH-) > c(H2S) |
B.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O )+2c(H2C2O4) )+2c(H2C2O4) |
C.pH=5的NaHSO3溶液: c(Na+)>c(H2SO3)>c(SO )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】浓度均为0.1 mol / L的①NaHCO3、②Na2CO3、③NaCl、④NaHSO4四种溶液,按pH值由小到大排列的顺序是
| A.①②③④ | B.④③①② | C.③④①② | D.②①④③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列关于电解质溶液中离子关系的说法中正确的是
A.0.1mol·L-1Na2CO3溶液中离子浓度关系:c(Na+)=2c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
B.0.1mol·L-1NH4Cl和0.1mol·L-1NH3·H2O等体积混合后离子浓度关系c(Cl-)>c( )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| C.常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合液溶中:c(Na+)=c(CH3COO-) |
D.常温下,在pH=1的溶液中,Fe2+、 、ClO-、Na+能大量共存 、ClO-、Na+能大量共存 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列关于平衡体系的各说法中不正确的是( )
A.在N2+3H2 2NH3的平衡体系中,缩小体积,平衡向右移动,氨的产率增加 2NH3的平衡体系中,缩小体积,平衡向右移动,氨的产率增加 |
B.在CH3COOH CH3COO﹣+H+的平衡体系中加入CH3COONa固体,平衡向左移动 CH3COO﹣+H+的平衡体系中加入CH3COONa固体,平衡向左移动 |
C.对Ca(OH)2(s) Ca2+(aq)+2OH﹣(aq),升高温度,其Ksp一定增大 Ca2+(aq)+2OH﹣(aq),升高温度,其Ksp一定增大 |
| D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 |
您最近一年使用:0次
【推荐2】已知:pAg=-lgc(AgCl),Ksp(AgCl) =1×10-12,如图是向10mLAgNO3溶液中逐渐加入0.1mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图像(实线)。根据图像所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]
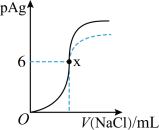

| A.原AgNO3溶液的物质的量浓度为0.1mol·L-1 |
| B.图中x点表示溶液中c(Ag+)=c(Cl-) |
| C.图中x点的坐标为(10,6) |
| D.把0.1mol·L-1的NaCl换成0.1 mol·L-1NaI,则图像在终点后变为虚线部分 |
您最近一年使用:0次

 微粒共NA个
微粒共NA个 的NaOH溶液分别滴定同体积的稀HCl溶液和稀HR溶液
的NaOH溶液分别滴定同体积的稀HCl溶液和稀HR溶液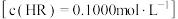 ,溶液电导率变化如图(忽略溶液体积的微小变化)。下列有关判断正确的是
,溶液电导率变化如图(忽略溶液体积的微小变化)。下列有关判断正确的是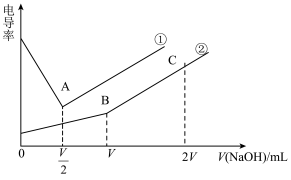
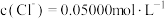

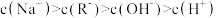
 Ca2++
Ca2++ ,其平衡常数Ksp=c(Ca2+)∙c(
,其平衡常数Ksp=c(Ca2+)∙c( ),称为CaCO3的溶度积。该温度下,向CaCO3悬浊液中加入少量水,下列叙述正确的是
),称为CaCO3的溶度积。该温度下,向CaCO3悬浊液中加入少量水,下列叙述正确的是

