1 . 在给定条件下、下列选项中所示的物质间转化均能一步实现的是
A. |
B.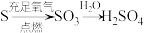 |
C.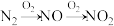 |
D.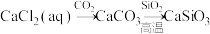 |
您最近半年使用:0次
名校
2 . 工业及汽车尾气已成为城市空气的主要污染源,研究其反应机理对于环境治理有重要意义。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=___________ kJ/mol。
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。___________ 。
②反应过程图中,虚线方框里的过程可描述为___________ 。
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是___________ 。
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和___________ 。(填化学式)
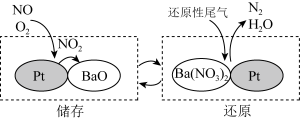
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。___________ 。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。
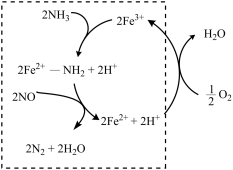
②反应过程图中,虚线方框里的过程可描述为
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是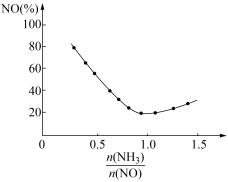
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。
您最近半年使用:0次
名校
解题方法
3 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)硅元素在元素周期表的位置是___________ 。
(2)沙子可用作建筑材料和制玻璃的原料,下列说法正确的是___________ (填字母)。
A.SiO2可用于制造光导纤维而不能直接作芯片
B.SiO2既能溶于氢氟酸、也能溶于氢氧化钠,是两性氧化物
C.普通玻璃是由SiO2、石灰石和纯碱制成的,其熔点很高
(3)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:___________ 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式___________ 。
(4)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下:
3SiO2+6C+2N2 Si3N4+6CO。若生成标准状况下33.6 L CO时,反应过程中转移的电子为
Si3N4+6CO。若生成标准状况下33.6 L CO时,反应过程中转移的电子为___________ mol。
(5)某同学设计的如图实验装置证明非金属性:N>C>Si。
你认为该同学实验能否说明N、C、Si的非金属性强弱,
若能或者不能,请用必要的文字及化学方程式说明___________ 。
(1)硅元素在元素周期表的位置是
(2)沙子可用作建筑材料和制玻璃的原料,下列说法正确的是
A.SiO2可用于制造光导纤维而不能直接作芯片
B.SiO2既能溶于氢氟酸、也能溶于氢氧化钠,是两性氧化物
C.普通玻璃是由SiO2、石灰石和纯碱制成的,其熔点很高
(3)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:
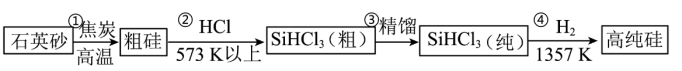
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
(4)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下:
3SiO2+6C+2N2
 Si3N4+6CO。若生成标准状况下33.6 L CO时,反应过程中转移的电子为
Si3N4+6CO。若生成标准状况下33.6 L CO时,反应过程中转移的电子为(5)某同学设计的如图实验装置证明非金属性:N>C>Si。
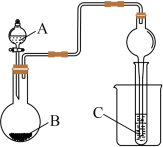
你认为该同学实验能否说明N、C、Si的非金属性强弱,
若能或者不能,请用必要的文字及化学方程式说明
您最近半年使用:0次
名校
解题方法
4 . 部分含N物质的分类与相应化合价之间的关系如图所示,下列推断正确的是
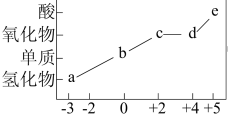
A.工业上通过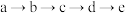 来制备 来制备 |
| B.不能通过化合反应生成c |
| C.用两根玻璃棒分别蘸取浓的a溶液和浓硫酸,将两根玻璃棒靠近时有白烟产生 |
| D.常温下,可以用铝制容器来盛装浓的e溶液 |
您最近半年使用:0次
名校
解题方法
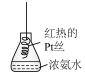
5 . 探究氨气性质的过程中,下列根据实验现象得出的结论不正确的是
| A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水 |
| B.液氨和氨水一样都是混合物 |
| C.氨气泄漏时,消防人员可喷洒大量的水,减少氨气的扩散 |
D.将红热的 丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的氧化产物为 丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的氧化产物为 ,然后被氧化为 ,然后被氧化为 |
您最近半年使用:0次
名校
解题方法
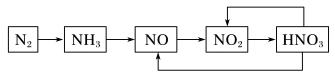
6 . 下图是氮气及几种氮的化合物间的转换关系。请回答下列问题:___________ 。
(2)工业上常用 制取
制取 ,请写出反应的化学方程式
,请写出反应的化学方程式___________ 。
(3)实验室里常用Cu与稀硝酸反应制取 ,当生成标准状况下3.36L
,当生成标准状况下3.36L 时,转移的电子数目为
时,转移的电子数目为___________ 。
(4)生产硝酸时排放的 会污染环境,一种治理方案是用氨气在催化剂作用下将
会污染环境,一种治理方案是用氨气在催化剂作用下将 还原成
还原成 ,请配平化学方程式:
,请配平化学方程式:___________ 。
___________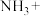 ___________
___________
 ___________
___________ ___________
___________
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中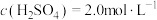 ,
,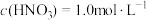 。取
。取 该混合溶液与12.8g铜粉反应,标准状况下生成
该混合溶液与12.8g铜粉反应,标准状况下生成 的体积为
的体积为___________ L。
(2)工业上常用
 制取
制取 ,请写出反应的化学方程式
,请写出反应的化学方程式(3)实验室里常用Cu与稀硝酸反应制取
 ,当生成标准状况下3.36L
,当生成标准状况下3.36L 时,转移的电子数目为
时,转移的电子数目为(4)生产硝酸时排放的
 会污染环境,一种治理方案是用氨气在催化剂作用下将
会污染环境,一种治理方案是用氨气在催化剂作用下将 还原成
还原成 ,请配平化学方程式:
,请配平化学方程式:___________
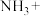 ___________
___________
 ___________
___________ ___________
___________
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中
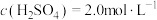 ,
,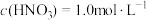 。取
。取 该混合溶液与12.8g铜粉反应,标准状况下生成
该混合溶液与12.8g铜粉反应,标准状况下生成 的体积为
的体积为
您最近半年使用:0次
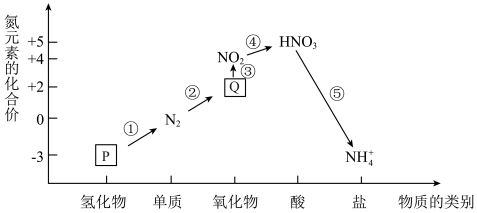
7 . “价-类”二维图是以物质的类别为横坐标,以某种元素的化合价为纵坐标,在二维平面内绘制的含有该元素物质的图像,该图是高中化学学习元素化合物知识的重要工具。氮及其部分化合物的“价-类”二维图如图所示:______ ,Q:_______ 。
(2)从氮元素化合价的角度分析,NO2具有_____ 性(选填“氧化”或“还原”、“既有氧化性又有还原性),写出一个体现出该性质的化学反应方程式_____ 。如何根据元素的化合价判断其性质____ 。
(3)P溶于水,大部分与水结合,写出结合产物的电离方程式______ 。
(4)以上①~⑤的转化过程,其中属于氮的固定的是_______ (填写编号)
(5)氮肥厂产生的氨氮废水中的氮元素多以 的形式存在,实验室里检验
的形式存在,实验室里检验 的方法
的方法_____ 。离子检验的常见方法有沉淀法、_______ (填写两种方法)。
(2)从氮元素化合价的角度分析,NO2具有
(3)P溶于水,大部分与水结合,写出结合产物的电离方程式
(4)以上①~⑤的转化过程,其中属于氮的固定的是
(5)氮肥厂产生的氨氮废水中的氮元素多以
 的形式存在,实验室里检验
的形式存在,实验室里检验 的方法
的方法
您最近半年使用:0次
名校
解题方法
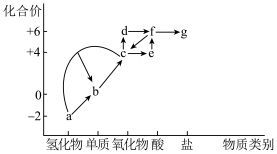
8 . “价-类”二维图是研究物质性质的重要工具,如图是硫元素的“价-类”二维图。回答下列问题:_______ 。(任写两种)
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为_______ 。
(3)溶液e久置于空气中会生成f,该过程溶液的酸性_____ (填“增强”或“减弱”)。
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液______ (填褪色或不褪色),反应的化学方程式为________ 。
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出______ (填“还原”或“漂白”)性。
(6)为避免硝酸工业尾气中氮的氧化物(以NO2为例)污染环境,可在“尾气处理装置”中盛装NaOH溶液(生成产物之一为NaNO2),相关反应的化学方程式为_____ 。
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为
(3)溶液e久置于空气中会生成f,该过程溶液的酸性
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出
(6)为避免硝酸工业尾气中氮的氧化物(以NO2为例)污染环境,可在“尾气处理装置”中盛装NaOH溶液(生成产物之一为NaNO2),相关反应的化学方程式为
您最近半年使用:0次
名校
9 . 氮及其化合物在农业、医药、国防等领域应用广泛。请回答下列问题。
(1)实验室加热 和
和 固体混合物制取
固体混合物制取 ,反应的化学方程式是
,反应的化学方程式是___________ 。
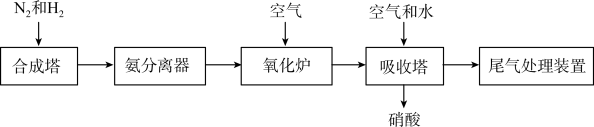
(2)工业合成氨及氨氧化制取硝酸的流程示意图如下。 ,说明
,说明 具有
具有___________ (填“氧化性”或“还原性”)。
②氧化炉中 转化为NO,发生反应的化学方程式是
转化为NO,发生反应的化学方程式是___________ 。
③吸收塔中NO最终可转化为 。通入空气是为了提供
。通入空气是为了提供___________ (填化学式)。
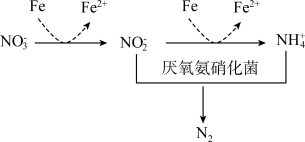
(3)氮元素含量过高会造成水体污染,添加铁粉能够提高氮的脱除率,工艺如下图所示。试从价态角度分析原因___________ 。
(1)实验室加热
 和
和 固体混合物制取
固体混合物制取 ,反应的化学方程式是
,反应的化学方程式是(2)工业合成氨及氨氧化制取硝酸的流程示意图如下。
 ,说明
,说明 具有
具有②氧化炉中
 转化为NO,发生反应的化学方程式是
转化为NO,发生反应的化学方程式是③吸收塔中NO最终可转化为
 。通入空气是为了提供
。通入空气是为了提供(3)氮元素含量过高会造成水体污染,添加铁粉能够提高氮的脱除率,工艺如下图所示。试从价态角度分析原因
您最近半年使用:0次
名校
10 . 将二氧化硫通入碳酸钠溶液的过程中,溶液中有关组分的质量分数变化如图所示。下列说法不正确 的是
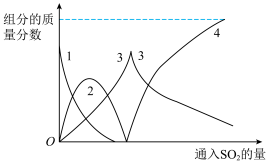
A.反应初期曲线1、2的变化主要原因是: |
B.曲线2下降的主要原因是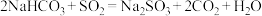 |
C.曲线3表示 变化质量分数 变化质量分数 |
D.随着二氧化硫的不断通入,溶液中最后剩余的全为 |
您最近半年使用:0次



