名校
1 . 央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的___________ (填序号)。
A.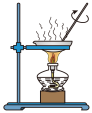 B.
B.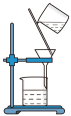 C.
C.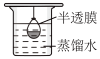
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(2)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
| A.都不稳定,密封放置会产生沉淀 | B.分散质粒子可通过滤纸 |
| C.分散质粒子可通过半透膜 | D.二者均有丁达尔效应 |
A.
 B.
B. C.
C.
您最近一年使用:0次
名校
2 . 对于成千上万、形形色色的化学物质,用分类的思想对其进行学习和研究极其重要。有以下物质,请按要求作答。
现有下列10种物质:①铝;②纯醋酸;③CO2;④H2SO4;⑤NaOH;⑥硫酸铜溶液;⑦熔融的NaCl;⑧NaHSO4;⑨硝酸钾晶体;⑩乙醇。
(1)上述物质中属于电解质的有___________ (填序号,下同);属于非电解质的有___________ ;①②⑥⑦⑨⑩六种物质中能导电的有___________ 。
(2)向⑥中加入⑤的离子方程式是___________ 。
(3)②在水中的电离方程式为___________ 。
(4)向Ba(OH)2的水溶液中逐滴滴加⑧的水溶液,当溶液恰好呈中性时NaHSO4与Ba(OH)2反应的化学计量数之比为___________ ,其离子反应方程式为___________ 。
现有下列10种物质:①铝;②纯醋酸;③CO2;④H2SO4;⑤NaOH;⑥硫酸铜溶液;⑦熔融的NaCl;⑧NaHSO4;⑨硝酸钾晶体;⑩乙醇。
(1)上述物质中属于电解质的有
(2)向⑥中加入⑤的离子方程式是
(3)②在水中的电离方程式为
(4)向Ba(OH)2的水溶液中逐滴滴加⑧的水溶液,当溶液恰好呈中性时NaHSO4与Ba(OH)2反应的化学计量数之比为
您最近一年使用:0次
名校
3 . 某同学在实验室进行如图所示实验,下列说法中不正确的是


| A.X中的溶液滴入沸水中可得到Z中液体 |
| B.X中分散系不能产生丁达尔效应 |
| C.用过滤和渗析的方法,可将Z中液体分离提纯 |
| D.Y中反应离子方程式:3CaCO3+2Fe3++3H2O=2Fe(OH)3(胶体)+3CO2↑+3Ca2+ |
您最近一年使用:0次
名校
4 . 对于反应CaH2+2H2O=Ca(OH)2+2H2↑有下列判断:①H2只是氧化产物;②H2只是还原产物;③H2O是氧化剂;④CaH2中H元素被还原;⑤此反应中的氧化产物和还原产物的分子个数之比为1:1。上述判断正确的是
| A.②④ | B.③⑤ | C.①③⑤ | D.①④⑤ |
您最近一年使用:0次
5 . FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述中不正确的是
| A.Fe(OH)3胶体、Fe(OH)3浊液均能与盐酸反应,且反应现象相同 |
| B.分别用一束光透过三种分散系,只有Fe(OH)3胶体具有丁达尔效应 |
| C.三种分散系的稳定性:FeCl3溶液>Fe(OH)3胶体>Fe(OH)3浊液 |
| D.胶体区别于其他分散系的本质特征是分散质粒子的直径在10-9-10-7m之间 |
您最近一年使用:0次
名校
解题方法
6 . 钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。
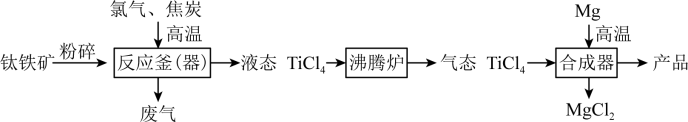
(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)反应釜中发生的反应是:2FeTiO3+7Cl2+6C 2X+2TiCl4+6CO,X的化学式是
2X+2TiCl4+6CO,X的化学式是___________ 。FeTiO3在该反应中发生了反应___________ (填“氧化”或“还原”)。
(3)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ 。由金属钛的性质可知,除去这种杂质可以用___________ 。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)反应釜中发生的反应是:2FeTiO3+7Cl2+6C
 2X+2TiCl4+6CO,X的化学式是
2X+2TiCl4+6CO,X的化学式是(3)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
您最近一年使用:0次
名校
解题方法
7 . 为确定某溶液中含有以下离子H+、Mg2+、Ba2+、Cl-、CO 、NO
、NO 中的几种,进行以下实验:
中的几种,进行以下实验:
①经测定,溶液呈强酸性;
②取部分未知溶液,加入过量NaOH溶液,有白色沉淀产生;
③取②中部分溶液,加入Na2CO3溶液,无明显现象。
分析上述实验,下面对溶液中含有离子的判断,正确的是
 、NO
、NO 中的几种,进行以下实验:
中的几种,进行以下实验:①经测定,溶液呈强酸性;
②取部分未知溶液,加入过量NaOH溶液,有白色沉淀产生;
③取②中部分溶液,加入Na2CO3溶液,无明显现象。
分析上述实验,下面对溶液中含有离子的判断,正确的是
A.一定含有H+、Mg2+、Ba2+、Cl-、NO |
B.一定含有H+、Mg2+、Cl-,一定不含有CO |
C.一定含有H+、Ba2+、NO ,一定不含有Cl- ,一定不含有Cl- |
D.一定含有H+、Mg2+,可能同时含有Cl-、NO |
您最近一年使用:0次
2023-09-22更新
|
170次组卷
|
2卷引用:江西省南昌第二中学2022-2023学年高一上学期第一次月考化学试题
名校
8 . 根据事物的某些相似性质类推其他的相似性,并预测类似的可能性,是我们经常使用的一种思维方法。以下推论正确的是
| 选项 | 实际事实 | 类推结果 |
| A | NaOH属于碱 | C2H5OH也属于碱 |
| B | CO2缓慢通入澄清石灰水中,溶液先变浑浊后变澄清 | CO2缓慢通入Ba(OH)2溶液中,溶液先变浑浊后变澄清 |
| C | 氢氧化钠能与酸反应 | 能与氢氧化钠反应的化合物都是酸 |
| D | 酸与碱发生中和反应生成盐和水 | 生成盐和水的反应都是中和反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-22更新
|
136次组卷
|
2卷引用:江西省南昌第二中学2022-2023学年高一上学期第一次月考化学试题
名校
解题方法
9 . 图中相连物质间在一定条件下可以发生反应,下表提供的四组物质符合要求的是


| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | H2 | O2 | CO2 | CuO |
| B | Mg | HCl | CuCl2 | NaOH |
| C | Ca(OH)2 | CO2 | NaOH | CuSO4 |
| D | Na2CO3 | BaCl2 | HCl | Ca(OH)2 |
| A.A | B.B | C.C | D. |
您最近一年使用:0次
2023-09-22更新
|
165次组卷
|
3卷引用:江西省南昌第二中学2022-2023学年高一上学期第一次月考化学试题
10 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态,设计并进行了如下实验:
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ (填名称),试剂2是_______ (填名称)。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与NaClO发生了化学反应。
与NaClO发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
【资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价,通常被氧化为+6价

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)写出在上述条件下Fe2+与NaClO发生反应的离子方程式:
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与NaClO发生了化学反应。
与NaClO发生了化学反应。a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
您最近一年使用:0次



