1 . 金属及其化合物转化关系是化学学习的重要内容之一,下列各组物质的转化关系不能全部通过一步反应完成的是
| A.Na→NaOH→Na2CO3→NaCl | B.Fe→FeCl3→Fe(OH)3→Fe2O3 |
| C.Al→Al2O3→Al(OH)3→AlCl3 | D.Mg→MgCl2→Mg(OH)2→MgSO4 |
您最近一年使用:0次
2023-09-04更新
|
272次组卷
|
5卷引用:上海市松江区2023届高三二模测试化学试题
名校
解题方法
2 . 将一定质量的Mg和Al的混合物投入100mL的稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示:

(1)当加入氢氧化钠溶液的体积为20mL时,溶液中的溶质有_________________ 。
(2)固体溶解时生成的气体在标准状况下的体积为____________ L。
(3)稀硫酸的物质的量浓度为____________  (结果保留一位小数)。
(结果保留一位小数)。

(1)当加入氢氧化钠溶液的体积为20mL时,溶液中的溶质有
(2)固体溶解时生成的气体在标准状况下的体积为
(3)稀硫酸的物质的量浓度为
 (结果保留一位小数)。
(结果保留一位小数)。
您最近一年使用:0次
名校
3 . 金属镁铝均为元素周期表第三周期的活泼金属,镁铝合金是合金中的一种,密度一般小于 ,具有很好的强度、刚性和尺寸稳定性,使其在交通运输、航空工业和航天工业上具有巨大的应用前景。
,具有很好的强度、刚性和尺寸稳定性,使其在交通运输、航空工业和航天工业上具有巨大的应用前景。
(1)镁铝合金的熔点和硬度与纯金属铝比较,正确的是______
(2)将等物质的量的镁和铝混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是______
(3)下列两瓶没有标签的无色透明溶液,不用任何试剂,只需互滴就能鉴别出来的是______
(4)甲、乙两烧杯中各盛有 盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2,则加入铝粉的质量为______
盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2,则加入铝粉的质量为______
(5)向硫酸铝钾 溶液中逐滴加入
溶液中逐滴加入 溶液,当
溶液,当 恰好完全沉淀时,溶液中的
恰好完全沉淀时,溶液中的 元素的存在形式为
元素的存在形式为_________ 。
 ,具有很好的强度、刚性和尺寸稳定性,使其在交通运输、航空工业和航天工业上具有巨大的应用前景。
,具有很好的强度、刚性和尺寸稳定性,使其在交通运输、航空工业和航天工业上具有巨大的应用前景。(1)镁铝合金的熔点和硬度与纯金属铝比较,正确的是______
| A.熔点高、硬度大 | B.熔点低、硬度小 | C.熔点高、硬度小 | D.熔点低、硬度大 |
A. 盐酸 盐酸 | B. 溶液 溶液 |
C. 溶液 溶液 | D. 溶液 溶液 |
| A.明矾溶液和烧碱溶液 | B.明矾溶液和盐酸 |
C.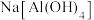 溶液和烧碱溶液 溶液和烧碱溶液 | D.盐酸与烧碱溶液 |
 盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2,则加入铝粉的质量为______
盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2,则加入铝粉的质量为______| A.1.6g | B.2.7g | C.3.6g | D.5.4g |
 溶液中逐滴加入
溶液中逐滴加入 溶液,当
溶液,当 恰好完全沉淀时,溶液中的
恰好完全沉淀时,溶液中的 元素的存在形式为
元素的存在形式为
您最近一年使用:0次
名校
4 . 在如图所示的装置中,用NaOH溶液、铁粉、稀H2SO4等试剂制备氢氧化亚铁。
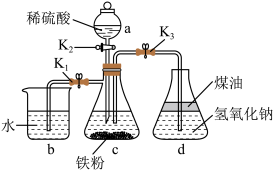
(1)仪器a的名称是 。
(2)关闭 ,打开
,打开 和
和 ,向仪器c中加入适量稀硫酸,然后关闭
,向仪器c中加入适量稀硫酸,然后关闭 ,c中有气体产生,写出装置c中发生反应的离子方程式
,c中有气体产生,写出装置c中发生反应的离子方程式______ ,如此操作的目的是________ 。
(3)当仪器b中产生均匀气泡后的操作是______________ ,完成该操作后仪器c、d中出现的实验现象是___________ 。
(4)Fe3+离子具有一定的氧化性,向FeCl3溶液中通入SO2至饱和,溶液逐渐由黄色变为浅绿色,向反应后的溶液中滴入BaCl2溶液,有白色沉淀生成,写出该反应的离子方程式____________ 。

(1)仪器a的名称是 。
| A.普通漏斗 | B.长颈漏斗 | C.分液漏斗 | D.球形漏斗 |
 ,打开
,打开 和
和 ,向仪器c中加入适量稀硫酸,然后关闭
,向仪器c中加入适量稀硫酸,然后关闭 ,c中有气体产生,写出装置c中发生反应的离子方程式
,c中有气体产生,写出装置c中发生反应的离子方程式(3)当仪器b中产生均匀气泡后的操作是
(4)Fe3+离子具有一定的氧化性,向FeCl3溶液中通入SO2至饱和,溶液逐渐由黄色变为浅绿色,向反应后的溶液中滴入BaCl2溶液,有白色沉淀生成,写出该反应的离子方程式
您最近一年使用:0次
名校
5 . 已知X、Y、Z、M四种主族元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子,其中MY2可以使红色的品红溶液褪色。请回答下列问题:
(1)Y在元素周期表中的位置为_______ ,写出离子化合物ZX的电子式_______ ;
(2)由X、Y、Z、M四种元素组成的一种固体化合物,属于强电解质,溶于水的过程中破坏了_______。
(1)Y在元素周期表中的位置为
(2)由X、Y、Z、M四种元素组成的一种固体化合物,属于强电解质,溶于水的过程中破坏了_______。
| A.离子键 | B.金属键 | C.共价键 | D.分子间作用力 |
您最近一年使用:0次
名校
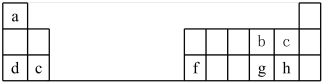
6 . 元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分。
(2)a-h元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式)。
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为___________ 。
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是___________ 。
(5)d元素的简单离子的结构示意图为___________ 。
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为___________ 。
(7)若d单质着火,可用于灭火的物质是___________。
(8)下列关于元素周期表的叙述正确的是___________。
| A.第三周期第6族 | B.第三周期VI主族 |
| C.第三周期第6A族 | D.第三周期VIA族 |
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是
(5)d元素的简单离子的结构示意图为
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为
(7)若d单质着火,可用于灭火的物质是___________。
| A.自来水 | B.CO2 | C.干沙子 | D.湿抹布 |
| A.元素周期表中所含元素最多的族是BVII族 |
| B.IA族的元素全部是金属元素 |
| C.在元素周期表中金属与非金属的分界处可以找到半导体材料 |
| D.只有IIA族元素的原子最外层有2个电子 |
您最近一年使用:0次
2023-04-25更新
|
192次组卷
|
2卷引用:上海市松江二中2022-2023学年高二下学期期中合格考化学试题
名校
解题方法
7 . 自然界中的含硫物质通过各种化学过程建立起硫循环,其循环过程如下图:

(1)从图中可以看出,火山喷发产生的气体中有 H2S。写出 H2S 的结构式___________ 。
(2)结合图中含硫物质,分析硫常见的化合价除了 0 价,还有___________ ,试写出一个含有最高价硫元素的物质和最低价硫元素的物质之间反应的化学方程式___________ 。
(3)除了硫,氮也是自然界常见的物质,含氮废水进入水体会对环境造成污染。某学生社团用铝将NO 还原为N2,从而消除污染。下列离子方程式:
还原为N2,从而消除污染。下列离子方程式:
① 标出该反应中的电子转移方向和数目_________
② 该反应中,被还原的元素是___________ ,每生成 1mol N2,转移的电子数目是___________ 。

(1)从图中可以看出,火山喷发产生的气体中有 H2S。写出 H2S 的结构式
(2)结合图中含硫物质,分析硫常见的化合价除了 0 价,还有
(3)除了硫,氮也是自然界常见的物质,含氮废水进入水体会对环境造成污染。某学生社团用铝将NO
 还原为N2,从而消除污染。下列离子方程式:
还原为N2,从而消除污染。下列离子方程式:
① 标出该反应中的电子转移方向和数目
② 该反应中,被还原的元素是
您最近一年使用:0次
名校
解题方法
8 . 奥司他韦的分子式为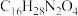 ,对由H5N1、H9N2等亚型流感病毒引起的流行性感冒有治疗和预防作用。奥司他韦所属的物质类别是
,对由H5N1、H9N2等亚型流感病毒引起的流行性感冒有治疗和预防作用。奥司他韦所属的物质类别是
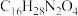 ,对由H5N1、H9N2等亚型流感病毒引起的流行性感冒有治疗和预防作用。奥司他韦所属的物质类别是
,对由H5N1、H9N2等亚型流感病毒引起的流行性感冒有治疗和预防作用。奥司他韦所属的物质类别是| A.单质 | B.氧化物 | C.无机物 | D.有机物 |
您最近一年使用:0次
2023-04-16更新
|
221次组卷
|
3卷引用:上海市松江一中2023-2024学年高一上学期期中考试化学试题
上海市松江一中2023-2024学年高一上学期期中考试化学试题浙江省宁波三锋教研联盟2022-2023学年高一下学期期中联考化学试题(已下线)【2023】【高一下】【期中考】【宁波三锋】【高中化学】【李鼎收集】
名校
解题方法
9 . 四种短周期元素 W、X、Y、Z 的核电荷数依次增大,它们的相关信息如下表。
完成下列填空:
(1)W 所形成的负离子的电子式为___________ ,该离子核外能量最高的电子位于___________ (填电子层符号)层。
(2)X 用于测定文物年代的 X 核素的符号为___________ ;该核素核内中子数与质子数之差为________ 。
(3)证明Y的气态氢化物极易溶于水的实验装置如所示。下列气体和液体的组合中不可能形成喷泉的是 _______

(4)Z 在元素周期表中的位置是___________ ,试比较元素 X 与Z 的简单氢化物稳定性大小___________ (用化学式表示)。
(5)通过如图装置可以比较X、Y、Z三种元素的非金属性强弱。已知硅酸是一种不溶于水的白色物质,则溶液Ⅰ的溶质是___________ (填化学式);进行实验时溶液Ⅲ中的现象是___________ 。有人认为上述装置存在缺陷,无法达到实验目的,请写出改进的措施 ______ 。

| 元素 | W | X | Y | Z |
| 相关信息 | 原子得到 1 个电子后达到稀有气体稳定结构 | 某种核素常用于测定文物年代 | 气态氢化物极易溶于水 | 原子最外层电子是最内层电子的 2 倍 |
(1)W 所形成的负离子的电子式为
(2)X 用于测定文物年代的 X 核素的符号为
(3)证明Y的气态氢化物极易溶于水的实验装置如所示。下列气体和液体的组合中不可能形成喷泉的是 _______

| A.HCl 和 H2O | B.O2和 H2O |
| C.HCl 和 AgNO3溶液 | D.CO2和 NaOH 溶液 |
(5)通过如图装置可以比较X、Y、Z三种元素的非金属性强弱。已知硅酸是一种不溶于水的白色物质,则溶液Ⅰ的溶质是

您最近一年使用:0次
名校
10 . 下列性质的比较,不能用元素周期律解释的是
| A.酸性:HClO4>H2SO4>H2SiO3 | B.熔点:SiO2>CO2 |
| C.热稳定性:H2O>H2S>SiH4 | D.非金属性:F>O>N |
您最近一年使用:0次



