名校
解题方法
1 . 某校化学兴趣小组的同学拟通过实验来探究菠菜中的营养成分。已知信息:
①菠菜中含有草酸,草酸具有还原性。
②菠菜中含有丰富的铁元素,主要以难溶的FeC2O4形式存在,其中铁元素为+2价。
⑧赤血盐K3[Fe(CN)6]用于检验Fe2+,产生特征蓝色沉淀。
Ⅰ.水煮检验法:

(1)操作i中起分离作用的仪器名称为_____________ 。
(2)溶液A中未能检测出Fe2+的可能原因是__________ 。
Ⅱ.灼烧检验法:
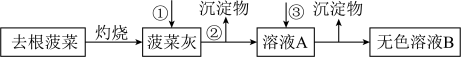
(3)向菠菜灰中加入盐酸浸取后进行操作②,下列操作不规范的有_________。
(4)操作⑧加入活性炭的作用是_____________ 。
(5)甲同学取少量溶液B,滴加酸性KMnO4溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有Fe2+。乙同学认为甲同学的实验方法不严谨,理由是:______________ 。
Ⅲ.分光光度法

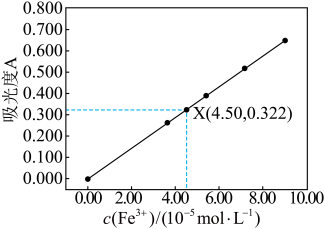
(6)该小组同学利用分光光度法来进行定量测定。已知溶液的吸光度A与溶液中c(Fe3+)关系如下图。该小组通过处理上述40 mL溶液使其中的铁元素全部转化为Fe3+,从中取出10 mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量____________ mg/100 g。(结果保留三位小数)
①菠菜中含有草酸,草酸具有还原性。
②菠菜中含有丰富的铁元素,主要以难溶的FeC2O4形式存在,其中铁元素为+2价。
⑧赤血盐K3[Fe(CN)6]用于检验Fe2+,产生特征蓝色沉淀。
Ⅰ.水煮检验法:

(1)操作i中起分离作用的仪器名称为
(2)溶液A中未能检测出Fe2+的可能原因是
Ⅱ.灼烧检验法:

(3)向菠菜灰中加入盐酸浸取后进行操作②,下列操作不规范的有_________。
| A.玻璃棒用作引流 |
| B.用玻璃棒在漏斗中轻轻搅动以加快过滤速度 |
| C.将滤纸湿润,使其紧贴漏斗壁 |
| D.漏斗末端颈尖未紧靠烧杯内壁 |
(5)甲同学取少量溶液B,滴加酸性KMnO4溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有Fe2+。乙同学认为甲同学的实验方法不严谨,理由是:
Ⅲ.分光光度法

(6)该小组同学利用分光光度法来进行定量测定。已知溶液的吸光度A与溶液中c(Fe3+)关系如下图。该小组通过处理上述40 mL溶液使其中的铁元素全部转化为Fe3+,从中取出10 mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量

您最近一年使用:0次
名校
解题方法
2 . 2020年,嫦娥五号的顺利发射,预示着中国对月球的探索更进一步。

月球土壤中富含铁元素,某难溶固体化合物A仅由3种元素组成,科学研究小组按如下流程探究其组成。
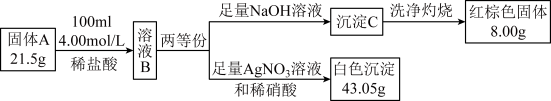
已知:A与稀盐酸恰好完全反应,且溶液B只含一种溶质。
(1)固体化合物A所含元素有______ (填元素符号)。
(2)在有氧条件下,Fe3O4 在含Cl-溶液中会转化成固体A且得到的溶液呈碱性,写出该反应的离子方程式___________ 。
(3)某同学将上述流程中所得的红棕色固体与一定量H2进行反应,取少许反应后的固体,溶于足量稀盐酸中,再向其中滴加硫氰化钾溶液,溶液未变红。据此,该同学得出结论:此红棕色固体已与H2反应完全。你认为该同学的结论是否严谨?____________ (填“是”或“否”")。请结合离子方程式说明原因____________ 。

月球土壤中富含铁元素,某难溶固体化合物A仅由3种元素组成,科学研究小组按如下流程探究其组成。

已知:A与稀盐酸恰好完全反应,且溶液B只含一种溶质。
(1)固体化合物A所含元素有
(2)在有氧条件下,Fe3O4 在含Cl-溶液中会转化成固体A且得到的溶液呈碱性,写出该反应的离子方程式
(3)某同学将上述流程中所得的红棕色固体与一定量H2进行反应,取少许反应后的固体,溶于足量稀盐酸中,再向其中滴加硫氰化钾溶液,溶液未变红。据此,该同学得出结论:此红棕色固体已与H2反应完全。你认为该同学的结论是否严谨?
您最近一年使用:0次
名校
解题方法
3 . 由我国自主研发的“奋斗者号潜水艇在大平洋马里亚纳海沟成功坐底,创造了中国载人深潜的新纪录。

(1)过氧化钠可用作潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:______________ ,该反应中生成1 mol O2转移的电子数为____________ 。
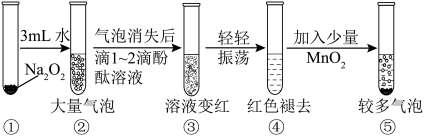
(2)某实验小组通过如图所示实验,探究Na2O2与水的反应,下列说法正确的是_______。 (双选)

(1)过氧化钠可用作潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:
(2)某实验小组通过如图所示实验,探究Na2O2与水的反应,下列说法正确的是_______。 (双选)

| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
| D.⑤中MnO2的主要作用是验证溶液中存在过氧化氢 |
您最近一年使用:0次
名校
解题方法
4 . 某化学兴趣小组据用金属钠和空气制备纯度较高的Na2O2(N2不与金属钠反应),可利用的装置如下,回答下列问题:

(1)装置Ⅳ中盛放的药品是________ ,若没有该装置可能导致生成的Na2O2中含有碳酸钠,其反应方程式为______________ 。
(2)若规定气体的气流方向从左到右,则各仪器接口的标号字母(a、b.....)顺序应为:空气进入h→___ →d。
(3)装置Ⅱ的作用是____________ 。
(4)该兴趣小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量 粉末,又有气泡产生。
粉末,又有气泡产生。
①酚酞溶液变红的原因是_________ ,红色褪去的可能原因是___________ 。设计一个简单的实验方案证明你的猜想_______________ 。
②加入 反应的化学方程式为
反应的化学方程式为______________ 。

(1)装置Ⅳ中盛放的药品是
(2)若规定气体的气流方向从左到右,则各仪器接口的标号字母(a、b.....)顺序应为:空气进入h→
(3)装置Ⅱ的作用是
(4)该兴趣小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量
 粉末,又有气泡产生。
粉末,又有气泡产生。①酚酞溶液变红的原因是
②加入
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
2023-06-23更新
|
261次组卷
|
2卷引用:上海市控江中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
5 . 下图中甲是演示金属钠与水反应的实验装置,为收集并检验气体产物,某兴趣小组将甲装置改进成如图中乙或丙所示的装置,请根据要求回答下列问题。
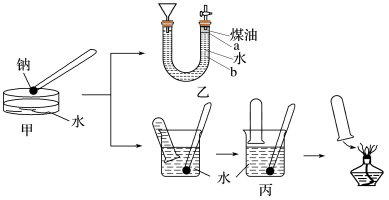
(1)写出钠与水反应的离子方程式:___________ 。和铝相比,钠与水反应更剧烈的原因是___________ (从原子结构的角度进行解释说明)。
(2)若按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是________。
(3)用乙装置实验,点燃气体产物时,是否需要检验纯度?___ (填“是“或“否”)。
(4)按图丙所示方法来收集产生的气体,需将钠用某种金属包好,再放入水中。取相同质量的钠按下列两种情况收集产生的气体:①用扎有多个小孔的铝箔包住钠②用扎有多个小孔的铜箔包住钠,在相同条件下的体积关系是________ 。
A.二者收集气体一样多 B.①收集气体体积较大 C.②收集气体体积较大

(1)写出钠与水反应的离子方程式:
(2)若按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是________。
| A.钠块始终保持在煤油中的a处,直至完全消失 |
| B.钠处于煤油和水的交界处上下浮动 |
| C.随反应的进行煤油与胶塞处液面下降,漏斗中液面上升 |
| D.最终钠块在煤油中燃烧起来 |
(4)按图丙所示方法来收集产生的气体,需将钠用某种金属包好,再放入水中。取相同质量的钠按下列两种情况收集产生的气体:①用扎有多个小孔的铝箔包住钠②用扎有多个小孔的铜箔包住钠,在相同条件下的体积关系是
A.二者收集气体一样多 B.①收集气体体积较大 C.②收集气体体积较大
您最近一年使用:0次
6 . 纳米材料一直是人们研究的重要课题,例如纳来级Fe粉表面积大,具有超强的磁性,高效的催化性等优良性质。
Ⅰ.实验室采用气相还原法制备纳米级Fe,其流程如图所示:____________ 。
Ⅱ.查阅资料得知:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570°C时生成FeO,高于570°C时生成Fe3O4。甲同学用图甲所示装置进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。________________ 。
(3)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。丙同学认为乙同学的结论不正确,他的理由是_________ (用简要文字描述)。
(4)丁同学称取5.60gFe粉,用乙装置反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为_______ (结果保留三位有效数字)。
Ⅰ.实验室采用气相还原法制备纳米级Fe,其流程如图所示:
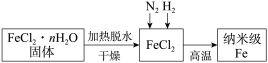
Ⅱ.查阅资料得知:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570°C时生成FeO,高于570°C时生成Fe3O4。甲同学用图甲所示装置进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。

(3)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后得到的黑色粉末X(假定为均匀的)。取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| Ⅱ | 向实验Ⅰ得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
(4)丁同学称取5.60gFe粉,用乙装置反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为
您最近一年使用:0次
7 . 家庭常用的除湿剂
氯化钙的用途广泛。在生产生活中常被用做干燥剂 ,因其溶解放热 可用于制作自加热罐头,也可用于食品添加剂等。
(1)常见的干燥剂
(2)已知市售氯化钙除湿剂主要成分为CaCl2·2H2O
①确认该除湿剂中的Cl-。简述检验Cl-的方法:___________ 。
②如图是某氯化钙除湿剂受热时固体质量的变化曲线,已知剩余固体全部为CaCl2,该除湿剂的纯度为___________ 。(保留3位小数)

(3)探究氯化钙除湿剂的使用过程
①如图是挂式家用氯化钙除湿剂装置示意图。

下表是CaCl2溶解度表。
氯化钙除湿剂吸水后变成溶液进入集水区,但使用时发现即使室温变化不大时,在集水区也会有晶体析出,请结合溶解度表和题给CaCl2性质,尝试解释上述现象的原因。___________ 。
②氯化钙除湿剂说明中写道:不慎渗漏后可用小苏打 水擦拭。取一定量集水区溶液于试管中,加入0.5mol/L的NaHCO3溶液,有白色沉淀和无色气体生成,该气体能使澄清石灰水变浑浊,请写出试管中发生反应的离子方程式。___________ 。(杂质不与NaHCO3溶液反应)
氯化钙的用途广泛。在生产生活中常被用做
(1)常见的干燥剂
| 浓H2SO4 | 有强腐蚀性,不适合家庭除湿。 ①下列不可用浓H2SO4干燥的气体是 A.CO B.NH3 C.H2S D.H2 |
| 碱石灰 | 主要成分为氧化钙和氢氧化钠 ②实验中常置于如图所示  |
| 铁粉 | 可用于食品干燥,称为“双吸剂”。 ③除吸收水分之外,还可吸收 A.CO2 B.N2 C.O2 |
| 氯化钙 | ④吸水性强,可用于家庭除湿。CaCl2 A.是离子化合物 B.两种微粒核外电子排布不同 C.是漂白粉的有效成分 D.是粗盐易潮解的原因之一 |
①确认该除湿剂中的Cl-。简述检验Cl-的方法:
②如图是某氯化钙除湿剂受热时固体质量的变化曲线,已知剩余固体全部为CaCl2,该除湿剂的纯度为

(3)探究氯化钙除湿剂的使用过程
①如图是挂式家用氯化钙除湿剂装置示意图。

下表是CaCl2溶解度表。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度/g | 59.5 | 64.7 | 74.5 | 100 | 128 | 137 | 147 |
②氯化钙除湿剂说明中写道:不慎渗漏后可用
您最近一年使用:0次
名校
8 . 化学小组实验探究 与
与 溶液的反应。
溶液的反应。
实验一:用如图装置制备 ,并将足量
,并将足量 通入
通入 溶液中,
溶液中,迅速反应 ,得到无色溶液A和白色沉淀B(省略夹持、加热仪器)。
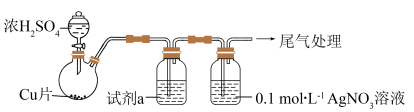
(1)制备的 中会混有少量的
中会混有少量的 ,原因可能为
,原因可能为_______ ,为了排除 的干扰,试剂a可以为
的干扰,试剂a可以为_______ 。
A. 溶液 B.饱和
溶液 B.饱和 溶液
溶液
C.饱和 溶液 D.饱和
溶液 D.饱和 溶液
溶液
实验二:验证白色沉淀B的成分。
已知: 微溶于水,
微溶于水, 难溶于水
难溶于水
分析:沉淀B可能为 、
、 或两者混合物。滴加氨水可释出其负离子,便于后续检验。
或两者混合物。滴加氨水可释出其负离子,便于后续检验。
相关反应为:①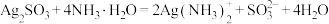 ,②
,②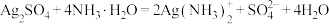 。
。
流程如下:

(2)欲检验溶液C中加入的 是否已经过量,请简述实验方法:
是否已经过量,请简述实验方法:_______ 。
(3)沉淀F是_______ ,沉淀D中主要含 ,理由是
,理由是_______ 。向滤液E中加入 溶液,产生的现象是
溶液,产生的现象是_______ ,可进一步证实B中含 。
。
实验三:探究 的产生途径。
的产生途径。
猜想1:实验一中, 在
在 溶液中被氧化生成
溶液中被氧化生成 ,随沉淀B进入D。
,随沉淀B进入D。
猜想2:实验二中, 被氧化为
被氧化为 进入D。
进入D。
(4)取少量溶液A,滴加过量盐酸,产生白色沉淀。静置后,取上层清液再滴加 溶液,未出现白色沉淀,可判断猜想1不合理。理由是:
溶液,未出现白色沉淀,可判断猜想1不合理。理由是:_______ 。根据以上实验结果,则可得出沉淀B的成分是_______ 。
(5)实验探究可知, 在
在_______ (选填“酸性”“中性”“碱性”)溶液中更易被氧化为 。
。
 与
与 溶液的反应。
溶液的反应。实验一:用如图装置制备
 ,并将足量
,并将足量 通入
通入 溶液中,
溶液中,
(1)制备的
 中会混有少量的
中会混有少量的 ,原因可能为
,原因可能为 的干扰,试剂a可以为
的干扰,试剂a可以为A.
 溶液 B.饱和
溶液 B.饱和 溶液
溶液C.饱和
 溶液 D.饱和
溶液 D.饱和 溶液
溶液实验二:验证白色沉淀B的成分。
已知:
 微溶于水,
微溶于水, 难溶于水
难溶于水分析:沉淀B可能为
 、
、 或两者混合物。滴加氨水可释出其负离子,便于后续检验。
或两者混合物。滴加氨水可释出其负离子,便于后续检验。相关反应为:①
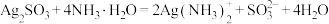 ,②
,②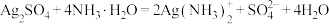 。
。流程如下:

(2)欲检验溶液C中加入的
 是否已经过量,请简述实验方法:
是否已经过量,请简述实验方法:(3)沉淀F是
 ,理由是
,理由是 溶液,产生的现象是
溶液,产生的现象是 。
。实验三:探究
 的产生途径。
的产生途径。猜想1:实验一中,
 在
在 溶液中被氧化生成
溶液中被氧化生成 ,随沉淀B进入D。
,随沉淀B进入D。猜想2:实验二中,
 被氧化为
被氧化为 进入D。
进入D。(4)取少量溶液A,滴加过量盐酸,产生白色沉淀。静置后,取上层清液再滴加
 溶液,未出现白色沉淀,可判断猜想1不合理。理由是:
溶液,未出现白色沉淀,可判断猜想1不合理。理由是:(5)实验探究可知,
 在
在 。
。
您最近一年使用:0次
名校
9 . 酸雨是全球三大环境危害之一,根据其所带的酸性物质不同,酸雨分为硫酸型酸雨和硝酸型酸雨。
(1)酸雨的标准是:降水的pH_______ 。测得某地雨水样本中的硫酸浓度为 ,计算pH=
,计算pH=_______ (计算结果保留一位小数)。
(2)写出硫酸型酸雨形成过程的两种途径(用化学方程式表示):①_______ 、_______ ;②_______ 、_______ 。
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:

写出装置C中反应的离子方程式_______ 。该流程中可以循环利用的物质是_______ (填写化学式)。
(4)还有学者提出利用 、
、 等离子的催化作用,常温下将
等离子的催化作用,常温下将 氧化成
氧化成 而实现
而实现 的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中
的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成
氧化成 的转化率。(转化率=
的转化率。(转化率= ×100%)
×100%)

该小组采用下图装置在实验室测定模拟烟气中 的体积分数,X溶液可以是_______。
的体积分数,X溶液可以是_______。

(5)若上述实验是在标准状况下进行的,欲测定转化器中 氧化成
氧化成 的转化率。已知气体流速,还需测定的数据有
的转化率。已知气体流速,还需测定的数据有_______ 、_______ 。
(1)酸雨的标准是:降水的pH
 ,计算pH=
,计算pH=(2)写出硫酸型酸雨形成过程的两种途径(用化学方程式表示):①
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:

写出装置C中反应的离子方程式
(4)还有学者提出利用
 、
、 等离子的催化作用,常温下将
等离子的催化作用,常温下将 氧化成
氧化成 而实现
而实现 的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中
的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中 氧化成
氧化成 的转化率。(转化率=
的转化率。(转化率= ×100%)
×100%)
该小组采用下图装置在实验室测定模拟烟气中
 的体积分数,X溶液可以是_______。
的体积分数,X溶液可以是_______。
| A.碘的淀粉溶液 | B.酸性高锰酸钾溶液 |
| C.氢氧化钠溶液 | D.氯化钡溶液 |
 氧化成
氧化成 的转化率。已知气体流速,还需测定的数据有
的转化率。已知气体流速,还需测定的数据有
您最近一年使用:0次
名校
解题方法
10 .  的转化目前主要有以下两种方法:
的转化目前主要有以下两种方法:
(1)方法①的化学方程式是_______ 。
(2)方法②,将 和
和 的混合气体通入
的混合气体通入 、
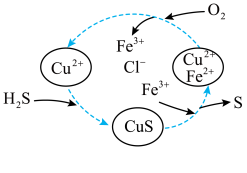
、 的混合溶液中反应回收S,物质转化如图所示。下列说法不正确的是_______。
的混合溶液中反应回收S,物质转化如图所示。下列说法不正确的是_______。
 的转化目前主要有以下两种方法:
的转化目前主要有以下两种方法:| 方法① | 克劳斯燃烧法 | 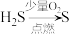 |
| 方法② | 铁盐、铜盐氧化法 |  |
(2)方法②,将
 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收S,物质转化如图所示。下列说法不正确的是_______。
的混合溶液中反应回收S,物质转化如图所示。下列说法不正确的是_______。
A. 和 和 反应的离子方程式为 反应的离子方程式为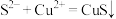 |
B. 在转化过程中发生的反应为 在转化过程中发生的反应为 |
C.整个反应过程中溶液的pH值变小(不考虑产生 的稀释效果) 的稀释效果) |
D.提高混合气体中 的比例可防止生成的硫单质中混有 的比例可防止生成的硫单质中混有 |
您最近一年使用:0次



