名校
1 . Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况,设计了如图所示装置进行有关实验。___________ ;实验开始时,先打开a、b产生氢气,一段时间后,再点燃酒精灯加热,目的是___________ 。
(2)实际实验过程中观察到Na2O2熔化后,很快变成白色粉末,但干燥管内硫酸铜并未变成蓝色。则Na2O2与H2反应的化学方程式为___________ 。
(3)出于实验安全考虑,实验结束时___________ 。
A.应先关闭活塞b,再移去酒精灯
B.应先移去酒精灯,再关闭活塞b
C.A、B均可以

(2)实际实验过程中观察到Na2O2熔化后,很快变成白色粉末,但干燥管内硫酸铜并未变成蓝色。则Na2O2与H2反应的化学方程式为
(3)出于实验安全考虑,实验结束时
A.应先关闭活塞b,再移去酒精灯
B.应先移去酒精灯,再关闭活塞b
C.A、B均可以
您最近一年使用:0次
2023-07-16更新
|
207次组卷
|
3卷引用:上海市大同中学2022-2023学年高一下学期期末考试化学试题
上海市大同中学2022-2023学年高一下学期期末考试化学试题(已下线)专题05 氧化还原反应和离子反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(上海专用)上海市建平中学2023-2024学年高一下学期期中教学质量检测化学试卷
名校
解题方法
2 . 某同学为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。

(1)实验Ⅰ、Ⅱ(盐酸足量且固体质量相同)中能够达到实验目的的是___________ (填装置序号)。
(2)实验Ⅲ、Ⅳ均能鉴别这两种物质,写出所发生的共同反应的化学方程式:___________ 、___________ 。
(3)与实验Ⅲ相比,实验Ⅳ的优点是___________。
(4)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________ 。

(1)实验Ⅰ、Ⅱ(盐酸足量且固体质量相同)中能够达到实验目的的是
(2)实验Ⅲ、Ⅳ均能鉴别这两种物质,写出所发生的共同反应的化学方程式:
(3)与实验Ⅲ相比,实验Ⅳ的优点是___________。
| A.Ⅳ比Ⅲ复杂 | B.Ⅳ比Ⅲ安全 |
| C.Ⅳ比Ⅲ操作简便 | D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
A.切开的金属Na暴露在空气中,光亮的表面逐渐变暗,发生的反应为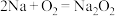 |
B.Na与稀硫酸反应的离子方程式为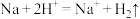 |
| C.4.6gNa与O2完全反应,生成7g产物时失去电子的物质的量为0.2mol |
| D.将少量Na投入到稀的CuSO4溶液中,会析出红色金属 |
您最近一年使用:0次
2023-07-16更新
|
226次组卷
|
2卷引用:上海市大同中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
4 . 下列各组中的两物质作用时,反应条件或反应物用量的改变,对生成物没有影响的是
| A.Na2O和CO2 | B.Na和O2 | C.NaOH与CO2 | D.碳与O2 |
您最近一年使用:0次
2023-07-16更新
|
249次组卷
|
3卷引用:上海市大同中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
5 . 按图所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列两种情况:
①用铝箔包住钠、②用铜箔包住钠。则收集产生的气体在相同条件下体积的关系是

①用铝箔包住钠、②用铜箔包住钠。则收集产生的气体在相同条件下体积的关系是

| A.二者收集气体一样多 | B.①收集气体体积较大 |
| C.②收集气体体积较大 | D.无法确定 |
您最近一年使用:0次
名校
解题方法
6 . 有一包氧化铁与铝粉的混合物,其中含有少量不溶于酸和碱的杂质,为了制取绿矾(FeSO4·xH2O)晶体,某同学设计实验方案如下。
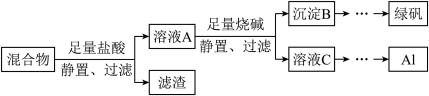
(1)沉淀B的化学式是___________ ,若要制得绿矾,还需要的化学试剂有___________ (填编号)。
a.硫酸铜 b.硫酸 c.过氧化氢 d.铁粉
(2)溶液C中含有多种溶质,除了氯化钠以外,属于盐类的有___________ (填化学式)。
(3)溶液C经过一系列操作可以转化成氧化铝,用氧化铝制取金属铝可以选择_________

(1)沉淀B的化学式是
a.硫酸铜 b.硫酸 c.过氧化氢 d.铁粉
(2)溶液C中含有多种溶质,除了氯化钠以外,属于盐类的有
(3)溶液C经过一系列操作可以转化成氧化铝,用氧化铝制取金属铝可以选择_________
| A.氢气还原法 | B.电解法 | C.加热分解法 | D.铝热法 |
您最近一年使用:0次
名校
解题方法
7 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:

(1)空白处还需加入的试剂为___________ 。
(2)写出一种铝热反应的实际应用___________ 。

(1)空白处还需加入的试剂为
(2)写出一种铝热反应的实际应用
您最近一年使用:0次
8 . 用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是
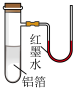

| A.实验中发生的反应都是氧化还原反应 | B.铝是一种较活泼的金属 |
| C.铝与氧气反应放出热量 | D.铝片上生成的白毛是氧化汞 |
您最近一年使用:0次
名校
解题方法
9 . 为了检验FeCl2溶液是否被氧化,可向溶液中加入
| A.新制氯水 | B.铁片 | C.KSCN溶液 | D.石蕊溶液 |
您最近一年使用:0次
名校
10 . 元素周期表的表达形式有多种,但都能表示出元素的周期性变化规律,请回答下列问题:
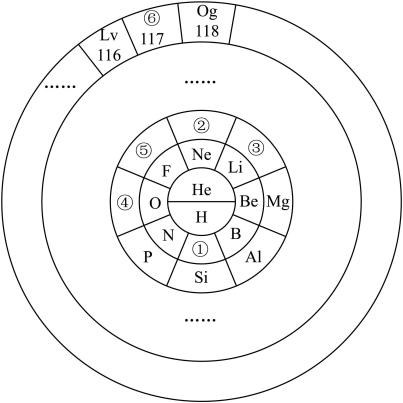
(1)①与④元素形成的化合物属于___________ 晶体。
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:__________ 。
(3)②号元素为___________ (填元素符号)。请写出1个与②核外电子数相同的简单离子组成的化合物的化学式:___________ 。其中存在的化学键属于___________ 键,该物质在熔融状态下___________ 导电(填“能”或“不能”)。
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:___________ ,将反应所得混合物溶于水,得到浅绿色的溶液,请写出相关的离子方程式:___________ 。
(5)其中非金属性④___________ ⑤(填“>”或“<”),请用一个化学方程式证明___________ 。
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为___________ ,根据元素的周期性规律,以下推测正确的是________
A.单质在常温下为气体 B.气态氢化物的稳定性较好
C.离子具有强还原性 D.半径大于⑤

(1)①与④元素形成的化合物属于
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:
(3)②号元素为
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:
(5)其中非金属性④
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为
A.单质在常温下为气体 B.气态氢化物的稳定性较好
C.离子具有强还原性 D.半径大于⑤
您最近一年使用:0次



