解题方法
1 . 某小组同学探究卤族元素性质递变规律,设计如下实验:
(1)实验①的离子方程式为_______ 。实验②的现象是_______ 。
(2)综合实验①②③,Cl2、Br2、I2单质的氧化性由强到弱的顺序是_______ (用化学式表示);从原子结构的角度解释上述递变规律。_______
(3)实验中加入CCl4萃取的目的是_______ ;CCl4可以作为萃取剂的原因是_______ 。
| 序号 | 过程 | 现象 | 结论 |
| ① | 向NaBr溶液中加入少量氯水,再加入CCl4,振荡后静置 | 液体分层,下层呈红棕色 | 氧化性:Cl2>Br2 |
| ② | 向KI溶液中加入少量氯水,再加入CCl4,振荡后静置 | 氧化性:Cl2>I2 | |
| ③ | 向KI溶液中加入少量溴水,再加入CCl4,振荡后静置 |
(2)综合实验①②③,Cl2、Br2、I2单质的氧化性由强到弱的顺序是
(3)实验中加入CCl4萃取的目的是
您最近一年使用:0次
2 . 元素周期表是元素周期律的具体表现形式,是学习和研究化学的重要工具,下图是元素周期表的一部分。

(1)氧元素在周期表中的位置是第_______ 周期_______ 族,氧原子的电子式为_______ 。
(2)某元素的结构示意图为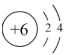 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号_______ 。
(3)元素性质呈现周期性变化的根本原因是_______。

(1)氧元素在周期表中的位置是第
(2)某元素的结构示意图为
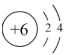 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号(3)元素性质呈现周期性变化的根本原因是_______。
| A.元素相对原子质量的递增 |
| B.元素原子半径呈现周期性变化 |
| C.元素原子核外电子排布呈现周期性变化 |
| D.元素金属性和非金属性呈现周期性变化 |
您最近一年使用:0次
9-10高一·浙江·阶段练习
名校
解题方法
3 . 已知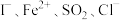 和
和 均有还原性,它们在酸性溶液中还原性的强弱顺序为
均有还原性,它们在酸性溶液中还原性的强弱顺序为 ,则下列反应不能发生的是
,则下列反应不能发生的是
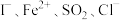 和
和 均有还原性,它们在酸性溶液中还原性的强弱顺序为
均有还原性,它们在酸性溶液中还原性的强弱顺序为 ,则下列反应不能发生的是
,则下列反应不能发生的是A. |
B. |
C. |
D.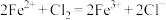 |
您最近一年使用:0次
2023-11-11更新
|
338次组卷
|
38卷引用:上海市进才中学2022-2023学年高一上学期期末考试化学试题
上海市进才中学2022-2023学年高一上学期期末考试化学试题第一章 化学物质及其变化 第4讲 氧化还原反应黑龙江省哈尔滨市第三中学校 2023-2024 学年高一上学期第一次验收考试化学试题湖北省宜昌市长阳土家族自治县第一高级中学2023-2024学年高一上学期9月月考化学试题广东省深圳市龙华中学2023-2024学年高一上学期12月期中考试化学试题山西省太原市第四十八中学校2023-2024学年高一上学期第一次月考化学试题福建省厦门双十中学2023-2024学年高一上学期期中考试化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷(已下线)09-10年瑞安中学高一提前招阶段性检测化学卷(已下线)2010年江苏省灌南县第二高级中学高二下学期期末考试化学试题(已下线)2010年黑龙江牡丹江一中高一上学期期中考试化学试卷(已下线)2010—2011学年福建省安溪一中、养正中学高二下学期期末联考化学试卷(理)(已下线)2012届甘肃省天水市二中高三模拟(5月)考试化学试卷(已下线)2013-2014学年辽宁省抚顺市六校联合体高二下学期期末考试化学试卷2016届内蒙古巴彦淖尔市第一中学高三上学期9月月考化学试卷2017届广东省仲元中学高三上9月月考化学试卷黑龙江省大庆铁人中学2017-2018学年高一上学期期中考试化学试题1江西省九江市第一中学2017-2018学年高一上学期期中考试化学试题黑龙江省大庆铁人中学2017-2018学年高一上学期期中考试化学试题2【全国百强校】内蒙古自治区集宁一中2018-2019学年高一上学期12月月考化学试题四川省广元市川师大万达中学2018-2019学年高一上学期11月月考化学试题【全国百强校】云南省云天化中学2018-2019学年高一上学期期末考试化学试题云南省弥勒市第四中学2019-2020学年高二上学期开学考试化学试题山东省滨州市邹平双语学校2019年高一上学期《氧化还原专题》检测广东省深圳市实验中学2019-2020学年高一上学期期中考试化学试题江西省山江湖协作体2019-2020学年高一上学期第三次月考(统招班)化学试题云南省红河州泸西一中2019-2020学年高一上学期期中考试化学试题广东省梅州市兴宁市第一中学2019-2020学年高一上学期第二次月考化学试题山西省怀仁市重点中学2019-2020学年高一上学期期末考试化学试题鲁教版高中化学必修1第二章《元素与物质世界》测试卷1人教版高中化学必修1第二章《化学物质及其变化》测试卷5云南省普洱市墨江第二中学2019-2020学年高一上学期期末考试化学试题人教版(2019)高一必修第一册第一章 物质及其变化 素养拓展区甘肃省天水市一中2020-2021学年高一下学期开学考试化学试题黑龙江省大庆中学2020—2021学年高一下学期开学考试化学试题安徽省合肥市第六中学2021-2022学年高一上学期第一次月考化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高一上学期期末考试化学试题云南省曲靖市会泽县实验高级中学校2022-2023学年高一上学期12月月考化学(理)试题
名校
解题方法
4 . 碳酸亚铁(白色固体,难溶于水)是一种重要的工业原料,可用于制备补血剂乳酸亚铁,也可用作可充电电池的电极。某研究小组通过下列实验,寻找利用复分解反应制备 的最佳方案:
的最佳方案:
(1)实验Ⅰ中红褐色沉淀的化学式为___________ 。
(2)实验Ⅱ中产生白色沉淀 及少量无色气泡的离子方程式为
及少量无色气泡的离子方程式为___________ 。
(3)小组同学讨论认为,定性实验现象并不能直接证明实验Ⅲ中 的纯度最高,需要利用如图所示的装置进行定量测定。
的纯度最高,需要利用如图所示的装置进行定量测定。 处的广口瓶中,经一系列操作后,称量装置
处的广口瓶中,经一系列操作后,称量装置 的增重来测定沉淀中
的增重来测定沉淀中 的纯度。
的纯度。
①仪器 的名称为
的名称为___________ ,所盛试剂应选择下列试剂中的___________ (填字母),请写出 中
中 发生反应的离子方程式
发生反应的离子方程式___________ 。
A.稀盐酸 B.稀硝酸 C.稀硫酸
②B中浓硫酸的作用为___________ ,若无该装置,则测定结果会___________ (填“偏大”“偏小”或“无影响”);D中碱石灰的作用为___________ 。
③在 中充分反应后打开左侧止水夹通入一段时间的
中充分反应后打开左侧止水夹通入一段时间的 ,其目的是
,其目的是___________ 。
(4)实验反思:经测定,实验Ⅲ中的 纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备
纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备 实验成功的关键因素是
实验成功的关键因素是___________ 。
 的最佳方案:
的最佳方案:| 实验 | 试剂 | 现象 | |
| 滴管(一滴管) | 试管(2mL) | ||
|  溶液 溶液 |  溶液 溶液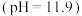 | 实验Ⅰ:立即产生灰绿色沉淀,5min后出现明显的红褐色 |
 溶液 溶液 | 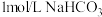 溶液 溶液 | 实验Ⅱ:产生白色沉淀及少量无色气 泡,2min 后出现明显的灰绿色 | |
 溶液 溶液 |  溶液 溶液 | 实验Ⅲ:产生白色沉淀及无色气泡,较长时间保持白色 |
(1)实验Ⅰ中红褐色沉淀的化学式为
(2)实验Ⅱ中产生白色沉淀
 及少量无色气泡的离子方程式为
及少量无色气泡的离子方程式为(3)小组同学讨论认为,定性实验现象并不能直接证明实验Ⅲ中
 的纯度最高,需要利用如图所示的装置进行定量测定。
的纯度最高,需要利用如图所示的装置进行定量测定。
 处的广口瓶中,经一系列操作后,称量装置
处的广口瓶中,经一系列操作后,称量装置 的增重来测定沉淀中
的增重来测定沉淀中 的纯度。
的纯度。①仪器
 的名称为
的名称为 中
中 发生反应的离子方程式
发生反应的离子方程式A.稀盐酸 B.稀硝酸 C.稀硫酸
②B中浓硫酸的作用为
③在
 中充分反应后打开左侧止水夹通入一段时间的
中充分反应后打开左侧止水夹通入一段时间的 ,其目的是
,其目的是(4)实验反思:经测定,实验Ⅲ中的
 纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备
纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析,制备 实验成功的关键因素是
实验成功的关键因素是
您最近一年使用:0次
5 . SiO2、KNO3能与分解出的金属钠发生反应生成Na2SiO3,化学方程式为: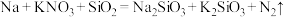 (未配平)
(未配平)
(1)配平化学方程式,并用单线桥法标出电子转移的方向和数目。
___________Na+___________ KNO3+___________ SiO2=___________Na2SiO3+___________K2SiO3+___________N2↑___________
(2)在该反应中KNO3体现___________ (填“氧化性”或“还原性”),Na2SiO3为___________ (填“氧化产物”或“还原产物”)。
(3)当反应转移5mol电子时,生成标准状况下的氮气___________ L。
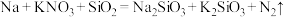 (未配平)
(未配平)(1)配平化学方程式,并用单线桥法标出电子转移的方向和数目。
___________Na+___________ KNO3+___________ SiO2=___________Na2SiO3+___________K2SiO3+___________N2↑
(2)在该反应中KNO3体现
(3)当反应转移5mol电子时,生成标准状况下的氮气
您最近一年使用:0次
名校
6 . 某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)甲组同学通过研究 对
对 稳定性的影响,得到如图所示结果,增强
稳定性的影响,得到如图所示结果,增强 稳定性的措施为
稳定性的措施为___________ 。

乙组同学为探究 与的反应,进行如图所示实验:
与的反应,进行如图所示实验:

(2) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.的化学性质与 相似;
相似;
iii.
实验方案如下:
(3) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(4) 可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?
”的结论?___________ (填“能”或“否”)请说明理由___________ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)甲组同学通过研究
 对
对 稳定性的影响,得到如图所示结果,增强
稳定性的影响,得到如图所示结果,增强 稳定性的措施为
稳定性的措施为
乙组同学为探究
 与的反应,进行如图所示实验:
与的反应,进行如图所示实验:
(2)
 与
与 反应的离子方程式为
反应的离子方程式为为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.的化学性质与
 相似;
相似;iii.

实验方案如下:
| 实验方案 | 实验现象 |
步骤1:取 溶液,向其中滴加3滴 溶液,向其中滴加3滴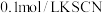 溶液 溶液 | 无明显现象 |
步骤2:取 溶液,向其中滴加3滴 溶液,向其中滴加3滴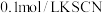 溶液 溶液 | 产生白色沉淀 |
 与
与 反应的离子方程式为
反应的离子方程式为(4)
 可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
 转化为
转化为 ”的结论?
”的结论?
您最近一年使用:0次
名校
7 . 金属的性质
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
(2)我国自主研发的大飞机C919大量使用了铝锂合金。这是利用了铝锂合金的下列性质___________
(3)常温下,将铁片放到浓硫酸中,一段时间后___________
(4)下列关于碳酸钠和碳酸氢钠的叙述正确的是___________
(5)实验室测定氧化物X(FexOy)的组成实验如下:

下列有关说法正确的是___________
金属材料在人类社会发展中起到了举足轻重的作用,因为它具有比其他材料更优越的综合性能,能够更适应科技和生活方面提出的各种不同的要求。
(1)向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是___________
| A.钠沉入水底 | B.钠熔成小球 |
| C.发出“嘶嘶”声音 | D.溶液变红 |
| A.低强度 | B.低密度 | C.导热性 | D.熔点低 |
| A.溶液呈棕黄色 | B.铁片质量减轻 |
| C.有大量气泡产生 | D.铁片表面生成致密氧化膜 |
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,热稳定性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应的速率:碳酸钠>碳酸氢钠 |
| D.一定条件下,碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |

下列有关说法正确的是___________
A.样品X中含有+2价铁元素 |
B.溶液 中 中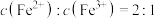 |
C.溶液 中的离子只有 中的离子只有 和 和 |
D.根据步骤I、II可判断 为 为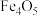 |
您最近一年使用:0次
名校
8 . 元素周期律
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
(2) 的电子式正确的是________
的电子式正确的是________
(3)有关N、O两种元素,下列排序错误的是________
(4)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是________
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
A. | B. | C. | D. |
 的电子式正确的是________
的电子式正确的是________A.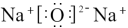 | B. |
C.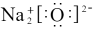 | D. |
| A.元素的最高化合价:O>N | B.简单氢化物的稳定性: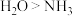 |
| C.元素的电负性:O>N | D.离子半径: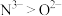 |
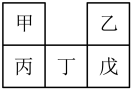
| A.原子半径:丁>戊>乙 |
| B.非金属性:戊>丁>丙 |
| C.甲的氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E、F为短周期元素,其中C的原子序数最小,它们的最高正价与原子半径关系如图所示。

回答下列问题:
(1)F离子结构示意图为_______ ;化合物EF2的化学式为_______ 。
(2)从原子结构角度解释A金属性强于B的原因:_______ 。
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为_______ ,写出CE2在足量O2中燃烧的化学方程式_______ 。
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有_______ (填“离子键”、“极性键”或“非极性键”)。
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为_______ 。

回答下列问题:
(1)F离子结构示意图为
(2)从原子结构角度解释A金属性强于B的原因:
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 .  气体可处理污水中的
气体可处理污水中的 ,以下是
,以下是 的两种制备方法:
的两种制备方法:
方法一:
方法二:
(1) 与
与 (C是+2价)反应产生2种无毒气体,反应中氧化剂和还原剂物质的量之比为
(C是+2价)反应产生2种无毒气体,反应中氧化剂和还原剂物质的量之比为_______ 。
(2)请评价上述哪一种方法制备的 更适合用于饮用水的消毒。
更适合用于饮用水的消毒。_____________
 气体可处理污水中的
气体可处理污水中的 ,以下是
,以下是 的两种制备方法:
的两种制备方法:方法一:

方法二:

(1)
 与
与 (C是+2价)反应产生2种无毒气体,反应中氧化剂和还原剂物质的量之比为
(C是+2价)反应产生2种无毒气体,反应中氧化剂和还原剂物质的量之比为(2)请评价上述哪一种方法制备的
 更适合用于饮用水的消毒。
更适合用于饮用水的消毒。
您最近一年使用:0次




