1 . 氨水中存在的主要溶质微粒是NH3·H2O。
已知:常温下,醋酸和NH3·H2O的电离平衡常数均为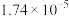
(1)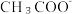 结合H+的能力
结合H+的能力___________  结合OH-的能力(填“>”“=”或“<”),则
结合OH-的能力(填“>”“=”或“<”),则 溶液呈
溶液呈___________ 性。
(2)为证明一水合氨是弱电解质,甲乙丙三位同学利用下面的试剂进行实验:
试剂: 氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
①甲用pH试纸测出 氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?
氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?___________ (“正确”或“错误”)。
②乙取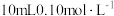 氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b
氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b___________ 2(填“>”“=”或“<”)即可确认一水合氨是弱电解质。
③丙取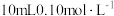 氨水,滴入2滴酚酞试液,显粉红色,再加入
氨水,滴入2滴酚酞试液,显粉红色,再加入 晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质
晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质___________ (填“能”或“否”)。
(3)常温下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
①温度升高, 的电离平衡向
的电离平衡向___________ 方向移动,能支持该结论的表中数据是___________ 。
a.电离常数 b.电离程度 c.c(OH⁻) d.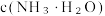
②表中c(OH-))基本不变的原因是___________ 。
③常温下,在氨水中加入少量的氯化铵晶体,下列说法错误的是___________ 。
a.溶液的pH增大 b. 减小 c.
减小 c.  减小
减小
已知:常温下,醋酸和NH3·H2O的电离平衡常数均为
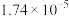
(1)
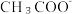 结合H+的能力
结合H+的能力 结合OH-的能力(填“>”“=”或“<”),则
结合OH-的能力(填“>”“=”或“<”),则 溶液呈
溶液呈(2)为证明一水合氨是弱电解质,甲乙丙三位同学利用下面的试剂进行实验:
试剂:
 氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。①甲用pH试纸测出
 氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?
氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?②乙取
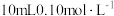 氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b
氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b③丙取
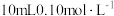 氨水,滴入2滴酚酞试液,显粉红色,再加入
氨水,滴入2滴酚酞试液,显粉红色,再加入 晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质
晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质(3)常温下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
| 温度 | c(NH₃·H₂O)/mol·L⁻¹ | 电离常数 | 电离程度 | c(OH~)/mol·L⁻¹ |
| 0℃ | 16.56 | 1.37×10˜5 | 9.098% | 1.507×10⁻² |
| 10℃ | 15.16 | 1.57×10˜5 | 10.18% | 1.543×10⁻² |
| 20℃ | 13.63 | 1.71×10~5 | 11.2% | 1.527×10⁻² |
 的电离平衡向
的电离平衡向a.电离常数 b.电离程度 c.c(OH⁻) d.
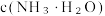
②表中c(OH-))基本不变的原因是
③常温下,在氨水中加入少量的氯化铵晶体,下列说法错误的是
a.溶液的pH增大 b.
 减小 c.
减小 c.  减小
减小
您最近一年使用:0次
名校
解题方法
2 .  和
和 在生产、生活和科学研究中有着广泛的应用,也是大气主要污染物。硫酸盐(含
在生产、生活和科学研究中有着广泛的应用,也是大气主要污染物。硫酸盐(含 、
、 )气溶胶是
)气溶胶是 的成分之一,
的成分之一, 在
在 催化作用下与空气中的
催化作用下与空气中的 在接触室中发生可逆反应,反应的热化学方程式表示为:
在接触室中发生可逆反应,反应的热化学方程式表示为: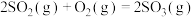
 。向
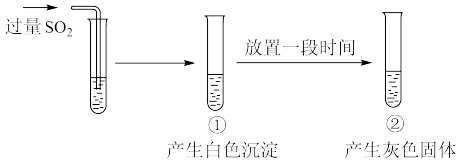
。向 溶液中通入过量
溶液中通入过量 ,过程和现象如下图。经检验,白色沉淀为
,过程和现象如下图。经检验,白色沉淀为 ;灰色固体中含有Ag。下列说法
;灰色固体中含有Ag。下列说法不正确 的是
 和
和 在生产、生活和科学研究中有着广泛的应用,也是大气主要污染物。硫酸盐(含
在生产、生活和科学研究中有着广泛的应用,也是大气主要污染物。硫酸盐(含 、
、 )气溶胶是
)气溶胶是 的成分之一,
的成分之一, 在
在 催化作用下与空气中的
催化作用下与空气中的 在接触室中发生可逆反应,反应的热化学方程式表示为:
在接触室中发生可逆反应,反应的热化学方程式表示为: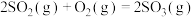
 。向
。向 溶液中通入过量
溶液中通入过量 ,过程和现象如下图。经检验,白色沉淀为
,过程和现象如下图。经检验,白色沉淀为 ;灰色固体中含有Ag。下列说法
;灰色固体中含有Ag。下列说法
A.①中生成白色沉淀的离子方程式为: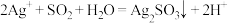 |
B.①中未生成 ,证明溶度积: ,证明溶度积: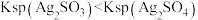 |
C.②中的现象体现了 的氧化性 的氧化性 |
D.该实验条件下, 与 与 反应生成 反应生成 的速率大于生成Ag的速率 的速率大于生成Ag的速率 |
您最近一年使用:0次
2022-11-24更新
|
275次组卷
|
2卷引用:天津外国语大学附属外国语学校2022-2023学年高二上学期期末考化学试题
名校
解题方法
3 . Ⅰ. 溶液与
溶液与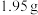 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为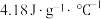 、溶液的密度均近似为
、溶液的密度均近似为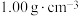 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_______  。
。
(2)反应 的
的
_______  。
。
(3)可以证明乙酸是弱酸的事实是_______(填序号)
(4)有下列物质的溶液:a. b.
b. c.
c. d.
d. 。若四种溶液的物质的量浓度相同,其
。若四种溶液的物质的量浓度相同,其 由大到小顺序为
由大到小顺序为_______ (用字母序号表示,下同)。若四种溶液的 相同,其物质的量浓度由大到小顺序为
相同,其物质的量浓度由大到小顺序为_______ 。
(5)常温下,有 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)

Ⅱ.纯过氧化氢( )是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
)是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
(6)该兴趣小组的同学查阅资料后发现 为二元弱酸,其酸性比碳酸弱。写出
为二元弱酸,其酸性比碳酸弱。写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
(7)同学们用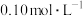 的
的 标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为
标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为 。
。
①在该反应中, 被
被_______ (填“氧化”或“还原”)。
②用移液管吸取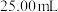 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性
试样置于锥形瓶中,重复滴定四次,每次消耗的酸性 标准溶液体积如下表所示:
标准溶液体积如下表所示:
则试样中过氧化氢的浓度为_______  。
。
③若滴定前尖嘴中有气泡,滴定后消失,则测定结果_______ (填“偏低”“偏高”或“不变”)。
(8)同学们发现向滴加了酚酞的NaOH溶液中加入 后,溶液中红色消失。关于褪色原因,甲同学认为
后,溶液中红色消失。关于褪色原因,甲同学认为 是二元弱酸,消耗了
是二元弱酸,消耗了 使红色消失;乙同学认为
使红色消失;乙同学认为 具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:
具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:_______ 。
 溶液与
溶液与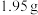 锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为
锌粉在量热计中充分反应。测得反应前温度为20.1℃,反应后最高温度为30.1℃。已知:反应前后,溶液的比热容均近似为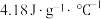 、溶液的密度均近似为
、溶液的密度均近似为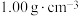 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:(1)反应放出的热量Q=
 。
。(2)反应
 的
的
 。
。(3)可以证明乙酸是弱酸的事实是_______(填序号)
| A.乙酸钠水溶液显碱性 | B.在乙酸水溶液中含有未电离的乙酸分子 |
C.乙酸与 溶液反应放出 溶液反应放出 气体 气体 | D.常温下, 的乙酸水溶液pH为3 的乙酸水溶液pH为3 |
 b.
b. c.
c. d.
d. 。若四种溶液的物质的量浓度相同,其
。若四种溶液的物质的量浓度相同,其 由大到小顺序为
由大到小顺序为 相同,其物质的量浓度由大到小顺序为
相同,其物质的量浓度由大到小顺序为(5)常温下,有
 相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
Ⅱ.纯过氧化氢(
 )是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:
)是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体,用途广泛。回答下列问题:(6)该兴趣小组的同学查阅资料后发现
 为二元弱酸,其酸性比碳酸弱。写出
为二元弱酸,其酸性比碳酸弱。写出 在水溶液中的电离方程式:
在水溶液中的电离方程式:(7)同学们用
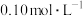 的
的 标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为
标准溶液(硫酸酸化)滴定某试样中过氧化氢的含量,反应原理为 。
。①在该反应中,
 被
被②用移液管吸取
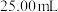 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性
试样置于锥形瓶中,重复滴定四次,每次消耗的酸性 标准溶液体积如下表所示:
标准溶液体积如下表所示:| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
则试样中过氧化氢的浓度为
 。
。③若滴定前尖嘴中有气泡,滴定后消失,则测定结果
(8)同学们发现向滴加了酚酞的NaOH溶液中加入
 后,溶液中红色消失。关于褪色原因,甲同学认为
后,溶液中红色消失。关于褪色原因,甲同学认为 是二元弱酸,消耗了
是二元弱酸,消耗了 使红色消失;乙同学认为
使红色消失;乙同学认为 具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:
具有漂白性使溶液褪色(酚酞生成了其他物质)。请设计一个简单的实验方案判断甲、乙同学的说法是否正确:
您最近一年使用:0次
名校
4 . 对于 H2O2 分解反应,Cu2+也有一定的催化作用。为比较 Fe3+和 Cu2+对 H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。下列说法不正确的是

| A.图甲可通过观察气泡产生快慢来比较反应速率的大小 |
| B.用图乙装置测定反应速率时,若 10s 产生标况下氢气 22.4ml,则用氢气表示的10s 内反应速率为 0.0001mol·s-1 |
| C.图甲所示实验中,若左边试管里的反应速率大于右边的,则证明 Fe3+对 H2O2 分解的催化效果比 Cu2+的好 |
| D.为检查乙装置的气密性,可关闭 a 处旋塞,将注射器活塞拉出一定距离,一段时间后松 开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2021-10-16更新
|
306次组卷
|
3卷引用:天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题
名校
5 . 下列说法不正确的是
| A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,容量瓶水洗后不用润洗 |
| B.因为盐的水解是吸热过程,所以加热可提高盐的水解速率 |
C.为了证明氯化铵溶液可促进 固体的溶解,可向两份等量 固体的溶解,可向两份等量 固体中分别加入等体积蒸馏水和 固体中分别加入等体积蒸馏水和 溶液 溶液 |
D.在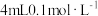 的 的 溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 溶液中滴加数滴1mol/L的NaOH溶液,溶液颜色从橙色变成黄色 |
您最近一年使用:0次
6 . 下列说法中正确的是( )
| A.饱和石灰水中加入一定量生石灰,溶液温度明显升高,pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s)  Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度减小 |
| C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI) |
| D.硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可以完全除去其中的Ca2+、Mg2+ |
您最近一年使用:0次
2019-12-03更新
|
127次组卷
|
9卷引用:天津市滨海新区大港油田第三中学2020-2021学年高二上学期期中考试化学试题
天津市滨海新区大港油田第三中学2020-2021学年高二上学期期中考试化学试题(已下线)浙江省南马高中2009-2010学年高二下学期第一次月考化学试题江西省南康中学、于都中学2017-2018学年高二上学期第四次联考化学试题吉林省松原市长岭县第三中学2021-2022学年高二上学期第三次考试化学试题(已下线)2014年高考化学苏教版总复习 8-4 难溶电解质的溶解平衡练习卷2016届宁夏银川市第二中学高三上学期统练(三)化学试卷(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》广东省肇庆市广宁第一中学2021届高三上学期9月月考化学试题河北省石家庄市藁城区第一中学2020届高三上学期第三次月考化学试题
名校
7 . 磷酸氯喹(结构如图所示)可用于治疗新冠肺炎,临床证明磷酸氯喹对治疗“新冠肺炎”有良好的疗效。2020年3月4日印发的《新型冠状病毒肺炎诊疗方案(试行第七》版中)明确规定了其用量。磷酸氯喹的结构如图所示,下列关于磷酸氯喹的说法错误的是
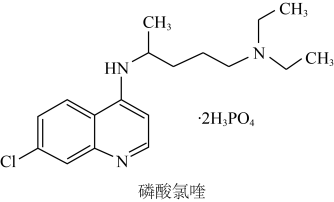

| A.化学式为C18H33ClN3O8P2 |
| B.1mol磷酸氯喹能与5molH2发生加成反应 |
| C.分子中的—C1被—OH取代后的产物能与溴水作用 |
| D.可以发生取代反应、加成反应和氧化反应 |
您最近一年使用:0次
2020-07-13更新
|
331次组卷
|
2卷引用:天津市第一中学2019-2020学年高二下学期期末考试化学试题
名校
8 . 丁子香酚可用于制备杀虫剂和防腐剂,结构简式如图所示。下列说法中,不正确的是


| A.丁子香酚分子中的含氧官能团是羟基和醚键 |
| B.1 mol 丁子香酚与足量氢气加成时,最多能消耗 4 mol H2 |
| C.1mol丁子香酚与浓溴水反应,最多消耗 2 mol Br2 |
| D.丁子香酚能使酸性 KMnO4 溶液褪色,可证明其分子中含有碳碳双键 |
您最近一年使用:0次
9 . 下列有关实验的说法中正确的是( )
| A.向丙烯醛(CH2=CH-CHO)中滴入KMnO4酸性溶液,若紫色褪去,就能证明结构中存在碳碳双键 |
| B.实验时手指不小心沾上苯酚,立即用酒精清洗 |
| C.将电石与水反应产生的气体通入溴水中,溴水褪色,就能证明乙炔和溴水发生了加成反应 |
| D.将(CH3)2CHOH与NaOH的醇溶液共热制备CH3-CH=CH2 |
您最近一年使用:0次
10 . 下列实验处理可行的有几项
①将CH3CH(OH)CHO与NaOH的醇溶液共热制备CH3CH=CH2
②向丙烯醛(CH2=CHCHO)中加入溴水,观察橙色褪去,能证明结构中存在碳碳双键
③实验时手指不小心沾上苯酚,立即用乙醇冲洗,再用水冲洗
④用溴水除去混在苯中的己烯,分液得到纯净的苯
⑤利用重结晶法可以提纯含有少量NaCl的苯甲酸
⑥在分别盛有少量苯和四氯化碳的试管中加碘水后振荡,可根据现象区分苯和四氯化碳
⑦向含有苯酚的苯中加入碳酸钠溶液,反应后分液,可除去苯中的少量苯酚
⑧用碳酸钠溶液可区分乙醇、甲苯、乙酸、溴乙烷和苯
⑨煤油的主要成分为烃类物质,可用来保存金属钠
①将CH3CH(OH)CHO与NaOH的醇溶液共热制备CH3CH=CH2
②向丙烯醛(CH2=CHCHO)中加入溴水,观察橙色褪去,能证明结构中存在碳碳双键
③实验时手指不小心沾上苯酚,立即用乙醇冲洗,再用水冲洗
④用溴水除去混在苯中的己烯,分液得到纯净的苯
⑤利用重结晶法可以提纯含有少量NaCl的苯甲酸
⑥在分别盛有少量苯和四氯化碳的试管中加碘水后振荡,可根据现象区分苯和四氯化碳
⑦向含有苯酚的苯中加入碳酸钠溶液,反应后分液,可除去苯中的少量苯酚
⑧用碳酸钠溶液可区分乙醇、甲苯、乙酸、溴乙烷和苯
⑨煤油的主要成分为烃类物质,可用来保存金属钠
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次



