名校
解题方法
1 . 已知冰醋酸能与Cl2在I2催化下发生反应生成ClCH2COOH和HCl。对实验过程进行监测,发现反应过程中出现了C―I键,下列有关说法错误的是
| A.实验中C―I键的产生,可通过红外光谱结果证明 |
B.ClCH2COOH中存在 键 键 |
| C.C―I键比C―Cl键更易形成,且键能更大 |
D. 与 与 的空间构型相似 的空间构型相似 |
您最近一年使用:0次
名校
2 . 下列说法不正确 的是
| A.常温下,测定0.1mol·L-1醋酸溶液的pH可证明醋酸是弱电解质 |
| B.相同温度下,与相同浓度、相同体积的盐酸和醋酸溶液恰好中和时消耗NaOH的物质的量相同 |
| C.由反应NaR+CO2(少量)+H2O=HR+NaHCO3可知:Ka1(H2CO3)>Ka(HR)>Ka2(H2CO3) |
| D.等体积pH=2的两种酸分别与足量的铁反应,单位时间内酸性较强的酸与铁反应速率更快 |
您最近一年使用:0次
名校
3 . Ⅰ.化学电源在生产生活中有着广泛的应用,请回答下列问题。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是______。
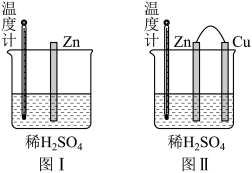
(2)为了探究化学反应能量变化,某同学设计了两个实验(如图Ⅰ,Ⅱ)。有关实验现象,说法正确的是:_______。
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为:___________ 。
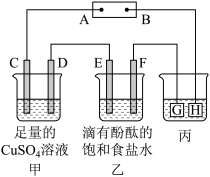
(4)以上述氨燃料电池接下图(甲乙丙) A、B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:_____ ,C电极反应式:_____ ,乙池中发生的离子反应方程式为:_____ ,丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在_____ 处(填G或H)。为证明铁被保护,可先取少量电解后溶液于试管中,向溶液中加入_____ 溶液观察颜色变化。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是______。
A.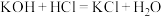 | B. |
C.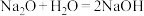 | D. |
(2)为了探究化学反应能量变化,某同学设计了两个实验(如图Ⅰ,Ⅱ)。有关实验现象,说法正确的是:_______。

| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 | B.图Ⅰ和图Ⅱ中温度计示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ中的气泡均产生于锌棒表面 | D.图Ⅱ中产生气体的速率比Ⅰ慢 |
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:
 ,该电池负极的电极反应为:
,该电池负极的电极反应为:(4)以上述氨燃料电池接下图(甲乙丙) A、B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:

您最近一年使用:0次
解题方法
4 .  加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
(1)由 加氢生成
加氢生成 的反应为
的反应为
①若 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
___________ 
②若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高 平衡转化率的措施有
平衡转化率的措施有___________ (写出两种)。
③下列说法可以证明该反应已达到平衡状态的是___________ (填字母)。
a.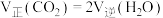 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变
c.容器内气体密度不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2
e.混合气的平均摩尔质量不再变化 f.单位时间内生成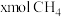 的同时又消耗
的同时又消耗
④ 催化加氢合成
催化加氢合成 过程中,
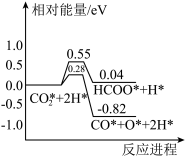
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是___________ 。
(2)一定条件下 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
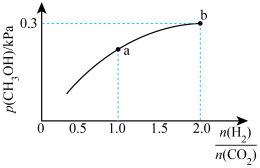
。 的平衡分压与起始投料比
的平衡分压与起始投料比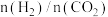 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
___________ 。b点时,再充入 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡___________ (填“正向”、“逆向”或“不”)移动。
(3)一定条件下 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。

提示:CO(或氢气)的选择性
图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:___________ ;400°C时 的体积分数为
的体积分数为___________ 。
 加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。(1)由
 加氢生成
加氢生成 的反应为
的反应为
①若
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热

| 物质 |  |  |  |  |
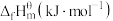 |  | 0 | 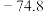 | 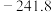 |
 平衡转化率的措施有
平衡转化率的措施有③下列说法可以证明该反应已达到平衡状态的是
a.
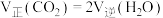 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变c.容器内气体密度不再改变 d.
 和
和 的浓度之比为1:2
的浓度之比为1:2e.混合气的平均摩尔质量不再变化 f.单位时间内生成
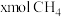 的同时又消耗
的同时又消耗
④
 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是
(2)一定条件下
 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
。 的平衡分压与起始投料比
的平衡分压与起始投料比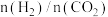 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡
(3)一定条件下
 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。
提示:CO(或氢气)的选择性

图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:
 的体积分数为
的体积分数为
您最近一年使用:0次
名校
解题方法
5 . 下列说法不正确 的是
| A.常温下,测定0.1mol·L-1醋酸溶液的pH可证明醋酸是弱电解质 |
| B.等体积pH=2的两种酸分别与足量的铁反应,单位时间内酸性较强的酸与铁反应速率更快 |
| C.由反应NaR+CO2(少量)+H2O=HR+NaHCO3可知:Ka1(H2CO3)>Ka(HR)>Ka2(H2CO3) |
| D.室温下,pH=2的醋酸溶液和pH=12的氢氧化钠溶液等体积混合,混合溶液显酸性 |
您最近一年使用:0次
6 . 下列关于各图的说法错误的是
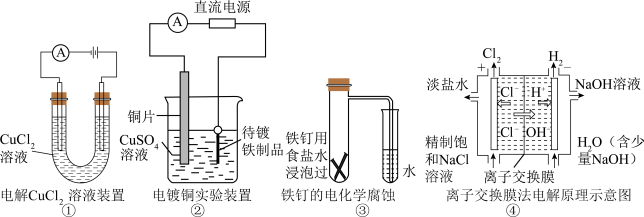

| A.①中阳极处能产生使湿润的淀粉-KI试纸变蓝的气体 |
| B.②中待镀铁制品应与电源负极相连而形成铜镀层 |
| C.③中可证明铁发生了析氢腐蚀 |
D.④中的离子交换膜可以避免生成的 与NaOH溶液反应 与NaOH溶液反应 |
您最近一年使用:0次
2023-10-22更新
|
753次组卷
|
6卷引用:福建省厦门外国语学校2023-2024学年高二上学期期中考试化学试题
7 . 下列说法中,可以证明醋酸是弱电解质的是
A.某温度下,等浓度的醋酸溶液和盐酸,醋酸溶液中水电离出的 浓度较大 浓度较大 |
| B.醋酸溶液连接到一电路中,发现灯泡较暗 |
C.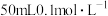 的醋酸溶液恰好中和 的醋酸溶液恰好中和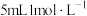 的 的 溶液 溶液 |
| D.稀释醋酸溶液,pH值会增大 |
您最近一年使用:0次
2023-10-11更新
|
349次组卷
|
2卷引用:福建省福清西山学校2023-2024学年高二上学期12月月考化学试题
8 . 探究浓度对化学平衡的影响,某同学进行如图实验。下列说法不正确的是
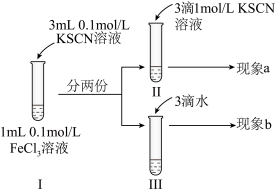

| A.该实验通过观察颜色变化来判断生成物浓度的变化 |
| B.实验Ⅱ中加3滴KSCN溶液后溶液颜色变深,说明平衡常数变大 |
| C.观察到现象a比现象b中红色更深,即可证明增加反应物浓度,平衡正向移动 |
| D.实验Ⅲ加3滴水的目的是保证体积与实验Ⅱ一致,是对比实验 |
您最近一年使用:0次
2023-11-18更新
|
159次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题
名校
解题方法
9 . 有关下列实验的说法正确的是
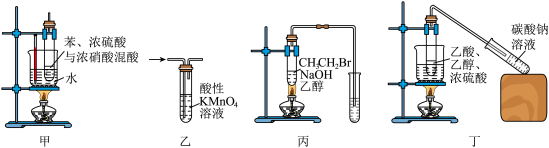

| A.甲装置中试剂的加入顺序为:苯、浓硝酸、浓硫酸 |
B.乙装置可用于提纯混有少量 的 的 |
C.丙装置右侧试管内的酸性 溶液褪色,证明溴乙烷发生了消去反应 溶液褪色,证明溴乙烷发生了消去反应 |
D.丁装置导气管口应在右侧试管中 溶液液面上方,以防止倒吸 溶液液面上方,以防止倒吸 |
您最近一年使用:0次
名校
10 .  遇水极易发生水解。某化学兴趣小组设计实验制备
遇水极易发生水解。某化学兴趣小组设计实验制备 并探究其性质。
并探究其性质。
Ⅰ.氯化铁的制备:
(1)图1为湿法制备的装置,仪器A的名称为___________ ,烧杯中发生反应的离子方程式为___________ 。

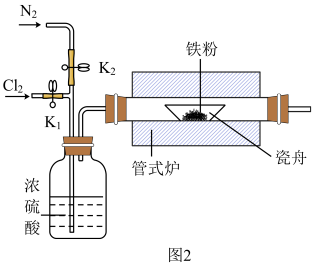
(2)图2为干法制备的装置。反应前后都要鼓入氮气,目的是___________ 。
Ⅱ.氯化铁的性质探究:
(3)查阅资料:氯化铁在水溶液中分多步水解,生成净水性能更好的聚合氯化铁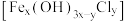 。写出氯化铁水解生成聚合氯化铁的总化学方程式
。写出氯化铁水解生成聚合氯化铁的总化学方程式___________ 。
(4)为了探究外界条件对氯化铁水解平衡的影响,该兴趣小组设计实验方案(忽略溶液体积的变化, 的浓度为1mol/L),获得以下数据:
的浓度为1mol/L),获得以下数据:
①实验1和实验2说明 的水解是
的水解是___________ (填“吸热”或“放热”)反应。
②由实验1和3可知,稀释 溶液,
溶液, 水解平衡
水解平衡___________ (填“正”或“逆”)向移动;结合表中数据,给出判断理由:___________ 。
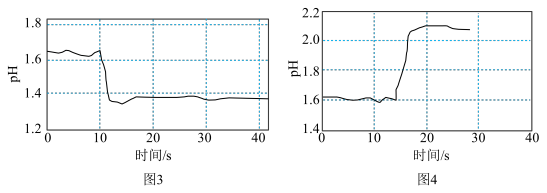
③查阅资料,加入强电解质后,由于溶液中离子总浓度增大,离子间的相互牵制作用增强,水解离子的活性会改变。该兴趣小组同学求助老师,利用计算机手持技术得到实验4和实验5的结果分别如图3和图4所示。
ⅰ.根据上述实验数据和结果,下列说法不正确的是___________ (填标号)。
A.实验过程中量取 溶液时应选用酸式滴定管
溶液时应选用酸式滴定管
B.实验4和实验5中a与b的关系式为
C.根据图3与图4结果可知,离子的水解活性强弱还受离子种类的影响
ⅱ.有同学猜想图3结果是因为氯离子促进了 的水解,请你设计其他简单实验证明该猜想成立:
的水解,请你设计其他简单实验证明该猜想成立:___________ (写出实验操作、现象或结果)。
 遇水极易发生水解。某化学兴趣小组设计实验制备
遇水极易发生水解。某化学兴趣小组设计实验制备 并探究其性质。
并探究其性质。Ⅰ.氯化铁的制备:
(1)图1为湿法制备的装置,仪器A的名称为

(2)图2为干法制备的装置。反应前后都要鼓入氮气,目的是

Ⅱ.氯化铁的性质探究:
(3)查阅资料:氯化铁在水溶液中分多步水解,生成净水性能更好的聚合氯化铁
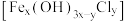 。写出氯化铁水解生成聚合氯化铁的总化学方程式
。写出氯化铁水解生成聚合氯化铁的总化学方程式(4)为了探究外界条件对氯化铁水解平衡的影响,该兴趣小组设计实验方案(忽略溶液体积的变化,
 的浓度为1mol/L),获得以下数据:
的浓度为1mol/L),获得以下数据:| 实验 | 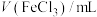 | 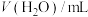 | n(NaCl)/mol | 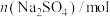 | 温度/℃ | pH |
| 1 | 10.00 | 90.00 | 0 | 0 | 25 | 1.62 |
| 2 | 10.00 | 90.00 | 0 | 0 | 35 | 1.47 |
| 3 | 10.00 | 0 | 0 | 0 | 25 | 0.74 |
| 4 | 10.00 | 90.00 | a | 0 | 25 | x |
| 5 | 10.00 | 90.00 | 0 | b | 25 | y |
 的水解是
的水解是②由实验1和3可知,稀释
 溶液,
溶液, 水解平衡
水解平衡③查阅资料,加入强电解质后,由于溶液中离子总浓度增大,离子间的相互牵制作用增强,水解离子的活性会改变。该兴趣小组同学求助老师,利用计算机手持技术得到实验4和实验5的结果分别如图3和图4所示。

ⅰ.根据上述实验数据和结果,下列说法不正确的是
A.实验过程中量取
 溶液时应选用酸式滴定管
溶液时应选用酸式滴定管B.实验4和实验5中a与b的关系式为

C.根据图3与图4结果可知,离子的水解活性强弱还受离子种类的影响
ⅱ.有同学猜想图3结果是因为氯离子促进了
 的水解,请你设计其他简单实验证明该猜想成立:
的水解,请你设计其他简单实验证明该猜想成立:
您最近一年使用:0次
2024-01-22更新
|
94次组卷
|
2卷引用:福建省福州第三中学2023-2024学年高二上学期1月期末考试化学试题



