名校
1 . 科学家通过X射线证明,MgO、CaO、NiO、FeO的晶体结构与NaCl的晶体结构相似。某同学画出的MgO晶胞结构示意图如图所示,下列说法错误的是


| A.图中的错误的是⑧ |
| B.MgO是优良的耐高温材料,MgO的熔点比CaO的高 |
| C.NiO晶胞中Ni和O周围等距离且最近的O和Ni分别为6、6 |
| D.晶体中与每个O2-距离最近且等距离的O2-有6个 |
您最近一年使用:0次
解题方法
2 . 下列涉及有机物结构与性质的说法错误的是
A.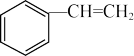 中所有原子可能共平面 中所有原子可能共平面 |
| B.乙烯易与溴水发生加成反应,且1mol乙烯完全加成需要消耗1molBr2,可证明乙烯分子里含有一个碳碳双键 |
| C.1mol乙烯与氯气完全加成后,产物再与氯气发生取代反应,则两个过程中消耗氯气的总物质的量最多是5mol |
D.有机物M(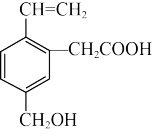 )可发生酯化反应、氧化反应、水解反应等 )可发生酯化反应、氧化反应、水解反应等 |
您最近一年使用:0次
3 . 二甲醚(CH3OCH3)是一种清洁能源由合成气(CO,H2)制备二甲醚的反应原理如下:
反应Ⅰ:CO(g) +2H2(g)⇌CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)⇌CH3OCH3(g) +H2O(g)△H2
回答下列问题:
(1)上述反应符合“原子经济”原则的是____ (填“反应Ⅰ”或“反应Ⅱ”)。下图中使曲线a对应反应按曲线b进行的措施是____ ,该反应自发进行的条件为____ (填“低温”或“高温")。
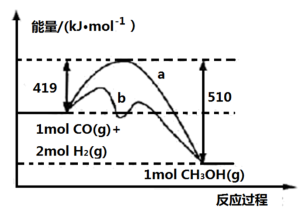
(2)已知△H2=-20.0kJ ·mol-1;H2O(l)=H2O (g)△H= +44.0 kJ·mol-1,则由合成气(CO、H2)制备1 mol CH3OCH3(g),且生成H2O (l)的热化学方程式为____ ;
(3)模拟该制备原理,起始时在某容器中充入2 mol CO和4 mol H2合成CH3OCH3(g),平衡时混合物中氢气的体积分数与温度、压强的关系如下图所示。
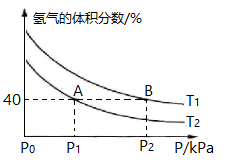
①下列有关说法能够证明恒温恒压时,反应2CO(g) +4H2(g)⇌CH3OCH3(g)+H2O (g)一定达到平衡状态的是 (填序号)___ 。
a.CO和H2的转化率相等
b.反应体系中混合气体密度保持不变
c. c(H2):c( CH3OCH3)的值保持不变
d.反应体系压强保持不变
②上图中T1____ (填“>”、“ <””或“=”,下同)T2;在A、B两点条件下,该反应从开始到平衡时生成二甲醚的平均速率:v (A)_____ v(B)。
③A点对应的CH3OCH3(g)的体积分数为_______ ,B点对应的Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
反应Ⅰ:CO(g) +2H2(g)⇌CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)⇌CH3OCH3(g) +H2O(g)△H2
回答下列问题:
(1)上述反应符合“原子经济”原则的是

(2)已知△H2=-20.0kJ ·mol-1;H2O(l)=H2O (g)△H= +44.0 kJ·mol-1,则由合成气(CO、H2)制备1 mol CH3OCH3(g),且生成H2O (l)的热化学方程式为
(3)模拟该制备原理,起始时在某容器中充入2 mol CO和4 mol H2合成CH3OCH3(g),平衡时混合物中氢气的体积分数与温度、压强的关系如下图所示。

①下列有关说法能够证明恒温恒压时,反应2CO(g) +4H2(g)⇌CH3OCH3(g)+H2O (g)一定达到平衡状态的是 (填序号)
a.CO和H2的转化率相等
b.反应体系中混合气体密度保持不变
c. c(H2):c( CH3OCH3)的值保持不变
d.反应体系压强保持不变
②上图中T1
③A点对应的CH3OCH3(g)的体积分数为
您最近一年使用:0次
2014·全国·一模
解题方法
4 . 下列说法中可以证明反应H2(g)+I2(g) 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是
①单位时间内生成nmol H2的同时生成nmol HI;②一个H-H键断裂的同时有两个H-I键断裂;③百分含量w(HI)=w(I2);④反应速率v(H2)=v(I2)=v(HI);⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1;⑥温度和体积一定时,生成物浓度不再变化;⑦温度和体积一定时,容器内的压强不再变化;⑧条件一定时,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化
 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是①单位时间内生成nmol H2的同时生成nmol HI;②一个H-H键断裂的同时有两个H-I键断裂;③百分含量w(HI)=w(I2);④反应速率v(H2)=v(I2)=v(HI);⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1;⑥温度和体积一定时,生成物浓度不再变化;⑦温度和体积一定时,容器内的压强不再变化;⑧条件一定时,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化
| A.①②③④ | B.②⑥⑨ | C.②⑥⑨⑩ | D.③⑤⑥⑦⑧ |
您最近一年使用:0次
2019-01-30更新
|
375次组卷
|
4卷引用:贵州省长顺县二中2019-2020学年高二上学期期末考试化学试题
贵州省长顺县二中2019-2020学年高二上学期期末考试化学试题2015-2016学年湖北省宜昌市示范高中高二下期中化学试卷(已下线)2014高考名师推荐化学化学平衡的标志2016届福建省三明一中高三上学期第二次月考化学试卷
名校
5 . 在恒容隔热容器中,下列说法可以证明可逆反应N2+3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①1mol N≡N键断裂的同时,有6mol N-H键断裂
②v(H2)=0.9 mol·L-1·min-1,v(NH3)=0.6 mol·L-1·min-1
③保持其他条件不变时,体系气体密度不再改变
④NH3、N2、H2的体积分数都不再改变
⑤体系温度不再改变
 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是①1mol N≡N键断裂的同时,有6mol N-H键断裂
②v(H2)=0.9 mol·L-1·min-1,v(NH3)=0.6 mol·L-1·min-1
③保持其他条件不变时,体系气体密度不再改变
④NH3、N2、H2的体积分数都不再改变
⑤体系温度不再改变
| A.②③④ | B.①③⑤ | C.①④⑤ | D.③④⑤ |
您最近一年使用:0次
2017-12-28更新
|
173次组卷
|
3卷引用:贵州省遵义市第四中学2017-2018学年高二上学期第二次月考化学试题
贵州省遵义市第四中学2017-2018学年高二上学期第二次月考化学试题【全国百强校】贵州省贵阳市第一中学2018-2019学年高二上学期第一次月考化学试题(已下线)黄金30题系列 高二化学(选修4) 小题易丢分
解题方法
6 . 下列操作能达到实验目的的是
| A | B | C | D |
|
|
|
|
| 用酒精萃取碘水中的碘 | 蒸馏实验中将蒸气冷凝为液体 | 混合浓硫酸和乙醇 | 证明乙炔可使酸性高锰酸钾溶液褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
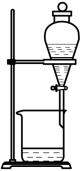
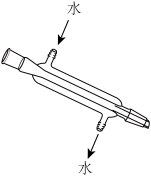
7 . 用甲、乙两个装置都可以制取溴苯,下列说法正确的是
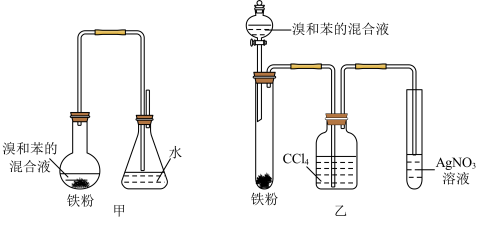

A.反应的化学方程式为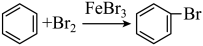 |
| B.反应后圆底烧瓶得褐色混合物,是因为溴苯有颜色 |
| C.乙装置的优点是可证明该反应是取代反应 |
| D.甲装置左侧的长导管只起到导气的作用 |
您最近一年使用:0次
名校
8 . 下列实验方案不能达到实验目的是
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反产生的气体通入溴的四氯化碳溶液 |
| B | 检验卤代烃中卤原子的种类 | 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液滴加硝酸酸化后滴加硝酸银溶液 |
| C | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| D | 验证苯和液溴在FeBr3的催化下发生取代反应 | 将反应产生的混合气体先通入溴的四氯化碳溶液再通入AgNO3溶液中,观察是否有淡黄色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-29更新
|
1032次组卷
|
34卷引用:贵州省贵阳市花溪第六中学2021-2022学年高二下学期诊断性考试化学试题
贵州省贵阳市花溪第六中学2021-2022学年高二下学期诊断性考试化学试题2016-2017学年天津市和平区高二下学期期中质量调查化学试卷人教版高二化学选修5 第二章 烃和卤代烃 第三节 卤代烃练习题天津市武清区杨村第三中学2018-2019学年高二下学期第一次月考化学试题吉林省舒兰市第一高级中学校2018-2019学年高二下学期第一次月考化学试题内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题内蒙古自治区翁牛特旗乌丹第一中学2018-2019学年高二下学期期中考试化学试题山东省聊城市东阿县第一中学2018-2019学年高二第二学期阶段性测试化学试题辽宁省沈阳市郊联体2019-2020学年高二下学期期中考试化学试题云南省玉溪市第一中学2020-2021学年高二上学期第二次月考化学试题重庆市第六十六中学2020-2021学年高二下学期第二次月考化学试题甘肃省民乐县第一中学2021-2022学年高二下学期3月教学质量检测化学试题(已下线)第12讲 卤代烃(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)天津市第二十一中学2021-2022学年高二下学期期中考试化学试题广东省江门市鹤山市第一中学2021-2022学年高二下学期第二次月考化学试题山东省淄博市淄川区般阳中学高二下学期6月学情调研化学试题河北省唐山市第一中学2021-2022学年高二下学期6月份考试化学试题江西省赣州市赣县第三中学2021-2022学年高二下学期4月月考化学试题内蒙古集宁新世纪中学2021-2022学年高二上学期期中考试化学试题(已下线)上海市华东师范大学第二附属中学2022-2023学年高二上学期12月月考化学试题天津市五区县重点校2022-2023学年高二下学期4月期中联考化学试题(已下线)烃的衍生物——课时1卤代烃河北省唐县第一中学2022-2023学年高二下学期5月月考化学试题山东省淄博市第六中学2022-2023学年高二6月月考化学试题河北省唐山市乐亭第一中学2022-2023学年高二下学期6月月考化学试题陕西省宝鸡市渭滨区2022-2023学年高二下学期期末检测化学试题辽宁省七校协作体2023-2024学年高二下学期5月期中联考化学试题辽宁省沈阳市东北育才学校双语校区2023-2024学年高二下学期期中考试化学试题吉林省通化市梅河口市第五中学2023-2024学年高二下学期5月期中化学试题(已下线)第29讲 化学实验方案的设计与评价-2021年高考化学一轮复习名师精讲练(已下线)考点35 卤代烃-备战2023年高考化学一轮复习考点帮(全国通用)云南省蒙自市第一高级中学2022-2023学年高一下学期6月月考化学试题(已下线)考点34 卤代烃(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)黑龙江省牡丹江市第二高级中学2023-2024学年高三上学期8月月考化学试题
名校
解题方法
9 . 食醋是烹饪美食的调味品,有效成分主要为醋酸。醋酸的应用与其电离平衡密切相关。
(1)配制 的醋酸溶液需要用到容量瓶。下列关于容量瓶的操作正确的是_______。
的醋酸溶液需要用到容量瓶。下列关于容量瓶的操作正确的是_______。
(2)为证明醋酸是弱酸,某化学小组设计了如下2个实验:
①实验a中,pH_______ 1(填“>”“<”或“=”)。
②实验b中,测得pH>7,能说明醋酸是弱酸的理由是_______ 。
(3)酸碱中和滴定:常温下,用 溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:

①滴定时,量取NaOH溶液应选用图中的仪器_______ (填标号)。

②滴定盐酸的曲线是图_______ (填“1”或“2”)。
③达到B、D状态时,反应消耗的NaOH溶液的体积a_______ (填“>”“<”或“=”)b。
④向醋酸溶液滴加 溶液至碱性,整个过程中
溶液至碱性,整个过程中 变化情况为
变化情况为_______ (填“增大”、“减小”或“不变”)。
(1)配制
 的醋酸溶液需要用到容量瓶。下列关于容量瓶的操作正确的是_______。
的醋酸溶液需要用到容量瓶。下列关于容量瓶的操作正确的是_______。A. | B. | C. | D. |
| 序号 | 实验 |
| a | 测定的 醋酸溶液的pH 醋酸溶液的pH |
| b | 测定 溶液的pH 溶液的pH |
②实验b中,测得pH>7,能说明醋酸是弱酸的理由是
(3)酸碱中和滴定:常温下,用
 溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
溶液分别滴定20.00mL等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
①滴定时,量取NaOH溶液应选用图中的仪器

②滴定盐酸的曲线是图
③达到B、D状态时,反应消耗的NaOH溶液的体积a
④向醋酸溶液滴加
 溶液至碱性,整个过程中
溶液至碱性,整个过程中 变化情况为
变化情况为
您最近一年使用:0次
名校
解题方法
10 . 1—溴丙烷作为一种有机合成原料,在农药上用于合成有机磷杀虫杀螨剂硫丙磷、丙硫磷、丙溴磷等,也可用于医药、染料、香料工业,以及作为格氏试剂原料。下列关于1—溴丙烷的实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A. | 证明1—溴丙烷发生消去反应有烯烃生成 | 向试管中加入适量的1—溴丙烷和NaOH的乙醇溶液,加热,将反应后产生的气体通入酸性高锰酸钾溶液 |
| B. | 证明1—溴丙烷发生水解反应后NaBr生成 | 将1—溴丙烷与氢氧化钠溶液共热,取反应后溶液先加入硝酸酸化,再加硝酸银溶液 |
| C. | 证明1—溴丙烷发生水解反应后有1—丙醇生成 | 将1—溴丙烷与氢氧化钠溶液共热,取反应后溶液加入一小块金属Na,检验是否有1—丙醇生成 |
| D. | 证明1—溴丙烷发生消去反应有烯烃生成 | 向试管中加入适量的1—溴丙烷和NaOH的水溶液,加热,将反应后产生的气体通入溴的四氯化碳溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次