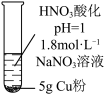
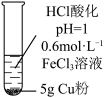
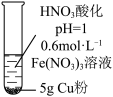
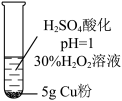
1 . 某课外小组通过如下实验探究铜的还原性。其中溶液体积均为15mL,反应时间均为30min。已知: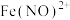 为深棕色。下列说法错误的是
为深棕色。下列说法错误的是
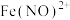 为深棕色。下列说法错误的是
为深棕色。下列说法错误的是| ① | ② | ③ | ④ | |
| 实验 |
|
|
| |
| 现象 | 无明显现象 | Cu粉逐渐溶解,溶液变为蓝绿色 | Cu粉逐渐溶解,溶液变为深棕色,无气泡生成 | Cu粉逐渐溶解,开始有少量气泡,后气泡越来越多,溶液变为蓝色 |
| A.实验①中加入一定量绿矾,铜粉可溶解,溶液变为深棕色 |
B.实验②证明还原性: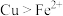 |
C.实验③中存在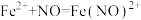 |
| D.实验④中气体可以使新制氯水褪色 |
您最近一年使用:0次
2024-08-12更新
|
241次组卷
|
2卷引用:山东省烟台市2023-2024学年高二下学期7月期末考试化学试题
解题方法
2 . 淀粉水解及产物检验的实验步骤如下。
步骤1:取 淀粉溶液,加入
淀粉溶液,加入 滴稀硫酸,水浴加热
滴稀硫酸,水浴加热 ;
;
步骤2:向步骤1所得溶液中加入 溶液调节
溶液调节 至碱性;
至碱性;
步骤3:再加入少量新制 悬浊液,加热
悬浊液,加热 ,观察到有砖红色沉淀生成;
,观察到有砖红色沉淀生成;
步骤4:取 淀粉溶液,重复步骤3操作,未观察到砖红色沉淀生成。
淀粉溶液,重复步骤3操作,未观察到砖红色沉淀生成。
下列有关说法正确的是
步骤1:取
 淀粉溶液,加入
淀粉溶液,加入 滴稀硫酸,水浴加热
滴稀硫酸,水浴加热 ;
;步骤2:向步骤1所得溶液中加入
 溶液调节
溶液调节 至碱性;
至碱性;步骤3:再加入少量新制
 悬浊液,加热
悬浊液,加热 ,观察到有砖红色沉淀生成;
,观察到有砖红色沉淀生成;步骤4:取
 淀粉溶液,重复步骤3操作,未观察到砖红色沉淀生成。
淀粉溶液,重复步骤3操作,未观察到砖红色沉淀生成。下列有关说法正确的是
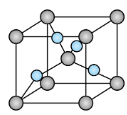
| A.上述实验可证明淀粉水解产生还原性糖 |
B.上图所示的 晶胞中铜原子的配位数为4 晶胞中铜原子的配位数为4 |
| C.向步骤2所得溶液中加入碘水检验水解是否完全 |
| D.步骤1中稀硫酸是淀粉水解的重要反应物之一 |
您最近一年使用:0次
名校
3 . 溴乙烷是重要的化工原料,沸点38.4℃。某兴趣小组设计如下实验装置,利用如下反应制备溴乙烷:NaBr+H2SO4(浓)+C2H5OH→NaHSO4+C2H5Br,并验证可能存在的几种副产物,已知SO2不与Br2的CCl4溶液反应。下列说法错误的是
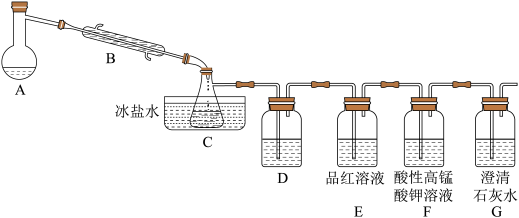
| A.装置C中所得物质可通过水洗-Na2CO3溶液洗-水洗-干燥-蒸馏的方式进行除杂 |
| B.分离提纯过程中将所需产物从分液漏斗下口放出 |
| C.装置D 中盛有Br2的CCl4溶液,用于检验存在副产物乙烯 |
| D.装置G中有白色沉淀的产生即可证明一定有CO2的生成 |
您最近一年使用:0次
名校
解题方法
4 . 某白色粉末可能含有 、
、 、
、 中的一种或几种,现进行如下实验:
中的一种或几种,现进行如下实验:
①将少量粉末加入水中,振荡,得悬浊液;
②向①所得的悬浊液中加入过量的稀盐酸,溶液变澄清,并有气泡产生;
③向②所得的澄清溶液中滴入少量 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
根据上述实验现象,下列说法错误的是
 、
、 、
、 中的一种或几种,现进行如下实验:
中的一种或几种,现进行如下实验:①将少量粉末加入水中,振荡,得悬浊液;
②向①所得的悬浊液中加入过量的稀盐酸,溶液变澄清,并有气泡产生;
③向②所得的澄清溶液中滴入少量
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。根据上述实验现象,下列说法错误的是
A.原白色粉末中一定含有 |
B.不能确定原白色粉末中是否含有 |
C.实验②中发生反应的离子方程式为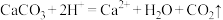 |
D.向实验②所得的澄清溶液中滴加少量淀粉KI溶液,若溶液变蓝,则可证明原白色粉末中一定含有 |
您最近一年使用:0次
5 . 一定条件下在容积不变的容器中充入 和
和 发生如下反应:
发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。已知:
与时间的关系如图所示。已知:

ⅰ.起始投料比 均为2:3;
均为2:3;
ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确的是
 和
和 发生如下反应:
发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。已知:
与时间的关系如图所示。已知:
ⅰ.起始投料比
 均为2:3;
均为2:3;ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确的是
| A.Ⅰ、Ⅱ曲线证明催化剂比表面积对上述反应有影响 |
B.Ⅱ中 的平衡转化率为50% 的平衡转化率为50% |
C.在Ⅲ的条件下,该反应的平衡常数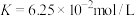 |
D. min,Ⅲ中平均反应速率 min,Ⅲ中平均反应速率 |
您最近一年使用:0次
解题方法
6 . 下列说法不正确的是
| A.欲除去苯中混有的少量苯酚,可向混合液中加入浓溴水,充分反应后,过滤 |
| B.欲除去乙酸乙酯中残留的乙酸,可向混合液中加过量饱和碳酸钠溶液,振荡后静置分液 |
| C.可用煤油、花生油、苯萃取溴水中的溴单质 |
| D.向麦芽糖溶液中加入稀硫酸并加热,再调节pH呈碱性,再加入银氨溶液,水浴加热,有银镜产生,证明麦芽糖发生水解 |
您最近一年使用:0次
解题方法
7 . 设计如下实验探究Fe与AgNO3溶液的反应。下列说法错误的是
| 实验 | 实验操作及现象 |
| ① | 取2 mL 0.1 mol·L-1 AgNO3溶液,加入0.5 g铁粉,溶液无色,再加入铁氰化钾溶液,未观察到蓝色沉淀 |
| ② | 取2 mL 0.1 mol·L-1硝酸酸化的NaNO3溶液,加入0.5g铁粉,溶液变浅绿色,再加入铁氰化钾溶液,有蓝色沉淀 |
| ③ | 取2 mL 0.1 mol·L-1 FeSO4溶液,加入10滴0.1 mol·L-1硝酸酸化的NaNO3溶液,溶液呈浅绿色,再加入KSCN溶液,溶液变为极浅红色 |
| ④ | 取2 mL 0.1 mol·L-1 FeSO4溶液,加入10滴0.1 mol·L-1 AgNO3溶液,溶液呈黄色且有少量黑色颗粒生成,再加入KSCN溶液,溶液变为深红色且有白色沉淀生成 |
| A.实验②证明HNO3只能将Fe氧化为Fe2+ |
| B.实验③出现极浅红色,可能是空气中O2氧化Fe2+生成少量Fe3+ |
| C.向实验③所得溶液中加入1 mL浓硝酸,红色可能加深 |
D.实验③④证明发生反应: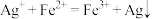 |
您最近一年使用:0次
名校
解题方法
8 . 如图是兴奋剂的某种同系物X的结构,下列关于X的说法正确的是

| A.1 mol X与NaOH溶液反应最多消耗4mol NaOH |
| B.X能使酸性KMnO4溶液褪色,可证明其分子中含有碳碳双键 |
| C.1 mol X与足量的饱和溴水反应,最多消耗6 mol Br2 |
| D.X可与NH4HCO3溶液作用产生气泡 |
您最近一年使用:0次
名校
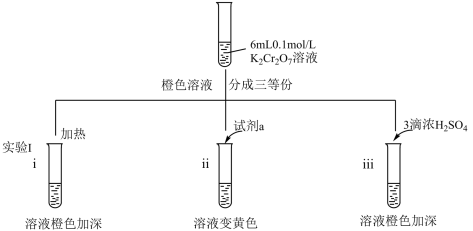
9 . 某兴趣小组以重铬酸钾(K2Cr2O7)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法错误的是
已知:①K2Cr2O7溶液存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
②含铬元素的离子在溶液中的颜色:Cr2O (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。
已知:①K2Cr2O7溶液存在平衡:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。 ②含铬元素的离子在溶液中的颜色:Cr2O
 (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。 
A.i 可证明反应 Cr2O +H2O +H2O 2CrO 2CrO +2H+的正反应放热 +2H+的正反应放热 |
| B.ii 是验证“只降低生成物的浓度,该平衡正向移动”,试剂 a 可以是 NaOH |
| C.iii 平衡逆向移动仅仅是因为增大了生成物的浓度 |
| D.向 iii 所得橙色溶液中加入乙醇,溶液将由橙色变为绿色 |
您最近一年使用:0次
2023-08-26更新
|
442次组卷
|
4卷引用:山东省青岛第一中学2023-2024学年高二上学期10月月考化学试题
名校
10 . 10 mL 0.1 mol·L-1KI溶液与5 mL 0.1 mol·L-1FeCl3溶液发生反应:2Fe3+(aq)+2I-(aq)  2Fe2+(aq)+I2(aq),达到平衡,下列说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡,下列说法不正确的是
 2Fe2+(aq)+I2(aq),达到平衡,下列说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡,下列说法不正确的是| A.加入少量氯化钾固体,平衡不移动 |
| B.加适量水稀释,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该化学反应存在限度 |
D.该反应的平衡常数K=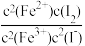 |
您最近一年使用:0次
2023-08-14更新
|
749次组卷
|
2卷引用:山东省鄄城县第一中学2023-2024学年高二上学期9月月考化学试题